
2、非金属元素在周期表中的位置及结构特点
(1) 除H外,非金属元素均在“金属与非金属分界线”的右上方。
(2) 非金属元素(包括稀有元素)均在主族(零族)。
(3) 最外层电子数一般≥4(H、B除外)
(4) 原子半径比同周期金属半径小(稀有元素除外)。
5.酸式盐的种类、性质、形成及其电离与水解。
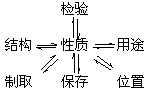 复习方法:(1)每族元素抓住代表物,重点讨论该元素的单质、氧化物、氢化物、酸、碱或盐等有关知识,并理清下列关系:
复习方法:(1)每族元素抓住代表物,重点讨论该元素的单质、氧化物、氢化物、酸、碱或盐等有关知识,并理清下列关系:
(2)运用元素周期表知识比较每族元素与其代表物在结构、性质上的相似性、递变性和特殊性。
4.碳族中碳、硅单质与氧化物的物理性质和化学性质,及其比较,碳酸和硅酸的性质对比碳酸盐与硅酸盐的相互转化及条件。
3.NH3、NO、NO2和硝酸的物理性质和化学性质;硝酸的实验室制法和工业制法。
2.H2S、硫的氧化物和硫酸的物理性质、化学性质,以及H2S和SO2的实验室制法。
1.卤族元素的原子结构,卤族元素的单质与化合物的性质及其速度规律。
1、非金属元素及其化合物知识是中学化学的核心和基础,它几乎贯穿在中学化学的各部分内容之中。这部分的知识要点有:
19.(1)
|
|
(1) |
(2) |
(3) |
(4) |
|
A的分子式 |
CO |
CO |
O2 |
|
|
B的分子式 |
O2 |
CO2 |
CO2 |
|
(2)由于4/3<2<8/3,可知这时A和B有两种组成。
①当A为CO,B为O2时:
设n(CO)=x ,n(O2)=y ,则有16(x+2y)/12x =2 ,解之x=4y,故n(CO)/ n(O2)=4
②当A为CO,B为CO2时,同样方法可解得n(CO)/ n(CO2)=1
18.(1)n=2 m=4 (2) a=119
17.2PbO·PbO2 Pb2 (PbO4) Fe3O4 + 8HCl = 2FeCl3 + FeCl2 + 4H2O
Pb3O4 + 8HCl = 3PbCl2 + Cl2↑+ 4H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com