
2.已知HF的酸性比HCN强。现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,已知前者溶液中离子数目为n1,后者溶液中离子数目为n2。下列关系中正确的是
A.n1=n2 B.n1>n2 C.n1<n2 D.c(F-)>c(CN-)
1.某一元强酸稀溶液和某一元弱碱稀溶液等体积混合后,其pH=7.0。下列叙述正确的是
A.酸溶液的物质的量浓度大于碱溶液
B.酸溶液中H+的浓度大于碱溶液中OH-的浓度
C.酸溶液的物质的量浓度小于碱溶液
D.两种溶液的物质的量浓度相等
11.解释事实:用水解原理可解释诸多相关事实
(1)FeCl3、KAl2(SO4)2·12H2O等可作净水剂
原因:Fe3+、Al3+水解产生少量胶状的Fe(OH)3、Al(OH)3,它们结构疏松、表面积大、吸附能力强,故能吸附水中悬浮的小颗粒而沉降,从而起到净水的作用。
新型水处理剂:Na2FeO4(铁酸钠)的氧化杀菌原理,及还原产物Fe3+水解生成的Fe(OH)3胶体,吸附水中悬浮杂质。
(2)某些化学肥料不能混合使用
如铵态(NH4+)氮肥、过磷酸钙[含Ca(H2PO4)2]均不能与草木灰(主要成分K2CO3)混合使用。
(3) 热的纯碱液去油污效果好
加热能促进纯碱Na2CO3水解,产生的[OH-]较大,而油污中的油脂在碱性较强的条件
下,水解受到促进,故热的比冷的效果好。
(4)在NH4Cl浓溶液中加入Mg粉, Mg溶解,同时放出气体? Mg(OH)2溶于NH4Cl浓溶液中如何解释?在CH3COONH4溶液中加入Mg(OH)2,为何能够溶解?写出反应的离子方程式。
[典型例题]
[例1](2004年北京理综,11)已知0.1 mol·L-1的二元酸H2A溶液的pH=4.0,则下列说法正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
剖析:0.1 mol·L-1的强酸pH=1.0,0.1 mol·L-1的H2A溶液pH=4.0,说明它是一种弱酸。Na2A发生水解A2-+H2O HA-+OH-和HA-+H2O
HA-+OH-和HA-+H2O H2A+OH-,溶液中存在HA-、A2-、H+、OH-;NaHA发生水解HA-+H2O
H2A+OH-,溶液中存在HA-、A2-、H+、OH-;NaHA发生水解HA-+H2O H2A+OH-和电离HA-
H2A+OH-和电离HA- H++A2-,溶液中存在HA-、A2-、H+、OH-,所以两溶液中离子种类相同,A不正确。
H++A2-,溶液中存在HA-、A2-、H+、OH-,所以两溶液中离子种类相同,A不正确。
物质的量相等的Na2A和NaHA因为存在上述水解、电离等过程,阴离子数量发生变化,所以阴离子总量不相等,B不正确。
由电荷守恒可知c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-),C正确。Na2A溶液显碱性,c(OH-)>c(H+),D不正确。
[例2]在常温下10mlpH=10的KOH溶液中,加入pH=4的一元酸HA溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述正确的是
A.c(A-)=c(K+) B.c(H+)=c(OH-)<c(K+)<c(A-)
C.V(混)≥20ml D.V(混)≤20ml
[例3]已知常温下KHSO3溶液的pH<7,且等浓度的HSO3-的电离程度大于SO32-的水解程度。等物质的量的KHSO3、K2SO3、K2SO4溶于足量水形成的溶液中,有关粒子之间的关系正确的是 A.c(SO42-)>c(HSO3-)>c(SO32-) >c(H2SO3)
B.c(K+)>c(SO42-)>c(SO32-)>c(HSO3-)>c(H+)>c(OH-)
C.c(K+)=c(HSO3-)+2c(SO32-)+2c(SO42-)
D.c(K+)+c(H+)=c(HSO3-)+c(SO32-)+c(SO42-)+c(OH-)
[当堂反馈]
10.物质鉴别时要考虑水解。
如:鉴别:NaCl和NaCN
再如:只用一种试剂鉴别:NaHCO3、AlCl3、NaOH、KSCN、AgNO3五种无色溶液
再如:只用一种试剂鉴别:AlCl3、HCl、NaCl、Ba(OH)2
再如:只用一种试剂鉴别:AlCl3、HCl、NaCl、BaCl2
9.除杂
例:除去MgCl2溶液中的Fe3+可在加热搅拌条件下,可加入的一种试剂,后过滤。下列试剂中合适的是
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3 E.MgO F.Mg(OH)2 G.Mg
8.两种盐溶液混合时要考虑水解。
如:①AlCl3和NaHCO3、②AlCl3和NaHS、③Al2(SO4)3和Na2CO3(反应有两种可能性)④Fe2(SO4)3和Na2CO3、⑤AlCl3和NaAlO2、⑥NH4Cl和NaAlO2⑦NH4Cl和NaClO⑧Fe3+和ClO-⑨Al3+和ClO-⑩NaHCO3和NaAlO2(不是发生双水解,而是强酸制弱酸。)
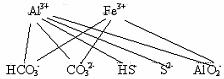
注意:①Fe3+与HS-及S2-发生氧化还原反应。
②CuSO4和Na2S及NaHS发生复分解反应。
7.溶液中各种微粒浓度之间的关系
以Na2S水溶液为例
(1)电荷守恒:
(2)物料守恒:
(3)质子守恒:
6.离子浓度大小的判断
在判断能发生水解的盐溶液中离子浓度大小时,首先要明确绝大部分可溶盐完全电离,电离出的弱离子部分水解(电离强烈、水解微弱);其次要知道多元弱酸分步电离,故其对应盐的水解也是分步进行的,以第一步水解为主;最后还要考虑水的电离。
①多元弱酸溶液,根据分步电离分析。如H3PO4溶液:
②弱酸正盐溶液,根据弱酸根分步水解分析。
ⅰ.当盐中阴、阳离子等价时
[不水解离子]>[水解的离子]>[水解后呈某性的离子]>[显性对应离子]
实例:a. CH3COONa b. NH4Cl
a. b.
ⅱ.当盐中阴、阳离子不等价时
要考虑是否水解,水解分几步。如多元弱酸根的水解,则是“几价分几步,为主第一步”。
实例:Na2S水解分二步:

各种离子浓度大小顺序为:
③不同溶液中同一离子浓度大小的比较,要看溶液中其它离子对其产生的影响。
如在相同物质的量浓度的下列溶液中:①(NH4)2SO4②(NH4)2Fe(SO4)2③(NH4)2CO3。
c(NH4+)由大到小的顺序为
④混合溶液中离子浓度大小的比较,首先要分析混合过程中是否发生化学反应,若发生反应,则要进行过量判断(注意混合后溶液体积的变化);然后再结合电离、水解等因素进行分析。
ⅰ.若酸与碱恰好完全反应,则相当于一种盐溶液。
ⅱ.若酸与碱反应后尚有弱酸或弱碱剩余,则一般弱电解质电离程度>盐的水解程度。
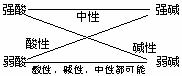
例:将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度的关系是:
,该溶液中NH3•H2O的电离与NH4+的水解相互抑制(缓冲溶液),NH3•H2O电离强于NH4+的水解,所以溶液呈碱性:c(OH-)>c(H+),且c(NH4+)>c(Cl-)
再如:某酸pH为a,某碱pH为b,已知a+b=14,则将两溶液等体积混合后溶液的酸碱性为:
5.某些盐溶液的配制、保存
Na2SiO3、Na2CO3、NH4F等不能贮存磨口玻璃塞的试剂瓶中.因Na2SiO3、Na2CO3水解呈碱性,产生较多OH-,NH4F水解产生HF。OH-、HF均能腐蚀玻璃。
4.判断加热浓缩盐溶液能否得到同溶质的固体
比较:
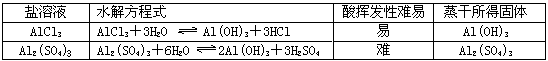 结论:
结论:

[思考] AlCl3、MgCl2、FeCl3、Al2(SO4)3、Fe2(SO4)3、NaAlO2、Na2SO3、NaHCO3、KMnO4等溶液加热蒸干能否得到无水盐?为什么?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com