
3. (2005江苏)氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子
工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C 2AlN+3CO,下列叙述正确的是
2AlN+3CO,下列叙述正确的是
A、在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B、上述反应中每生成2mol AlN,N2得到3mol电子
C、氮化铝中氮元素的化合价为-3价
D、氮化铝晶体属于分子晶体
2.(2005广东综合)下列反应的现象描述与离子方程式都正确的是
A.金属镁与稀盐酸反应,有氢气产生:Mg + 2H++ 2Cl- == MgCl2 + H2↑
B.氯化钡溶液与硫酸反应,有白色沉淀产生;Ba2+ + SO42- == BaSO4↓
C.碳酸钠溶液与盐酸反应,有气泡逸出;Na2CO3 +2H+ == 2Na+ + H2O + CO2↑
D.过量铁粉与氯化铁溶液反应,溶液变浅绿色;Fe + Fe3+ == 2Fe2+
1.(2005广东)铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第6周期。Tl3+与Ag在酸性介质中发生反应:Tl3++ 2Ag ==Tl+ + 2Ag+。下列推断正确的是
A.Tl+ 的最外层有1个电子 B.Tl3+ 的氧化性比Al3+弱
C.Tl能形成+3价和+1的化合物 D.Tl+ 的还原性比Ag强
7、关于KAl(SO4)2和Ba(OH)2反应的原理及图象:
(1)沉淀物质的量变化图象 (2)沉淀质量变化图象
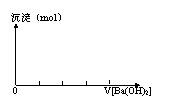
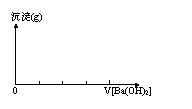
沉淀物质的量最大时反应的化学方程式 沉淀质量最大时反应的化学方程式
课后练习
6、向含等物质的量的Al3+、Mg2+的溶液中先加入NaOH,再加稀盐酸
实验现象:
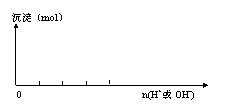 离子方程式:
离子方程式:
5、 AlCl3、MgCl2溶液中加过量的NaOH溶液
AlCl3、MgCl2溶液中加过量的NaOH溶液
实验现象:
离子方程式:
4、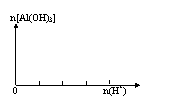 AlO2-与强酸反应
AlO2-与强酸反应
(1)向NaAlO2溶液中逐滴滴入稀盐酸至过量:
实验现象:
离子方程式:
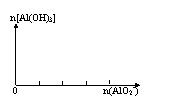
(2)向稀盐酸中逐滴滴入偏铝酸钠溶液至过量:
实验现象:
离子方程式:

(3)向含有NaOH的NaAlO2溶液中逐滴滴入稀盐酸至过量:
实验现象:
离子方程式:
3、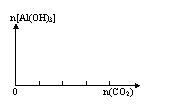 AlO2-与弱酸反应
AlO2-与弱酸反应
向NaAlO2溶液中逐渐通入CO2至过量:
实验现象:
离子方程式:
2、Al3+与强碱反应:
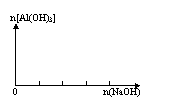 (1)在可溶性铝盐溶液中逐滴滴入NaOH溶液至过量。
(1)在可溶性铝盐溶液中逐滴滴入NaOH溶液至过量。
实验现象:
离子方程式:
(2)向NaOH溶液中逐滴滴入可溶性铝盐溶液至过量。
 实验现象:
实验现象:
离子方程式:
 (3)在含有盐酸的AlCl3溶液中逐滴滴入NaOH溶液至过量。
(3)在含有盐酸的AlCl3溶液中逐滴滴入NaOH溶液至过量。
实验现象:
离子方程式:
1、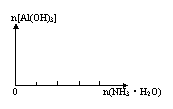 Al3+与弱碱反应:
Al3+与弱碱反应:
在可溶性铝盐溶液中逐滴滴入氨水至过量。
实验现象:
离子方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com