
8.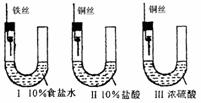 为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在图示的三个装置中,再放置于玻璃钟罩里保存一星期后,下列对实验结束时现象描述不正确的是
为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在图示的三个装置中,再放置于玻璃钟罩里保存一星期后,下列对实验结束时现象描述不正确的是
A.装置Ⅰ左侧的液面一定会上升
B.左侧液面装置Ⅰ比装置Ⅱ的低
C.装置Ⅱ中的铁钉腐蚀最严重
D.装置Ⅲ中的铁钉几乎没被腐蚀
7.用惰性电极电解一定浓度的下列物质的水溶液,通电一段时间后,溶液的pH值增大,向剩余电解液中加适量水,能使溶液与电解前相同的是)
A.NaCl B.CuCl2 C.H2SO4 D.NaOH
6.利用质量均为100.0克的金属铜作电极,电解AgNO3溶液。一段时间后,两电极的质量差为28.00克,则此时阳极和阴极质量(g)分别为
A.100.0 128.0 B.93.60 121.6 C.119.0 91.00 D.88.21 139.8
5.用阳极X和阴极Y电解Z的水溶液,电解一段时间,再加入W,能使溶液恢复到电解前的状态,符合题意的组是(各组物质依次分别为X、Y、Z、W)
A.C、Fe、NaCl、H2O B.Pt、Cu、CuSO4、CuSO4溶液
C.C、C、H2SO4、H2O D.Ag、Fe、AgNO3、AgNO3晶体
4.用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况):从而可知M的原子量为
A.22.4ax/b B.11.2ax/b C.5.6ax/b D.2.5ax/b
3.在铁品上镀一定厚度的锌层,以下方案设计正确的是
A.锌作阳极,镀件作阴极,溶液中含有锌离子
B.铂作阴极,镀件作阳极,溶液中含有锌离子
C.铁作阳极,镀件作阴极,溶液中含有亚铁离子
D.锌作阴极,镀件作阳极,溶液中含有锌离子
2.若某装置(电解池或原电池)中发生反应的离子方程式是:Cu+2H+=Cu2+ +H2↑,关于该装置的有
A.可能是原电池,也可能是电解池 B.只能是原电池,且电解质溶液为硝酸
C.只能是电解池,且金属铜为该电解池的阳极 D.只能是电解池,电解质溶液可以是硝酸
1.下列关于铜电极的叙述正确的是
A.铜锌原电池中铜是正极,锌是负极 B.用电解法精炼粗铜时,粗铜作阴极
C.在镀件上电镀铜时可用金属铜作阳极 D.电解稀硫酸制H2、O2时铜作阳极
6.氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如图所示:

依据上图,完成下列填空:⑴ 在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为____ ___,溶液的pH______(填“升高”或“降低”或“不变”);⑵ 工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为__ ____;⑶ 如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是_____(选填a、b、c);a.Ba(OH)2,b.Ba(NO3)2,c.BaCl2;
⑷ 为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为_____(选填a、b、c);a.先加NaOH,后加Na2CO3,再加钡试剂;b.先加NaOH,后加钡试剂,再加Na2CO3;c.先加钡试剂,后加NaOH,再加Na2CO3;⑸ 脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过_________、冷却、_______(填写操作名称)除去NaCl;⑹ 在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为__________。
课后练习
5.(2002春季12)通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银)︰n(硝酸亚汞)=2︰1,则下列表述正确的是
A.在两个阴极上得到的银和汞的物质的量之比n(银)︰n(汞)=2︰1
B.在两个阳极上得到的产物的物质的量不相等
C.硝酸亚汞的分子式为HgNO3
D.硝酸亚汞的分子式为Hg2(NO3)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com