
8、下列实验中没有白色沉淀或晶体析出的是( )
A. 饱和石灰水中加入少量固体烧碱
B. 向饱和碳酸钠溶液中通入足量CO2
C. 向氯化钙溶液中通入CO2
D. 向氯化钙溶液中通入CO2、NH3
7、2.1克平均分子量为7.2的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加( )
A. 2.1克 B. 3.6克 C. 7.2克 D. 不可求
6、某浅黄色粉末,常用作潜水员的供氧剂.在该供氧反应中,被氧化和被还原的物质的质量比为( )
A. 1:1 B. 2:1 C. 3:1 D. 3:2
5、0.1摩Na2O2、Na2O的混合物溶于水后,刚好被100克7.3%的盐酸中和.则混合物中Na2O2和Na2O的物质的量之比为( )
A. 1:1 B. 2:1 C. 任意比 D. 3:4
4、有50毫升某气体,可能含有CO2、O2、NH3等气体,将其通过浓硫酸没有发现体积变化,通过足量Na2O2后,体积变为30毫升,则该气体的组成为( )
A. CO2为20毫升,NH3为30毫升 B. NH3为40毫升,O2为10诧升
C. CO2为30毫升,O2为20毫升 D. CO2为40毫升,O2为10毫升
3、0.2摩某单质与足量硫在一定条件下充分反应后,质量增加了3.2克,则构成这种单质的元素可能是( )
A. Fe B. K C. Cu D. Mg
2、把6.2克Na2O溶于93.8克水中;把4.6克金属钠溶于95.6克水中;把7.8克Na2O2
溶于93.8克水中;把8克NaOH溶于92克水中,所得到的溶液的质量百分比浓度为( )
A.都是8% B.分别为8%、8%、7%、10%
C.都是9% D.分别为6%、7%、8%、10%
1、已知Li及其化合物的许多性质,与碱金属差异较大,都与Mg相似.下面有关Li
及其化合物性质的叙述不正确的是( )
A. Li在过量O2中燃烧主要产物是Li2O而不是Li2O2
B. Li2CO3受强热很难分解
C. 溶解性 Li2CO3>LiHCO3
D. Li可与N2化合生成Li3N
焰色反应检验金属离子的正确操作方法是 。
焰色反应检验在进行焰色反应时应注意如下几点:①焰色反应所用火焰本身颜色要浅;②蘸取待测物的金属丝本身在火焰上灼烧时应无颜色,同时熔点要高、不易被氧化。用铂丝效果最好;③金属丝在使用前要用稀盐酸将其表面的氧化物洗净,然后在火焰上灼烧至无色(这是因为金属氯化物灼烧时易气化而挥发),以除去能起焰色反应的少量杂质;④观察钾的焰色时,要透过蓝色的钴玻璃片。
典型例题
例1:下列物质性质的比较,正确的是 ( )
A. 热稳定性:Na2CO3 > NaHCO3 > H2CO3
B. 熔点:K > Na >Li
C. 溶解度:NaHCO3 > Na2CO3
D.氧化性:Li+ < Na+ < K+
答案:A
例2:取5.4g由某碱金属(R)及其氧化物(R2O)组成的混合物,使之与足量的水反应,蒸发反应后的溶液,得到8g无水晶体,通过计算
(1)判断该金属是哪一种金属?
(2)原混合物中R和R2O的质量各是多少?
解析:设R的原子量为x

 R
ROH R2O 2ROH
R
ROH R2O 2ROH
x x+17 2x+16 2(x+17)
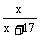 <
<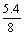 <
<
11<x<35
∴ 该碱金属为Na
设混合物含Na m mol.Na2O n mol.
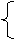 23m+62n=5.4
23m+62n=5.4
m+2n=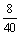
|
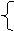
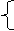 m=0.1 mol
Na:2.3g
m=0.1 mol
Na:2.3g
n=0.05 mol Na2O:3.1g
当堂反馈
(1)碱金属在空气或氧气中燃烧时,由于其活泼性不同、产物也不同。锂燃烧只生成 ,
钠燃烧生成 ,钾、铷、铯等燃烧主要生成 。
(2)钾的密度反而比钠 。
(3)一般来说,酸不稳定,其对应的盐也不稳定,但H2CO3 (填“稳定”或“不稳定”)
而Na2CO3却 (同前)。
(4)金属的置换反应,通常是活泼金属置换 金属。但工业上制取K却是:Na+KCl(熔融)===NaCl+K;在水溶液中,Na、K等金属 (填“能”或“不能”)从CuSO4溶液中置换Cu。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com