
12. 反应2X(g)+Y(g)
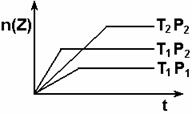
反应2X(g)+Y(g) 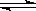 2Z △H<0 在不同温度和压强下,产物Z的物质的量与反应时间的关系如图所示。则下列叙述正确的是
2Z △H<0 在不同温度和压强下,产物Z的物质的量与反应时间的关系如图所示。则下列叙述正确的是
A. T1>T2,P1<P2 B. T1>T2,P1>P2
C. T1<T2,P1>P2 D. T1<T2,P1<P2
11.在一定条件下,发生CO + NO2
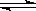 CO2 + NO 的反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是( )
CO2 + NO 的反应,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法中正确的是( )
A、正反应为吸热反应 B、正反应为放热反应
C、降温后CO的浓度增大 D、降温后各物质的浓度不变
10、在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g) 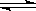
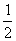 N2(g)+CO2(g);△H=-373.2kJ·mol-1 ,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g);△H=-373.2kJ·mol-1 ,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A. 加催化剂同时升高温度 B. 加催化剂同时增大压强
C. 升高温度同时充入N2 D. 降低温度同时增大压强
9、已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨)+O2(g)=CO2(g) △H=-393.51kJ·mol-1
C(金刚石)+O2(g)=CO2(g) △H=-395.41kJ·mol-1
据此判断,下列说法中正确的是( )
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
8.在一定温度下的密闭容器中, 能表示 A(s)+2B(g) C(g)+D(g) 已达到平衡状态的是(
)
C(g)+D(g) 已达到平衡状态的是(
)
①混合气体的压强,②混合气体的密度,③B的物质的量浓度,④气体的总物质的量,⑤混合气体的平均相对分子质量,⑥v(C)与v(D)的比值
A. ①②③ B. ②③④⑥ C.②③⑤ D.①③④⑤
7.碳铵[(NH4)2CO3]在室温下就能自发地分解产生氨气,对其说法正确的是( )
A、碳铵分解是放热反应,根据能量判据不能自发进行
B、碳铵分解是因为外界给予能量
C、碳酸盐都不稳定,都能自发分解
D、碳铵分解是因为生成了易挥发的气体,使体系的熵值增大
6.在2A + B = 3C + 4D的反应中,下列表示该反应速率最大的是( )
A、VA =0.5mol / (L·min) B、VB =0.3mol / (L·min)
C、VC =0.8mol / (L·min) D、VD = 1mol / (L·min)
5. 已知“凡气体分子总数增多的反应一定是熵增大的反应”。根据所学知识判断,下列反应中,在所有温度下都不自发进行的 A.2O3(g) === 3O2(g) △H<0 B.2CO(g) === 2C(s)+O2(g) △H>0 C.N2(g) + 3H2(g) === 2NH3(g) △H<0 D.CaCO3(s) === CaO(s) + CO2(g) △H>0
4.25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是
A.C(s)+O2(g)=CO(g) △H= ―393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(l) △H= +571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= ―890.3 kJ/mol
D.C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) △H= ―2800 kJ/mol
3.下列说法正确的是
A.热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量
B.热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据
C.书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态
D.凡是化合反应都是放热反应,分解反应都是吸热反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com