
31.

 (8分)
(8分)

 (1)右图表示A、B两种植物的光照等其他条件适宜的情况下,光合作用强度对环境中CO2浓度变化的响应特性。据图判断在CO2浓度为
(1)右图表示A、B两种植物的光照等其他条件适宜的情况下,光合作用强度对环境中CO2浓度变化的响应特性。据图判断在CO2浓度为 ·
· (接近大气CO2浓度)时,光合作用强度较高的植物是_______________。
(接近大气CO2浓度)时,光合作用强度较高的植物是_______________。

 (2)若将上述两种植物幼苗置于同一密闭的玻璃罩中,在光照等其他条件适宜的情况下,一段时间内,生长首先受影响的植物是____________,原因是____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
(2)若将上述两种植物幼苗置于同一密闭的玻璃罩中,在光照等其他条件适宜的情况下,一段时间内,生长首先受影响的植物是____________,原因是____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。

 (3)当植物净固定CO2量为0时,表明植物___________________________________。
(3)当植物净固定CO2量为0时,表明植物___________________________________。
 答案(1)A
答案(1)A
 (2)B 两种植物光合作用强度对CO2浓度变化的响应特性不同,在低浓度CO2条件下,CB植物利用CO2进行光合作用的能力弱,积累光合产物少,故随着玻璃罩中CO2浓度的降低,B植物生长首先受到影响。
(2)B 两种植物光合作用强度对CO2浓度变化的响应特性不同,在低浓度CO2条件下,CB植物利用CO2进行光合作用的能力弱,积累光合产物少,故随着玻璃罩中CO2浓度的降低,B植物生长首先受到影响。
 (3)光合作用固定的CO2量与呼吸释放的CO2量相等
(3)光合作用固定的CO2量与呼吸释放的CO2量相等

 [解析]⑴依题意,在CO2浓度为300μL·L-1时,A植物CO2净固定量较B植物多,因此,此时A植物光合作用强度较B植物高。
[解析]⑴依题意,在CO2浓度为300μL·L-1时,A植物CO2净固定量较B植物多,因此,此时A植物光合作用强度较B植物高。
 ⑵从图中可以看出两种植物对CO2浓度的反应不同,在低浓度下B植物利用CO2进行光合作用的能力较弱,产生的光合产物少,所以随着玻璃罩内CO2浓度的降低,B植物的生长首先受影响。
⑵从图中可以看出两种植物对CO2浓度的反应不同,在低浓度下B植物利用CO2进行光合作用的能力较弱,产生的光合产物少,所以随着玻璃罩内CO2浓度的降低,B植物的生长首先受影响。
 ⑶当植物净固定CO2量为0时,此时光合作用固定的CO2量与呼吸产生的CO2量相等,说明此时光合作用速率与细胞呼吸速率相等。
⑶当植物净固定CO2量为0时,此时光合作用固定的CO2量与呼吸产生的CO2量相等,说明此时光合作用速率与细胞呼吸速率相等。
30. (15分)
(15分)

 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反应如下图所示:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反应如下图所示:




 已知R-CH=CHOH(烯醇)不稳定,很快转化为
已知R-CH=CHOH(烯醇)不稳定,很快转化为 。
。

 根据以上信息回答下列问题:
根据以上信息回答下列问题:

 (1)
A的分子式为
;
(1)
A的分子式为
;

 (2)
反应②的化学方程式是
;
(2)
反应②的化学方程式是
;

 (3)
A的结构简式是
;
(3)
A的结构简式是
;

 (4)
反应①的化学方程式是
(4)
反应①的化学方程式是

 ;
;

 (5)
A有多种同分异构体,写出四个同时满足(i)能发生水解反应(ii)能使溴的四氯化碳溶液褪色两个条件的同分异构体的结构简式:
、
、
、
(5)
A有多种同分异构体,写出四个同时满足(i)能发生水解反应(ii)能使溴的四氯化碳溶液褪色两个条件的同分异构体的结构简式:
、
、
、

 ;
;

 (6)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为
(6)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为

 。
。

 答案
答案


 [解析]本题考查有机物的结构推断和性质,注意结构简式、同分异构体、化学方程式的书写。根据题意,A分子中碳的原子数为4个,氢原子的个数为6个,则氧原子的个数为2个,即A的分子式为C4H6O2。由于A可以发生聚合反应,说明含有碳碳双键,在硫酸存在条件下生成两种有机物,则为酯的水解,即A中含有酯基。根据不饱和度,没有其他功能团。由A的水解产物C和D的关系可判断C与D中的碳原子数相等,均为两个。则A的结构为CH3COOCH=CH2,因此A在酸性条件下水解后得到CH3COOH和CH2=CHOH,碳碳双键的碳原子上接羟基不稳定,转化为CH3CHO。A聚合反应后得到的产物B为
[解析]本题考查有机物的结构推断和性质,注意结构简式、同分异构体、化学方程式的书写。根据题意,A分子中碳的原子数为4个,氢原子的个数为6个,则氧原子的个数为2个,即A的分子式为C4H6O2。由于A可以发生聚合反应,说明含有碳碳双键,在硫酸存在条件下生成两种有机物,则为酯的水解,即A中含有酯基。根据不饱和度,没有其他功能团。由A的水解产物C和D的关系可判断C与D中的碳原子数相等,均为两个。则A的结构为CH3COOCH=CH2,因此A在酸性条件下水解后得到CH3COOH和CH2=CHOH,碳碳双键的碳原子上接羟基不稳定,转化为CH3CHO。A聚合反应后得到的产物B为 ,在酸性条件下水解,除了生成乙酸和
,在酸性条件下水解,除了生成乙酸和 。
。


29. (15分)
(15分)

 现有A、B、C、D、E、F六种化合物,已知它们的阳离子有
现有A、B、C、D、E、F六种化合物,已知它们的阳离子有 ,
, 阴离子有
阴离子有 ,现将它们分别配成
,现将它们分别配成 的溶液,进行如下实验:
的溶液,进行如下实验:
①

 测得溶液A、C、E呈碱性,且碱性为A>E>C;
测得溶液A、C、E呈碱性,且碱性为A>E>C;
②

 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③

 向D溶液中滴加
向D溶液中滴加 溶液,无明显现象;
溶液,无明显现象;
④

 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。

 根据上述实验现象,回答下列问题:
根据上述实验现象,回答下列问题:
(1)

 实验②中反应的化学方程式是
实验②中反应的化学方程式是

 ;
;

 (2)E溶液是 ,判断依据是
(2)E溶液是 ,判断依据是

 ;
;

 (3)写出下列四种化合物的化学式:A
、C
、
(3)写出下列四种化合物的化学式:A
、C
、

 D
、F
.
D
、F
.

 答案
答案


 [解析]本题考查离子共存、盐类水解综合运用。根据溶液的性质,确定CO32-只能与K+形成显碱性的溶液,另外可能形成的碱性溶液为碱Ba(OH)2 。由于醋酸的酸性大于碳酸,所以醋酸盐水解的碱性小于碳酸盐,因此A为Ba(OH)2,E为K2CO3,C为醋酸盐,由②可得B中阳离子为Ag+,则肯定为AgNO3,由③可得D中无SO42-,则F中的阴离子为SO42-,D中的阴离子为Cl-。由④可得F中的阳离子为Fe2+,即F为FeSO4,而CH3COO-若与Al3+形成溶液时,Al3+也发生水解,所以C为醋酸钙,而D为AlCl3。
[解析]本题考查离子共存、盐类水解综合运用。根据溶液的性质,确定CO32-只能与K+形成显碱性的溶液,另外可能形成的碱性溶液为碱Ba(OH)2 。由于醋酸的酸性大于碳酸,所以醋酸盐水解的碱性小于碳酸盐,因此A为Ba(OH)2,E为K2CO3,C为醋酸盐,由②可得B中阳离子为Ag+,则肯定为AgNO3,由③可得D中无SO42-,则F中的阴离子为SO42-,D中的阴离子为Cl-。由④可得F中的阳离子为Fe2+,即F为FeSO4,而CH3COO-若与Al3+形成溶液时,Al3+也发生水解,所以C为醋酸钙,而D为AlCl3。

28.
 (15分)
(15分)

 已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。






 回答下列问题:
回答下列问题:

 (1)A中加入的物质是_____________①_____________________________.
(1)A中加入的物质是_____________①_____________________________.

 发生反应的化学方程式是_______________②_______________________;
发生反应的化学方程式是_______________②_______________________;

 (2)B中加入的物质是_____③________,其作用是_________④_______________:
(2)B中加入的物质是_____③________,其作用是_________④_______________:

 (3)实验时在C中观察到得现象是_____________⑤_________________,
(3)实验时在C中观察到得现象是_____________⑤_________________,

 发生反应的化学方程式是_________________⑥____________________;
发生反应的化学方程式是_________________⑥____________________;

 (4)
实验时在D中观察到得现象是________________⑦__________________,
(4)
实验时在D中观察到得现象是________________⑦__________________,

 D中收集到的物质是_______⑧_______,检验该物质的方法和现象是_________⑨_____________.
D中收集到的物质是_______⑧_______,检验该物质的方法和现象是_________⑨_____________.

 答案
答案


 [解析]本题考查化学实验和有关化学方程式,注意化学实验现象的描述和试剂的选择。根据反应原理,反应物为氨气和氧化铜,可以判断试管A为制取氨气的装置,因此装入的药品应该为氯化铵和氢氧化钙,氨气要使用碱石灰。加热后,黑色氧化铜变为红色的铜,生成的水和氨气生成氨水留在了D中,而氮气通过排水法进行收集。检验氨气可利用其碱性,检验水可以用无水硫酸铜。
[解析]本题考查化学实验和有关化学方程式,注意化学实验现象的描述和试剂的选择。根据反应原理,反应物为氨气和氧化铜,可以判断试管A为制取氨气的装置,因此装入的药品应该为氯化铵和氢氧化钙,氨气要使用碱石灰。加热后,黑色氧化铜变为红色的铜,生成的水和氨气生成氨水留在了D中,而氮气通过排水法进行收集。检验氨气可利用其碱性,检验水可以用无水硫酸铜。

27. (15分)
(15分)

 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。

 (1)根据左表中数据,在右图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
(1)根据左表中数据,在右图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
|
t/min |
X/mol |
Y/mol |
Z/mol |
|
0 |
1.00 |
1.00 |
0.00 |
|
1 |
0.90 |
0.80 |
0.20 |
|
3 |
0.75 |
0.50 |
0.50 |
|
5 |
0.65 |
0.30 |
0.70 |
|
9 |
0.55 |
0.10 |
0.90 |
|
10 |
0.55 |
0.10 |
0.90 |
|
14 |
0.55 |
0.10 |
0.90 |


 (2)
体系中发生反应的化学方程式是___________________________;
(2)
体系中发生反应的化学方程式是___________________________;


 (3)
列式计算该反应在0-3min时间内产物Z的平均反应速率:_______________;
(3)
列式计算该反应在0-3min时间内产物Z的平均反应速率:_______________;

 (4)
该反应达到平衡时反应物X的转化率
(4)
该反应达到平衡时反应物X的转化率 等于___________________________;
等于___________________________;

 (5)
如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应的实验条件改变分别是:
(5)
如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应的实验条件改变分别是:

 ① _________________ ②________________ ③__________________
① _________________ ②________________ ③__________________

 答案
答案
(1)



 [解析]本题考查化学反应速率和化学平衡的综合运用,注意图像和有关计算。
[解析]本题考查化学反应速率和化学平衡的综合运用,注意图像和有关计算。
 (1)根据题目中表格给出的数据,在坐标系中找出相应的点,然后用光滑的曲线描点即可。
(1)根据题目中表格给出的数据,在坐标系中找出相应的点,然后用光滑的曲线描点即可。
 (2)根据题意,可以利用“三步法”求解
(2)根据题意,可以利用“三步法”求解
 aX + bY
aX + bY cZ
cZ
 开始 1.00 1.00 0
开始 1.00 1.00 0
 转化 0.45 0.9 0.9
转化 0.45 0.9 0.9
 平衡 0.55 0.1 0.9
平衡 0.55 0.1 0.9
 根据各物质的量之比可得体系中发生反应的化学方程式是: X+2Y
根据各物质的量之比可得体系中发生反应的化学方程式是: X+2Y 2Z。
2Z。
 (3)根据图像可知在3min时,生成物Z的物质的量为0.5mol, 其平均速率为0.083mol/L·min。
(3)根据图像可知在3min时,生成物Z的物质的量为0.5mol, 其平均速率为0.083mol/L·min。
 (4)X的转化率等于0.45。
(4)X的转化率等于0.45。
 (5)由题目所给图象可知,在1中,平衡时Z的物质的量小于原平衡的物质的量,说明平衡逆向移动,条件为升高温度。在2中,平衡时Z的物质的量与原平衡相同,且速率加快,条件为加入催化剂;在3中,平衡正向移动,且速率加快,条件为加压。
(5)由题目所给图象可知,在1中,平衡时Z的物质的量小于原平衡的物质的量,说明平衡逆向移动,条件为升高温度。在2中,平衡时Z的物质的量与原平衡相同,且速率加快,条件为加入催化剂;在3中,平衡正向移动,且速率加快,条件为加压。

26. (21分)
(21分)

 如图,P、Q为某地区水平地面上的两点,在P点正下方一球形区域内储藏有石油,假定区域周围岩石均匀分布,密度为
如图,P、Q为某地区水平地面上的两点,在P点正下方一球形区域内储藏有石油,假定区域周围岩石均匀分布,密度为 ;石油密度远小于
;石油密度远小于 ,可将上述球形区域视为空腔。如果没有这一空腔,则该地区重力加速度(正常值)沿竖直方向;当存在空腔时,该地区重力加速度的大小和方向会与正常情况有微小偏高。重力加速度在原坚直方向(即PO方向)上的投影相对于正常值的偏离叫做“重力加速度反常”。为了探寻石油区域的位置和石油储量,常利用P点附近重力加速度反常现象。已知引力常数为G。
,可将上述球形区域视为空腔。如果没有这一空腔,则该地区重力加速度(正常值)沿竖直方向;当存在空腔时,该地区重力加速度的大小和方向会与正常情况有微小偏高。重力加速度在原坚直方向(即PO方向)上的投影相对于正常值的偏离叫做“重力加速度反常”。为了探寻石油区域的位置和石油储量,常利用P点附近重力加速度反常现象。已知引力常数为G。



(1)

 设球形空腔体积为V,球心深度为d(远小于地球半径),
设球形空腔体积为V,球心深度为d(远小于地球半径), =x,求空腔所引起的Q点处的重力加速度反常
=x,求空腔所引起的Q点处的重力加速度反常
(2)

 若在水平地面上半径L的范围内发现:重力加速度反常值在
若在水平地面上半径L的范围内发现:重力加速度反常值在 与
与 (k>1)之间变
(k>1)之间变

 化,且重力加速度反常的最大值出现在半为L的范围的中心,如果这种反常是由于地下存在某一球形空腔造成的,试求此球形空腔球心的深度和空腔的体积。
化,且重力加速度反常的最大值出现在半为L的范围的中心,如果这种反常是由于地下存在某一球形空腔造成的,试求此球形空腔球心的深度和空腔的体积。

 答案(1)
答案(1)
 (2)
(2) ,
,

 [解析]本题考查万有引力部分的知识.
[解析]本题考查万有引力部分的知识.
 (1)如果将近地表的球形空腔填满密度为
(1)如果将近地表的球形空腔填满密度为 的岩石,则该地区重力加速度便回到正常值.因此,重力加速度反常可通过填充后的球形区域产生的附加引力
的岩石,则该地区重力加速度便回到正常值.因此,重力加速度反常可通过填充后的球形区域产生的附加引力 ………①来计算,式中的m是Q点处某质点的质量,M是填充后球形区域的质量,
………①来计算,式中的m是Q点处某质点的质量,M是填充后球形区域的质量, ……………②
……………②
 而r是球形空腔中心O至Q点的距离
而r是球形空腔中心O至Q点的距离 ………③
………③ 在数值上等于由于存在球形空腔所引起的Q点处重力加速度改变的大小.Q点处重力加速度改变的方向沿OQ方向,重力加速度反常
在数值上等于由于存在球形空腔所引起的Q点处重力加速度改变的大小.Q点处重力加速度改变的方向沿OQ方向,重力加速度反常 是这一改变在竖直方向上的投影
是这一改变在竖直方向上的投影 ………④联立以上式子得
………④联立以上式子得

 ,…………⑤
,…………⑤
 (2)由⑤式得,重力加速度反常
(2)由⑤式得,重力加速度反常 的最大值和最小值分别为
的最大值和最小值分别为 ……⑥
……⑥

 ……………⑦由提设有
……………⑦由提设有 、
、 ……⑧
……⑧
 联立以上式子得,地下球形空腔球心的深度和空腔的体积分别为
联立以上式子得,地下球形空腔球心的深度和空腔的体积分别为

 ,
,
25.
 (18分)
(18分)

 如图,在宽度分别为
如图,在宽度分别为 和
和 的两个毗邻的条形区域分别有匀强磁场和匀强电场,磁场方向垂直于纸面向里,电场方向与电、磁场分界线平行向右。一带正电荷的粒子以速率v从磁场区域上边界的P点斜射入磁场,然后以垂直于电、磁场分界线的方向进入电场,最后从电场边界上的Q点射出。已知PQ垂直于电场方向,粒子轨迹与电、磁场分界线的交点到PQ的距离为d。不计重力,求电场强度与磁感应强度大小之比及粒子在磁场与电场中运动时间之比。
的两个毗邻的条形区域分别有匀强磁场和匀强电场,磁场方向垂直于纸面向里,电场方向与电、磁场分界线平行向右。一带正电荷的粒子以速率v从磁场区域上边界的P点斜射入磁场,然后以垂直于电、磁场分界线的方向进入电场,最后从电场边界上的Q点射出。已知PQ垂直于电场方向,粒子轨迹与电、磁场分界线的交点到PQ的距离为d。不计重力,求电场强度与磁感应强度大小之比及粒子在磁场与电场中运动时间之比。




 答案
答案
 [解析]本题考查带电粒子在有界磁场中的运动.
[解析]本题考查带电粒子在有界磁场中的运动.

 粒子在磁场中做匀速圆周运动,如图所示.由于粒子在分界线处的速度与分界线垂直,圆心O应在分界线上,OP长度即为粒子运动的圆弧的半径R.由几何关系得
粒子在磁场中做匀速圆周运动,如图所示.由于粒子在分界线处的速度与分界线垂直,圆心O应在分界线上,OP长度即为粒子运动的圆弧的半径R.由几何关系得

 ………①
………①
 设粒子的质量和所带正电荷分别为m和q,由洛仑兹力公式和牛顿第二定律得
设粒子的质量和所带正电荷分别为m和q,由洛仑兹力公式和牛顿第二定律得


 ……………②
……………②

 设
设 为虚线与分界线的交点,
为虚线与分界线的交点, ,则粒子在磁场中的运动时间为
,则粒子在磁场中的运动时间为 ……③
……③
 式中有
式中有 ………④粒子进入电场后做类平抛运动,其初速度为v,方向垂直于电场.设粒子的加速度大小为a,由牛顿第二定律得
………④粒子进入电场后做类平抛运动,其初速度为v,方向垂直于电场.设粒子的加速度大小为a,由牛顿第二定律得 …………⑤
…………⑤
 由运动学公式有
由运动学公式有 ……⑥
……⑥
 ………⑦
………⑦
 由①②⑤⑥⑦式得
由①②⑤⑥⑦式得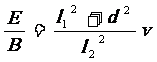 …………⑧
…………⑧
 由①③④⑦式得
由①③④⑦式得
24. (15分)
(15分)


 如图,匀强磁场的磁感应强度方向垂直于纸面向里,大小随时间的变化率
如图,匀强磁场的磁感应强度方向垂直于纸面向里,大小随时间的变化率 ,
, 为负的常量。用电阻率为
为负的常量。用电阻率为 、横截面积为
、横截面积为 的硬导线做成一边长为
的硬导线做成一边长为 的方框。将方框固定于纸面内,其右半部位于磁场区域中。求
的方框。将方框固定于纸面内,其右半部位于磁场区域中。求


(1)

 导线中感应电流的大小;
导线中感应电流的大小;
(2)

 磁场对方框作用力的大小随时间的变化
磁场对方框作用力的大小随时间的变化

 答案(1)
答案(1)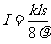
 (2)
(2)
 [解析]本题考查电磁感应现象.(1)线框中产生的感应电动势
[解析]本题考查电磁感应现象.(1)线框中产生的感应电动势
 ……①在线框产生的感应电流
……①在线框产生的感应电流 ……②
……② ,……③联立①②③得
,……③联立①②③得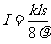
 (2)导线框所受磁场力的大小为
(2)导线框所受磁场力的大小为 ,它随时间的变化率为
,它随时间的变化率为 ,由以上式联立可得
,由以上式联立可得 .
.

23、
 (13分)
(13分)

 某同学得用图1所示装置做“研究平抛运动”的实验,根据实验结果在坐标纸上描出了小球水平抛出后的运动轨迹,但不慎将画有轨迹图线的坐标纸丢失了一部分,剩余部分如图2所示。图2中水平方向与竖直方向每小格的长度均代表0.10m,
某同学得用图1所示装置做“研究平抛运动”的实验,根据实验结果在坐标纸上描出了小球水平抛出后的运动轨迹,但不慎将画有轨迹图线的坐标纸丢失了一部分,剩余部分如图2所示。图2中水平方向与竖直方向每小格的长度均代表0.10m, 、
、 和
和 是轨迹图线上的3个点,
是轨迹图线上的3个点, 和
和 、
、 和
和 之间的水平距离相等。
之间的水平距离相等。

 完成下列真空:(重力加速度取
完成下列真空:(重力加速度取 )
)
(1)

 设
设 、
、 和
和 的横坐标分别为
的横坐标分别为 、
、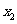 和
和 ,纵坐标分别为
,纵坐标分别为 、
、 和
和 ,从图2中可读出
,从图2中可读出 =____①_____m,
=____①_____m, =____②______m,
=____②______m, =____③______m(保留两位小数)。
=____③______m(保留两位小数)。
(2)

 若已测知抛出后小球在水平方向上做匀速运动。利用(1)中读取的数据,
求出小球从
若已测知抛出后小球在水平方向上做匀速运动。利用(1)中读取的数据,
求出小球从 运动到
运动到 所用的时间为______④__________s,小球抛出后的水平速度为________⑤__________
所用的时间为______④__________s,小球抛出后的水平速度为________⑤__________ (均可用根号表示)。
(均可用根号表示)。
(3)

 已测得小球抛也前下滑的高度为0.50m。设
已测得小球抛也前下滑的高度为0.50m。设 和
和 分别为开始下滑时和抛出时的机械能,则小球从开始下滑到抛出的过程中机械能的相对损失,
分别为开始下滑时和抛出时的机械能,则小球从开始下滑到抛出的过程中机械能的相对损失, =________⑥__________%(保留两位有效数字)
=________⑥__________%(保留两位有效数字)




 答案(1)0.61 1.61 0.60
答案(1)0.61 1.61 0.60
 (2)0.20 3.0
(2)0.20 3.0
 (3)8.2
(3)8.2
 [解析]本题考查研究平抛运动的实验.由图可知P1到P2两点在竖直方向的间隔为6格, P1到P3两点在竖直方向的间隔为16格所以有
[解析]本题考查研究平抛运动的实验.由图可知P1到P2两点在竖直方向的间隔为6格, P1到P3两点在竖直方向的间隔为16格所以有 =0.60m.
=0.60m. =1.60m.
P1到P2两点在水平方向的距离为6个格.则有
=1.60m.
P1到P2两点在水平方向的距离为6个格.则有 =0.60m.
=0.60m.
 (2)由水平方向的运动特点可知P1到P2 与P2到P3的时间相等,根据
(2)由水平方向的运动特点可知P1到P2 与P2到P3的时间相等,根据 ,解得时间约为0. 2s,则有
,解得时间约为0. 2s,则有
 (3)设抛出点为势能零点,则开始下滑时的机械能为E1=mgh=mg/2,抛出时的机械能为E2=
(3)设抛出点为势能零点,则开始下滑时的机械能为E1=mgh=mg/2,抛出时的机械能为E2= =4.5m,则根据
=4.5m,则根据 0.082
0.082

22、
 (5分)
(5分)

 某同学利用多用电表测量二极管的反向电阻。完成下列测量步骤:
某同学利用多用电表测量二极管的反向电阻。完成下列测量步骤:
(1)

 检查多用电表的机械零点。
检查多用电表的机械零点。
(2)

 将红、黑表笔分别插入正、负表笔插孔,将选择开关拔至电阻测量挡适当的量程处。
将红、黑表笔分别插入正、负表笔插孔,将选择开关拔至电阻测量挡适当的量程处。
(3)

 将红、黑表笔____①_______,进行欧姆调零。
将红、黑表笔____①_______,进行欧姆调零。
(4)

 测反向电阻时,将____②______表笔接二极管正极,将____③_____表笔接二极管负极,读出电表示数。
测反向电阻时,将____②______表笔接二极管正极,将____③_____表笔接二极管负极,读出电表示数。
(5)

 为了得到准确的测量结果,应让电表指针尽量指向表盘____④_______(填“左侧”、“右侧”或“中央”);否则,在可能的条件下,应重新选择量程,并重复步骤(3)、(4)。
为了得到准确的测量结果,应让电表指针尽量指向表盘____④_______(填“左侧”、“右侧”或“中央”);否则,在可能的条件下,应重新选择量程,并重复步骤(3)、(4)。
(6)

 测量完成后,将选择开关拔向_____________⑤________________位置。
测量完成后,将选择开关拔向_____________⑤________________位置。
 答案(3)短接
答案(3)短接
 (4)红 黑
(4)红 黑
 (5)中央
(5)中央
 (6)OFF
(6)OFF
 [解析]本题考查多用电表的使用.首先要机械调零.在选择量程后还要进行欧姆调零而且每一次换量程都要重复这样的过程.(3)将红黑表笔短接,即为欧姆调零.测量二极管的反向电阻时应将红笔接二极管的正极,黑接负极.欧姆表盘的刻度线分布不均匀,在中央的刻度线比较均匀,所以尽量让指针指向表盘的中央.测量完成后应将开关打到off档.
[解析]本题考查多用电表的使用.首先要机械调零.在选择量程后还要进行欧姆调零而且每一次换量程都要重复这样的过程.(3)将红黑表笔短接,即为欧姆调零.测量二极管的反向电阻时应将红笔接二极管的正极,黑接负极.欧姆表盘的刻度线分布不均匀,在中央的刻度线比较均匀,所以尽量让指针指向表盘的中央.测量完成后应将开关打到off档.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com