
23、(12分)A-I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第_______周期、第_______族 ;
(2)写出反应①的化学方程式___________ _________;
(3)写出反应④的离子方程式_____________ _______; (4)写出反应③的电极方程式:
阳极:_______________ _____ 阴极:____________ __________
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是___________。(填序号)
22、(13分)2g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075mol/L KMnO4溶液处理,发生反应如下:
① MnO4-+ Cu2S+ H+= Cu2++ SO2+ Mn2++ H2O
②6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL0.1mol/L(NH4)2Fe(SO4)2溶液完全反应,反应式为:
③MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
请回答:
(1) 配平KMnO4与Cu2S反应的离子方程式并用单线桥标出电子转移:
MnO4-+ Cu2S+ H+= Cu2++ SO2+ Mn2++ H2O
若标准状况下有1.12 L SO2生成,则转移电子的物质的量是 。
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为 mol。
(3)欲配制500mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为 g,配制时所需要的定量仪器是 。
(4)混合物中Cu2S的质量分数为 。
21、(11分)某无色溶液,其中可能存在如下离子:Na+、Ag+、Ba2+、Al3+、AlO2―、S2―、CO32―、SO32―、SO42―,现取该溶液进行有关实验,结果与下图所示。
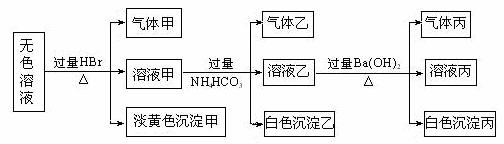
试回答下列问题:
(1)生成沉淀甲的离子方程式为 。
(2)由溶液甲生成沉淀乙的离子方程式 。
(3)沉淀丙是 。如何用一化学实验来确定其成分 。
(4)气体甲的成分有哪几种可能 。
(5)综合上述信息,可以肯定存在的离子有 ,
一定不存在的离子是 ,可能存在的离子是 。
20、下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象相同的是( )
A.NaHSO4和Ba(OH)2 B.AlCl3和NaOH
C.NaAlO2和H2SO4 D.Ba(HCO3)2和Ba(OH) 2
19、出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。下列说法正确的是
 A. 锡青铜的熔点比纯铜高
A. 锡青铜的熔点比纯铜高
 B.在自然环境中,锡青铜中的锡对铜起保护作用
B.在自然环境中,锡青铜中的锡对铜起保护作用
 C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
 D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
18、 下列离子方程式正确的是
下列离子方程式正确的是
 A.
A.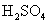 与
与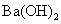 溶液反应:
溶液反应: 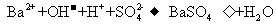
 B.
B.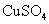 溶液吸收
溶液吸收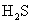 气体:
气体: 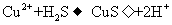
 C.
C.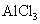 溶液中加入过量的浓氨水:
溶液中加入过量的浓氨水: 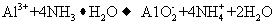
 D.等体积、等浓度的
D.等体积、等浓度的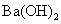 稀溶液与
稀溶液与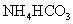 稀溶液混合:
稀溶液混合:

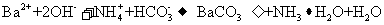
17、下列化学实验事实及其解释都正确的是
 A.向碘水中滴加
A.向碘水中滴加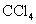 ,振荡静置后分层,
,振荡静置后分层,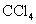 层呈紫红色,说明可用
层呈紫红色,说明可用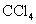 从碘水中萃取碘
从碘水中萃取碘
 B.向
B.向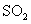 水溶液中滴加盐酸酸化的
水溶液中滴加盐酸酸化的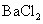 溶液,有白色沉淀生成,说明
溶液,有白色沉淀生成,说明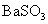 难溶于盐酸
难溶于盐酸
 C.向0.1mol·L-1
C.向0.1mol·L-1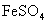 溶液中滴加少量酸性
溶液中滴加少量酸性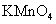 溶液,
溶液,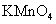 溶液褪色,说明
溶液褪色,说明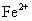 具有氧化性
具有氧化性
 D.
向2.0mL浓度均为0.1mol·L-1的
D.
向2.0mL浓度均为0.1mol·L-1的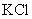 、
、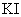 混合溶液中滴加1~2滴0.01mol·L-1
混合溶液中滴加1~2滴0.01mol·L-1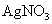 溶液,振荡,沉淀呈黄色,说明
溶液,振荡,沉淀呈黄色,说明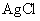 的
的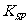 比
比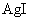 的
的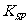 大
大
16、25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是
A.2H+(aq)
+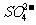 (aq)+
(aq)+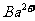 (aq)+2OH
(aq)+2OH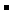 (aq)=BaSO4(s)+2H
(aq)=BaSO4(s)+2H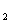 O(1);
O(1); H=
H=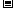 57.3 kJ/mol
57.3 kJ/mol
B.KOH(aq)+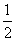 H
H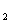 SO4(aq)=
SO4(aq)=
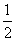 K
K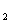 SO4(aq)+H
SO4(aq)+H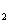 O(I);
O(I);
 H=
H=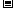 57.3kJ/mol
57.3kJ/mol
C.C8H18(I)+
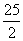 O
O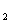 (g)=8CO
(g)=8CO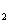 (g)+ 9H
(g)+ 9H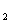 O;
O;  H=
H=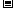 5518 kJ/mol
5518 kJ/mol
D.2C8H18(g)+25O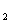 (g)=16CO
(g)=16CO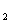 (g)+18H
(g)+18H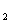 O(1);
O(1);  H=
H=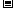 5518 kJ/mol
5518 kJ/mol
15、向某晶体的水溶液中加入FeCl2的溶液后,无明显变化,当滴加几滴溴水后,混合液出现血红色。那么,由此得出下列的结论错误的是 ( )
A.该晶体中一定含有SCN- B.Fe3+与SCN-形成了血红色Fe (SCN)3难溶物
C.Fe2+被Br2氧化为Fe3+ D.Fe2+与SCN-不能形成血红色物质
14、向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为
A.0.24mol B.0.21mol C.0.16mol D.0.14mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com