
12、已知某弱酸的酸式盐有NaH2XO4和Na2HXO4,其中NaH2XO4的溶液呈酸性,Na2HXO4溶液呈碱性。30℃时,浓度均为0.1mol•L-1NaH2XO4溶液和Na2HXO4溶液中均存在的关系是
A.c(H+)•c(OH-) >1×10-14
B.c(H+) + 2c(H3XO4)+ c(H2XO4-)=c(XO43-)+ c(OH-)
C. c(Na+)+ c(H+)= c(H2XO4-)+ c(OH-)+ 2c(HXO42-)+ 3c(XO43-)
D.c(H+) + c(H3XO4)= c(HXO42-)+ 2c(XO43-)+ c(OH-)
11.“人文奥运、科技奥运、绿色奥运”是2008年北京奥运会的重要特征。其中禁止运动员使用兴奋剂是重要举措之一。以下两种兴奋剂的结构分别为:
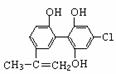
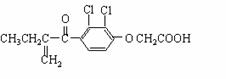
①利尿酸 ②兴奋剂X
则关于它们的说法中正确的是
A.利尿酸分子中有三种含氧官能团,在核磁共振氢谱上共有六个峰
B.1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br2
C.两种兴奋剂均属于芳香烃化合物
D.两种分子中的所有碳原子均不可能共平面
10、下列离子方程式不正确的是
A.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B.4mol·L-1的NaAlO2溶液和7mol·L-1的HCl等体积互相均匀混合
4AlO2-+ 7H+ + H2O = 3Al(OH)3↓+ Al3+
C.在含有Mn2+的溶液中加入HNO3再加入PbO2,则反应体系显紫红色
5PbO2 + 2Mn2+ + 4H+ = 5Pb2+ + 2MnO4- + 2H2O
D.甲醛溶液中加入足量的银氨溶液并加热
HCHO+2[Ag (NH3)2]++2OH- HCOO-+NH4++2Ag↓+3NH3+H2O
HCOO-+NH4++2Ag↓+3NH3+H2O
9、高铁酸钾K2FeO4是一种新型、高效、氧化性比Cl2更强的水处理剂,工业上通常用下列反应先制得高铁酸钠:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,然后在某低温下,在高铁酸钠溶液中加KOH固体至饱和就可析出高铁酸钾,下列有关说法不正确的是
A. Na2O2在反应中既作氧化剂,又作还原剂
 B. 制取高铁酸钠时,每生成lmolNa2FeO4反应中共有4mol电子转移
B. 制取高铁酸钠时,每生成lmolNa2FeO4反应中共有4mol电子转移
C.高铁酸钾在该温度下的溶解度比高铁酸钠的溶解度小
D. K2FeO4能消毒杀菌,其还原产物水解生成的Fe(OH)3胶体能吸附水中的悬浮杂质
8、 下列各组离子,在指定的环境中一定能大量共存的是
下列各组离子,在指定的环境中一定能大量共存的是
A.在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、HCO3-、Na+
B.在能使pH试纸变红色的溶液中:Na+、S2-、NO3-、CO32-
C.在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、Cl-、NO3-
D.由水电离出的c(H+)=1×10-12mol·L-1的溶液中:K+、Cl-、NO3-、Na+
7、下列有关叙述:① 非金属单质M能从N的化合物中置换出非金属单质N;② M原子比N原子容易得到电子;③单质M跟H2反应比N跟H2反应容易得多;④气态氢化物水溶液的酸性HmM>HnN;⑤氧化物水化物的酸性HmMOx>HnNOy;⑥熔点M>N。能说明非金属元素M比N的非金属性强的是
A.②⑤ B.①②③ C.①②③⑤ D.全部
6、A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+与C-具有相同的电子层结构,下列叙述一定不正确的是
A.离子半径A2-> C->B2+ B.它们的原子半径C>B>A
C.它们的原子序数A>B>C D.原子最外层上的电子数C>A>B
5、 一种甲醇、氧气和强碱溶液做电解质的新型手机电池,可连续使用一个月,其电池反应为:2CH3OH + 3O2 +4OH-
一种甲醇、氧气和强碱溶液做电解质的新型手机电池,可连续使用一个月,其电池反应为:2CH3OH + 3O2 +4OH-
 2CO32- +6H2O,则有关说法正确的是
2CO32- +6H2O,则有关说法正确的是
A . 放电时CH3OH参与反应的电极为正极
B . 放电时负极的电极反应为CH3OH +8 OH- - 6e- = CO32- + 6H2O
C . 标准状况下,通入5.6LO2并完全反应后,有0.5mol电子转移
D . 放电一段时间后,通入氧气的电极附近溶液的pH降低
4、下列颜色不属于因化学反应而产生的现象的是
A.无色试剂瓶中的浓硝酸呈黄色
B.久置的KI溶液呈黄色
C.新制氯水久置后变为无色
D.普通玻璃导管口点燃纯净氢气时,火焰呈黄色
3、NA代表阿伏加德罗常数。下列说法中,不正确的是
A.标准状况下,NO和 O2各11.2 L 混合,所得混合气体的分子总数为 0.75 NA
B.25℃时,l L pH=13的Ba(OH)2 溶液中含有OH―的数目为0.1 NA
C.1 mol C30H62 分子中含有共价键的数目为 91 NA
D.2.8g 乙烯与丙烯的混合物中含碳原子的数目为 0.2NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com