
19.(5分)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)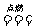 CO2(g) (
放热Q1 kJ )
CO2(g) (
放热Q1 kJ )
途径Ⅱ:先制水煤气
C(s)+H2O(g) == CO(g)+H2(g) (吸热Q2 kJ)
再燃烧水煤气
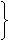
|
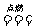 2CO2(g)
2CO2(g)
2H2(g)+O2(g) 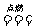 2H2O(g)
2H2O(g)
试回答下列问题:
(1)判断两种途径放热:途径Ⅰ放出的热量_________(填“大于”、“等于”或“小于”)途径Ⅱ放出的热量。
(2)Q1、Q2、Q3的数学关系式是__________________。
(3)由于制取水煤气反应里,反应物所具有的总能量________生成物所具有的总能量,那么在化学反应时,反应物就需要_______能量才能转化为生成物,因此其反应条件为______ 。
18.(7分)已知将盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。
现有一氧化还原反应的体系中,反应物和生成物共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
(1)该反应中,化合价升高的反应物是____,化合价没有发生变化的反应物是__ __。
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平)______ _____。
(3)上述反应中, 1 mol氧化剂在反应中_____(填“得到”或“失去”)____mol电子。
(4)如果在反应后的溶液中加入NaBiO3,溶液又变紫红色。说出NaBiO3的一个性质:_________________________________________。
17.(10分)下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
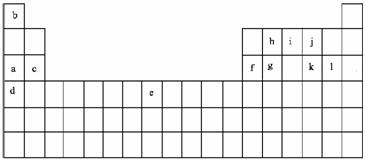
回答下列问题
⑴以上元素中原子半径最大的是 (填写元素符号)最小的是 (填写
元素名称)
⑵以上元素中,属于金属的:①在地壳中含量最高的是 ,(填写字母代号)②
单质的工业年产量最高的是 (填写周期表中的具体位置)
⑶h和g的最高价氧化物比较,熔点高的是 (填写氧化物化学式);j和
k的氢化物比较,熔点高的是 (填写氢化物化学式)
⑷以上元素两两形成的中学中常见的化合物中既有离子键,又有共价键的四核化合物有 (写一种) (填写化学式)
⑸按要求写出:①c的氧化物与l的氢化物反应的化学方程式
②都是由abjk四种元素形成的两种化合物反应的离子方程式
⑹bil三元素形成的化合物的电子式为
16.下列有关物质性质、结构的表述均正确,且存在因果关系的是:
|
|
表述Ⅰ |
表述Ⅱ |
|
A |
在水中,NaCl的溶解度比I2的溶解度大 |
NaCl晶体中C1-与Na+间的作用力大于碘晶体中分子间的作用力 |
|
B |
通常条件下,CH4分子比PbH4分子稳定性高 |
Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
|
C |
在形成化合物时,同一主族元素的化合价相同 |
同一主族元素原子的最外层电子数相同 |
|
D |
P4O10、C6H12O6溶于水后均不导电 |
P4O10、C6H12O6均属于共价化合物 |
15、下列说法正确的是
A.需要加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件下一定能发生反应
C.反应物和生成物所具有的总能量决定了反应结果是放热还是吸热
D.吸热反应在一定条件下也不能发生反应
14.LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠.已知该电池放电时的电极反应式为:正极 FePO4+Li++e-==LiFePO4 ,负极 Li-e-== Li+ .下列说法中正确的是
www.
A.充电时电池反应为FePO4+Li = LiFePO4
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
13.同一短周期的元素W、X、Y、Z的原子序数依次增加,下列叙述正确的是:
A.单质的化学活泼性:W<X<Y<Z B.原子最外层电子数:W<X<Y<Z
C.单质的氧化能力:W<X<Y<Z D.元素的最高化合价:W<X<Y<Z
12.A是一种常见的单质,B、C为中学化学常见的化合物,A、B、C均含有元素X,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列判断正确的是

 B H+
B H+

 A
A
A
A
① ②
 C
C
A.X元素可能为Al B.X元素可能为金属,也可能是非金属
C.反应①和②互为可逆反应 D.反应①和②一定为氧化还原反应
11.某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能得到的正确结论是
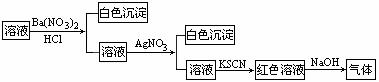
A.原溶液中一定含有SO42-离子 B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子
10.恒温下的下列实验过程中,有关溶液的浓度和质量始终不变的
A.向浓氨水中持续通入干燥洁净的空气(不含CO2)B.向KNO3饱和溶液中加入ngKNO3晶体
C.向98.3%浓H2SO4中加入ngSO3 D.向CuSO4饱和溶液中加入ng无水CuSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com