
3.本文题目是“唤醒火星”, 唤醒这个“冰冻的星球”可能采用哪些方法?
2.火星上有哪些奇异特征?
段军
①火星是一颗最具有传奇色彩的行星,有着许多令人向往的故事。然而,它并不像人们想象的那样完美。在干燥的火星表面上,遍地都是红色的土壤和岩石。由于不断受到风沙的作用,火星表面随处可见沙丘和类似河床的地形。这种河床地形分布在南半球及赤道附近,表明了距今大约30亿年前火星上曾有像地球上一样的河川,有水流动。
②火星的直径约为地球的1/2,体积还不到地球的1/6,质量仅是地球的1/10,火星大气远比地球稀薄,它的主要成分是二氧化碳,占95%,氮占3%,还有数量极少的氧气与水分。
③由于火星大气稀薄而干燥,所以它的昼夜温差变化很大,远远大于地球上的昼夜温差。因火星表面温度低、压力小,大气中的二氧化碳和水分大致都是呈饱和状态,只要气温稍一降低,二氧化碳和水蒸气都会凝结。火星大气中的水分极少,至多也只能在火星表面形成一个10m深的湖泊。与我们地球表面波涛茫茫的海洋相比,火星上的水量就显得微不足道了。
④火星上另一个奇异特征便是每年都要刮起一次让人难以想象的特大风暴,风速之大无法形容。地球上的特大台风,风速约60m/s,而火星上的风速竟高达180m/s。1971年,当美国“水手9号”火星探测器刚刚走了一半的路程时,就发现整个火星被一场大风暴所包围,火星表面70km~80km的高空被尘埃笼罩,白茫茫一片,根本无法观测。这场特大风暴竟连续不断地刮了半年时间才渐渐平息下来,火星才开始显露出它的真实面目。
⑤有一个问题总在困扰着人类:是否在一段时期内,火星上曾有生命出现,无论是动物、植物,甚至是病毒。在火星演化的早期阶段,红色星球上也有过山川、河流、云彩、雨雪、海岸和峡谷,但是后来都消失了。
⑥现在,人类希望征服这个冰冻的球体,虽然这里几乎没有氧气,而且温度极低,沙暴猛烈。即便如此,人类依然想要把它变成一个像伊甸园那样的花果园。
⑦唤醒这个“冰冻星球”的最基本办法是加热,在此之后,还要给它创造一个合适的大气环境,用水灌溉,让它远离酷热。研究人员认为,整个过程大约需要500~5万年的时间。但除此之外,更为重要的是,要让这个星球适合于生命的存在,乃至人类的生存。
(选自2009年《科学之友》第4期,有删改)
1.本文的说明对象是
30、在100mL 10mol/L的硝酸中,加入m克的Fe后,在加热条件下恰好完全反应,收集到NO与NO2的混合气体,将气体通过低温使NO2完全转化为N2O4晶体,得到9.2克晶体,反应后在溶液中滴入KSCN溶液,发现溶液不显红色。
(1)加入Fe的质量m为 g;
(2)反应中收集到的气体中NO的体积在标准状况下为 L。
29、某些化学反应可用下式表示
A + B ─→ C + D + H2O
请回答下列问题:
(1)若A、C、D均含有氯元素,且氯在A的化合价介于C与D之间,写出该反应的离子方程式: 。
(2)若C为氯化钠,D是能使澄清石灰水变浑浊的无味气体,则A与B的组合是:
或 。D的电子式为 。
(3)若A为黑色固体,C是黄绿色的单质气体,写出该反应的离子方程式: 。
(4)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是 。(写名称)
28、无水氯化铝是白色晶体,露置在空气中极易水解,在178℃升华,装有无水氯化铝试剂瓶露置空气中,会产生大量白雾,氯化铝常作为有机合成和石油工业的催化剂。
下图是实验室制取氯气并用于制取少量无水氯化铝的装置的仪器和药品。
可供选用的试剂如下:
A.浓H2SO4 B.水 C.饱和食盐水 D.烧碱溶液
E.铝粉 F.二氧化锰 G.浓盐酸 H.无水CaCl2 I.碱石灰
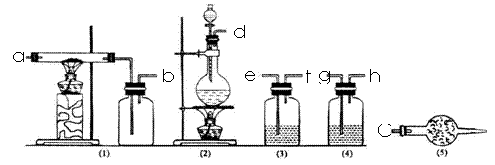
回答下列问题:
(1)从上述仪器中选取若干连成一制备并保存无水AlCl3的装置,用图中各管口标号按先后可连接为:d接e ,( )接( ),( )接( ),( )接( )。
(2)填写连接装置中各选用仪器里应盛放的物质:
|
仪器标号 |
(1) |
(2)(上) |
(2)(下) |
(3) |
(4) |
(5) |
|
试剂标号 |
|
G |
|
C |
|
|
(3)设计使用(5)仪器和药品有两个主要作用是: 和 。
(4)写出AlCl3露置在空气中生成白雾的化学方程式: 。
27、下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4︰5,化合物D是重要的工业原料。
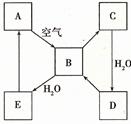
(1)已知4g固态A在O2中完全燃烧生成气体放热37kJ,写出此反应的热化学方程式_______________________________________________________________。
(2)写出E与A的氢化物反应生成A的化学方程式___________________________。
(3)写出一个由D生成B的化学方程式____________________________________。
(4)将5 mL0.10 mol·L-1的E溶液与10 mL0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式__________________________________________;
②反应后溶液的pH ____7(填“大于”、“小于”或“等于”),理由是 ;
26、(1)配制1mol·L-1H2SO4溶液200mL,需溶质质量分数为98%(ρ=1.84g·/cm3)的浓H2SO4
毫升。
(2)实验室欲配制80mL 1.4mol/L的NaNO3溶液,
①用不到的仪器是: ;
A.烧杯 B.500mL容量瓶 C.量筒 D.胶头滴管 E.玻璃棒 F.100mL容量瓶
②下列操作的顺序是(用字母表示) ;
A.放置至室温 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移
25.含有ag硝酸的稀溶液跟bg铁恰好反应,铁全部溶解,生成NO,已知有a/4克硝酸被还原,则a:b可能是( )
①3:1 ②3:2 ③4:1 ④9:2
A.① B. ④
C. ①③④
D. ①④

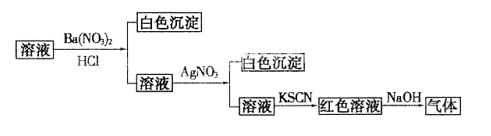
24.为检验某溶液中的离子,进行了如下图所示的实验操作,过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是( )
A.原溶液中一定含有SO42-离子
B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子
D.原溶液中一定含有Fe3+离子

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com