
8. 下列离子方程式书写正确的是 ( )
A.碳酸氢钙溶液中加入等物质的量的NaOH溶液:
Ca2++2HCO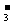 +2OH-=CaCO3↓+2H2O+CO
+2OH-=CaCO3↓+2H2O+CO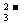
B.碳酸钠溶液中加入等物质的量的乙酸
CO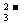 +2CH3COOH=CO2↑+H2O+2CH3COO-
+2CH3COOH=CO2↑+H2O+2CH3COO-
C.Ca(CIO)2溶液中通入过量的二氧化硫气体:
Ca2++2CIO-+H2O+SO2=CaSO3↓+2HCIO
D.用碳棒作电极电解氯化钠饱和溶液:
7. 已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出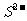 的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是
( )
的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是
( )
A.Mg2+ + 2HCO3- + 2Ca2+ + 4OH- → Mg(OH)2↓+ 2CaCO3↓+ 2H2O
B.Cu2+ + H2S → CuS↓+ 2H+
C.Zn2+ + S2- + 2H2O → Zn(OH)2↓+ H2S↑
D.FeS + 2H+ → Fe2+ + H2S↑
6. 下列离子方程式错误的是 ( )
A.硫化钠溶液中加生产方式足量盐酸:S2-+2H+→H2S↑
B.向碳酸氢钙溶液中开始滴入氢氧化钠溶液:
Ca2++2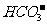 +2
+2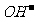 →CaCO3↓+2H2O+
→CaCO3↓+2H2O+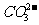
C.用硫酸铜溶液吸收硫化氢气体:Cu2++H2S→CuS↓+2H+
D.向浓氨水中开始滴入硫酸铝溶液:
A13++3NH3+H2O→A1(OH)3↓+3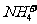
5. 能正确表示下列反应的离子方程式是 ( )
A.醋酸钠的水解反应 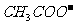 +H3O+=CH3COOH+ H2O
+H3O+=CH3COOH+ H2O
B.碳酸氢钙与过量的NaOH溶液反应
Ca2++2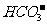 +2
+2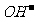 =CaCO3↓+ 2H2O+
=CaCO3↓+ 2H2O+ 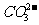
C.苯酚钠溶液与二氧化碳反应 C6H5O-+
CO2+ H2O=C6H5OH+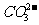
D.稀硝酸与过量的铁屑反应 3Fe+8H++2 =3Fe3++2NO↑+4 H2O
=3Fe3++2NO↑+4 H2O
4. 下列离子方程式书写正确的是: ( )
A.用铂电极电解氯化镁溶液: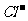 +2H2O
+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.NaHSO4溶液中滴入Ba(OH)2溶液至中性:H++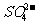 +Ba2+十OH-===BaSO4↓+H2O
+Ba2+十OH-===BaSO4↓+H2O
C.在H2O2中加入酸性KMnO4溶液:2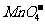 +5H2O2+6H+====2Mn2+
+5O2↑+8H2O
+5H2O2+6H+====2Mn2+
+5O2↑+8H2O
D.溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5Br +OH-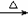 CH2=CH2↑+Br-+H2O
CH2=CH2↑+Br-+H2O
3. 在一无色未知液中已检出有Al3+存在,在此溶液中能大量共存的离子组是 ( )
A.Na+、NH4+、 、
、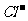 B.K+、Na+、
B.K+、Na+、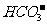 、
、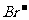
C.Na+、H+、 、
、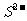 D. K+、Fe2+、
D. K+、Fe2+、 、
、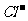
2. 在下述条件下,一定能大量共存的离子组是 ( )
A.无色透明的水溶液中:K+、Ba2+、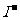 、
、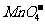
B.含有大量 的水溶液中:NH4+、Fe2+、
的水溶液中:NH4+、Fe2+、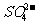 、H+
、H+
C.c (HCO3-)=0.1 mol·L-1的溶液中:Na+、K+、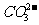 、
、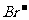
D.酸性溶液中: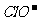 、
、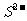 、
、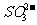 、Na+
、Na+
1. 在下述条件下,一定能大量共存的离子组是 ( )
A.无色透明的水溶液中:K+、Ba2+、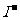 、
、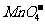
B.含有大量NO3-的水溶液中:NH4+、Fe2+、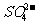 、H+
、H+
C.c (HCO3-)=0.1 mol·L-1的溶液中:Na+、K+、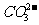 、
、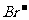
D.强碱性溶液中:ClO-、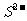 、
、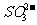 、Na+
、Na+
17. (1)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。
该反应中还原产物是______;若反应过程中转移了0.3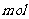 电子,则氧化产物的质量是______
电子,则氧化产物的质量是______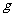 。
。
(2)将a mol Cl2 通入含b mol FeBr2的溶液中,当0< a / b≤1/2 时,反应的离子方程式为:
2Fe2+ + Cl2 = 2Fe3+ + 2Cl- ,写出另2个可能发生的离子方程式
① 当 a / b =1时____________________________________________;
② 当a / b≥3/2时____________________________________________。
③ (3)观察如下反应,总结规律,然后完成下列问题:
①Al(OH)3 +H2O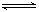 Al(OH)4- + H+ ②NH3+H2O
Al(OH)4- + H+ ②NH3+H2O NH4+ + OH_
NH4+ + OH_
(A)已知B(OH)3是一元弱酸,试写出其电离方程式__________________________________
(B)N2H4是二元弱碱,试写出其第二步电离方程式____________ ____
16.(1)配平氧化还原反应方程式:
__ C2O42-+__MnO4-+__H+= __CO2+__Mn2++__H2O
(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250mL溶液。量取两份此溶液各25mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25mol/LNaOH溶液至20mL时,溶液由无色变为浅红色。该溶液被中和的H+的物质的量为 mol;
②第二份溶液中滴加0.10mol/L的酸性高锰酸钾溶液至16mL时反应完全,此时溶液颜色由 变为 。该溶液中还原剂的物质的量为 mol;
③原试样中H2C2O4·2H2O和KHC2O4的质量分数分别是多少?
(请列式计算,写出运算过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com