
15. 有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验。通过SO2气体,将带余烬的木条插入试管C中,木条复燃。

请回答下列问题: (1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是:____________。 (2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3。 (3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:

上述方案是否合理?______________________________________________________。 请简要说明两点理由:①______________________;②___________________________。 16.为了测定足量铜与适量一定浓度的浓硝酸反应生成一氧化氮气体和二氧化氮气体的物质的量之比(用m表示),请从下图中选用合适的实验装置,设计一个合理而简单的实验,用于测定阴的值。(不考虑二氧化氮转化为四氧化二氮)其中E装置由甲、乙两根玻璃管组成,用橡皮管连通,并装人适量水,甲管有刻度(0-50mL),供量气用,乙管可上下移动,用来调节液面高低。回答下列问题:
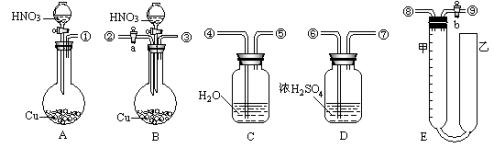
(1)装置的连接顺序是(填各接口的编号入____________。 (2)连接好装置并检查气密性后,应打开____________通人氮气;然后打开____________,从乙管注水至充满甲、乙两管,关上a、b。通人氮气的原因是____________。 (3)实验后,若量气管中气体的体积为VmL(已换算成标准状况下),要测定m的值,还要将中的溶液作_______实验,假设测得其中溶质物质的量为n,用含V和n的式子表示m:____________。 (4)下列操作中能造成m值偏小的是( ) A.反应前E中甲管所装水里气泡没赶尽,而最后读数时气泡消失 B.实验前,甲、乙两管液面在同一水平面上,最后读数时乙管的液面高于甲管的液面 C.实验前没有先通人足量的氮气 D.实验过程中,E装置乙管的水溢出 三、推断填空题
13、A是一种白色晶体,它与浓NaOH溶液共热,放出无色气体B。用圆底烧瓶收集干燥的B。按图所示装置仪器,挤压滴管的胶头时,可以得到蓝色喷泉;A与浓H2SO4反应,放出无色气体C。用圆底烧瓶收集干燥的C,仍按图所示装置仪器,挤压滴管的胶头时,可以得到红色喷泉。
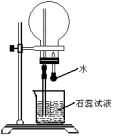
(1)A的化学式是____________。 (2)可用于除去B中水分的干燥剂是____________。收集气体B的方法是____________。 (3)收集气体C的方法是____________。 14、用下列装置连接成一套测定水的组成的实验装置。
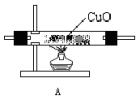
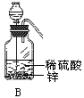
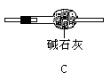
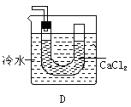
(1)所用装置的连接顺序是____________。 (2)装置C的作用是_______,若不用C,测得的氢、氧质量比会_________(偏高或偏低)。 (3)测量数据如下,则水中氢和氧的质量比为____________。
|
|
实验前 |
实验后 |
|
氧化铜和玻璃管质量 |
M1 |
M3 |
|
氯化钙和U形管质量 |
M2 |
M4 |
(4)如果在停止加热的同时就停止通氢气,并拆开装置,则测定结果氢与氧的质量比________。(偏高或偏低)
12.[山东省聊城一中08-09高三期末综合]将22.4 g铁粉逐渐加入到含HNO3 0.8 mol的稀硝酸中,反应生成的气体的物质的量(x)随消耗铁粉的物质的量(y)变化关系中正确的是 ( )
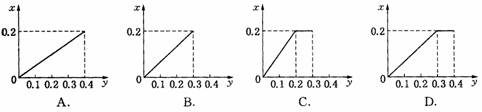
11. 在氯化钡溶液中通人SO2,溶液仍澄清;若将氯化钡溶液分盛两试管,一支加硝酸,另一支加烧碱溶液,然后再通人SO2,结果两试管都有白色沉淀,由此得出的结论合理的是( ) A.氯化钡有两性 B.两支试管中的沉淀均是亚硫酸钡 C.SO2有还原性,水溶液有酸性 D.升高pH使SO2水溶液中SO32-浓度降低
7. 某无色混合气体中可能含有CO2、CO、H2、H2O(气)中的一种或几种,依次进行如下处理(假定每次处理均反应完全):(1)通过碱石灰时,气体体积变小;(2)通过赤热的氧化铜时,固体变为红色;(3)通过无水硫酸铜粉末时,变为蓝色;(4)通过澄清石灰水时,溶液变浑浊。由此可以确定原混合气体中( ) A.一定含有CO、H2O,可能含有H2、CO B.一定含有H2O、CO,可能含有CO2、H2 C.一定含有CO、CO2,可能含有H2O、H2 D.一定含有CO、H2,可能含有H2O、CO2 8. 当锌与某浓度的硝酸反应时,如果参加反应的锌与硝酸物质的量之比为2:5,则硝酸的还原产物可能是( ) A.N2O B.NO C.N2 D.NH4NO3 9. 最近,科学家研制得到一种新的分子,它具有空心类似足球状的结构,化学式为C60。则下列说法正确的是( ) A.C60是一种新型化合物 B.C60中含离子键 C.C60与石墨都是碳的同素异形体 D.C60的摩尔质量为720 10. 下列说法不正确的是( ) A.陶瓷分为氧化物陶瓷和非氧化物陶瓷 B.生产普通水泥的原料是石灰石和粘土 C.玻璃是一种新型无机非金属材料 D.氮化硼陶瓷是一种新型无机非金属材料
5. 硒(Se)为第四周期VIA族元素,根据它在周期表中的位置,推测硒不可能具有的性质是( ) A.通常状况下是固体 B.SeO的水化物是一种酸 C.H2Se比H2S稳定 D.有+6、+4、-2三种常见的化合价 6、检验SO2气体中是否混有CO2气体,可采用的方法是( ) A.通过品红溶液 B.通过澄清石灰水 C.先通过NaOH溶液,再通过澄清石灰水 D.先通过酸性高锰酸钾溶液,再通过澄清石灰水
4.(山东省郯城三中08-09学年度上学期高三期末测试)下列说法正确的是 ( )
①电解质溶液导电过程属于化学变化
②稀有气体不活泼的原因是它们原子的最外层都达到8电子稳定结构
③FeC12、Fe(OH)3、NO都能通过化合反应来制取
④SiO2是制造光导纤维的材料
A.②④ B.①④ C.①③④ D.②③
2.CCTV《科技博览》中报道,2004年中科院首创用CO2合成可降解塑料聚二氧化碳。下列说法合理的是( ) A.聚二氧化碳塑料是通过加聚反应制得的B.聚二氧化碳塑料与干冰互为同素异形体 C.聚二氧化碳塑料与干冰都属于纯净物D.聚二氧化碳塑料的使用会产生白色污染 3.下列关于水污染叙述错误的是( ) A.水污染的程度,是由其溶氧量来测定 B.污染水的金属元素如汞、镉、铅等的含量极少时,不会对生物造成伤害 C.使用含磷洗衣粉,会造成河水、湖水污染,使海藻疯狂生长,鱼类死亡 D.工业冷却所排出的热水危害水生生物
1. 常见的污染物分为一次污染物和二次污染物。二次污染物是排人环境中的一次污染物在物理化学因素或微生物作用下,发生变化所生成的新污染物。如反应2NO+O2=NO2中,二氧化氮为二次污染物。下列三种气体:①硫化氢②二氧化硫③汽油,其中能生成二次污染物的是( ) A.①② B.②③ C.①③ D.全部都是
16.(15分)如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
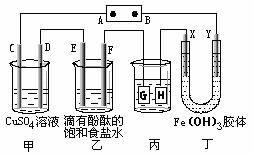
请回答:
(1)B极是电源的 ,一段时间后,甲中溶液颜色 ,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 ,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 。
(3)现用丙装置给铜件镀银,则H应该是 (填“镀层金属”或“镀件”),电镀液是 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为 ,甲中溶液的pH (填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com