
4.在容积相等的甲乙两个密闭容器中,分别都充入2mol SO2和1mol O2,使它们在相同温度下发生反应2SO2(g)+O2(g) 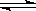 2SO3(g)。设在反应过程中,甲容器保持体积不变,乙容器保持压强不变,达到平衡后,如甲容器中SO2的转化率为25%,则乙容器中SO2的转化率应当是 ( )
2SO3(g)。设在反应过程中,甲容器保持体积不变,乙容器保持压强不变,达到平衡后,如甲容器中SO2的转化率为25%,则乙容器中SO2的转化率应当是 ( )
A.25% B.< 25% C.>25% D.无法判断
3.对于可逆反应2SO2(g)+O2(g) 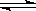 2SO3(g)
,ΔH= -98.3kJ/mol。下列说法中正确的是
2SO3(g)
,ΔH= -98.3kJ/mol。下列说法中正确的是
A.达到平衡时,反应物和生成物的浓度一定相等
B.达到平衡时,反应物和生成物的物质的量保持不变
C.加入催化剂,可以提高SO2的转化率
D.升高温度,可以提高SO2的转化率
B.提高训练
2.大气污染是环境污染的一个重要方面,常见的大气污染分一次污染物和二次污染物。二次污染物在物理、化学因素或生物作用下发生变化,或与环境中的其它物质发生反应,生成新的污染物。如2NO + O2=2NO2,则NO2就是二次污染物,由NO2导致的污染就是NO的二次污染。下列物质①SO2 ②NO ③NO2 ④HCl ⑤CO2不易导致二次污染的是
A.①②③④⑤ B.①③⑤ C.④⑤ D.只有④
1.“绿色化学”(Green Chemistry)的目标是研究和寻找能充分利用的无毒害原料,最大限度地节约能源,在化工生产各个环节都实现净化和无污染的反应途径。下列各项属于“绿色化学”的是 ( )
A.处理废弃物 B.治理污染点 C.减少有毒物质 D.杜绝污染源
4.为防治酸雨,降低煤燃烧时向大气排放的SO2,工业上将生石灰和含硫煤
混合使用。请写出燃烧时,有关“固硫”(不使含硫化合物进入大气)反应的
化学方程式: 。
思维方法: 。
展望高考:
[针对训练]
A.基础训练
3.以下烟气经净化处理后,可用做气体燃料的有( )。
①硫酸工业尾气 ②硝酸工业尾气 ③高炉煤气 ④焦炉煤气 ⑤炼钢过程中产生的棕色烟气 ⑥煅烧石灰石的气体产物
A.①②④ B.①③⑤ C.③④⑤ D.④⑤⑥
思维方法: 。
展望高考:
2.下列说法中不正确的是( )。
A.硫酸工业的尾气必须回收、净化处理,主要为了充分利用原料
B.“酸雨”中主要含有硫的氧化物以及所形成的硫酸及硫酸盐
C.大气中,大量的SO2来源于煤和石油燃烧、金属矿石的冶炼
D.消除大气污染的主要方法之一是减少污染物的排放
思维方法: 。
展望高考:
1.目前我国许多城市和地区定期公布空气质量报告,在空气质量报告中,一般不涉及
A.SO2 B.NO2 C.CO2 D.可吸入颗粒物
思维方法:
展望高考:
4.讨论:学过的化工生产(如钢铁工业、合成氨、硝酸工业、煤和石油
化工、氯碱工业等)中,应该如何处理环境和综合经济效益等问题?
[例题解析]
[例1]在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,
采用了中间有热交换器的接触室(如右图),图中在a、b、c处流入或流
 出的气体正确的是
( )
出的气体正确的是
( )
A.a处SO2、N2 B.b处SO2、O2、N2
C.a处SO3、O2 D.c处SO3、N2
解题思路: 。
易错点: 。
[例2]在接触法制硫酸的工业生产中,下列生产操作及其原因解释二者都正确
的是( )
A.硫铁矿燃烧前需要粉碎,因为块状硫铁矿不能燃烧
B.SO2氧化为SO3时需要高压,这样可以提高SO2的转化率
C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
D.用98.3%的浓H2SO4吸收SO3,可以防止形成酸雾阻碍SO3的吸收
解题思路: 。
易错点: 。
|
FeS2→SO2→SO3→H2SO4, NH3→NO→NO2→HNO3
下列说法正确的是( )。
A.所有变化都是氧化-还原反应 B.②③⑤⑥都是化合反应
C.②④反应都要用催化剂 D.②⑥反应需要足量的氧气
[例4]接触法制硫酸的原料是 ,生产过程的化学反应
原理: 。
解题思路: 。
易错点: 。
[例5]硫酸最古老的生产方法是:把绿矾装入反应容器中加强热,会流出油
状物,并放出有刺激性气味的气体,反应容器中的固体变为红色。这个变化 过程可用两个化学方程式表示 ,
.。
解题思路: 。
易错点: 。
[例6]在氧气中灼烧0.8g由硫、铁元素组成的化合物,使其中的硫经过一系
列变化最终全部转化为硫酸,用20 mL 1 mol·L-1的烧碱溶液恰好能完全中和这些硫酸,则原混合物中硫的质量分数约为 .。
解题思路: 。
易错点: 。
[例7]含FeS280%的硫铁矿,煅烧时损失硫5%,SO2氧化成SO3时利用率为98%,问生产1 t 98%的硫酸,需要这种硫铁矿多少t?
解题思路: 。
易错点: 。
[例8]取1g含SiO2和FeS2的矿石样品,在氧气中充分燃烧,残余固体质量为0.84g,用这种矿石100吨,可以制得98%的H2SO4多少吨?(设生产过程中硫损失2%)
解题思路:
易错点:
[考题再现]
3.如果要筹建一间硫酸厂,你认为应该考虑哪些因素?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com