
9.1895年有人题联京师城门:“万寿无疆,普天同庆;三军败绩,割地求和”。其中“割地”是指
A.割九龙司给英国 B.割香港岛给英国
C.割台湾、彭湖列岛给日本 D.划分北京东交民巷为使馆界
8.下列文件中属于近代中国第一个具有资本主义性质的社会改革方案的是

7.“经济上的暴力强制”是近代史上外国在华关系的一个重要特征。就连外国人也承认在华洋商人“个个都是大恶棍”,美国公使承认说:“我们的国旗曾经用来庇护在中国的所有流氓”。外国政府“庇护”在华外国“恶棍”、“流氓”所依据的特权是
A.设立和管理租界的权 B. 海关管理权
C. 领事裁判权 D. 片面最惠国待遇权
6.19世纪中期,欧美列强竭力推行对外侵略扩张政策根本目的在于
A.资本主义本性是殖民扩张
B.打开商品国外市场,夺取廉价原料产地
C.经济军事实力增强保护对外贸易
D.建立世界资本主义统一市场
5. 明清时期,民众衣食结构发生了重大变化,主要是因为
①小麦开始在南方广泛种植 ② 国外高产农作物玉米和甘薯的引进和推广
③ 棉花的广泛种植 ④ 丝织业的发达
A.①②③ B. ②③④ C. ②③ D. ①②③④
4. 图片中这一出土文物的用途主要是
图片中这一出土文物的用途主要是
A.装饰用品
B.松地下种
C.刻写文字
D.战争武器
3.宋代中枢权力体系中,掌管财政的是
A.尚书省 B.中书门下 C.枢密院 D.三司
2.据《资治通鉴》卷192载,唐太宗贞观元年对群臣说:“中书诏敕或有差失,则门下当然驳正。人心所见,至有不同,苟论难往来,务求至当,舍己从人,亦复何伤!比来护己之短,遂成怨隙,或苟避私怨,知非不正,顺一人之颜情,为兆民之深患,此乃亡国之政也。”对以上言论的理解正确的是
①门下省的设立主要是为了减少决策的失误
②唐太宗注重利用集体智慧提高决策效果
③说明唐朝的统治具有一定的民主性
④说明唐朝统治者注重运用中央机构的权力制衡机制来维护皇权
A.②③④ B.①③④ C.①②③ D.①②④
1.柳宗元《封建论》言:“陵夷迄于幽、厉,(周)王室东徙,而自列为诸侯。厥后,问鼎之轻重者有之,射王中肩者有之,伐凡伯、诛苌弘者有之,天下乖戾,无君君之心。”这些现象反映的实质问题是
A.东周时期我国封建制逐渐形成 B.周朝推行的分封制在走向崩溃
C.东周的统治越来越腐败 D.诸侯争霸导致天下大乱
5、其他类型
※※关注利用溶液中阴阳离子的种类来判断溶液中溶质的可能情况:
有些题目给定了盐溶液中的阴阳离子种类,可以假设该溶液是相应酸与碱反应后的产物,因此存在酸碱过量问题。
[例1]已知某无色透明的溶液中所含的离子仅有Na+、CH3COO-、H+和OH-四种离子,试回答下列问题:
⑴该溶液所含的四种离子的物质的量浓度大小之间的关系是否只有一种可能 (填“是”或“否”),其原因是: 。
⑵某学生将该溶液中的四种离子的物质的量浓度按从大到小的顺序排列了若干种可能,其中合理的是:
A. c(Na+)>c(CH3COO-)>c(OH-)>c(H+) B. c(CH3COO-)=c(Na+)>c(OH-)=c(H+)
C. c(H+)>c(OH-)>c(Na+)>c(CH3COO-) D. c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
解析:由于溶液中所含的离子仅有Na+、CH3COO-、H+和OH-四种离子,所以可以认为是醋酸和NaOH反应后的溶液。因此该溶液中可能含有溶质CH3COONa ; CH3COONa、CH3COOH; CH3COONa、NaOH等情况 所以该溶液所含的四种离子的物质的量浓度大小之间的关系不能只有一种。第(2)问中C D选项不符和溶液中电荷守恒规律,选AB.
练习.已知某溶液中存在Cl-、NH4+、H+、OH- 四种离子经过四位同学测定其浓度大小关系如下,其中不可能的是 ( )
A.C(Cl-)>C(NH4+)>C(H+)>C(OH-) B. C(Cl-)>C(H+)>C(NH4+)>C(OH-)
C.C(Cl-)>C(NH4+)>C(OH-)>C(H+) D. C(OH-)>C(H+)>C(Cl-)>C(NH4+)
※※对所给的二元酸的电离,要关注电离的程度:是否完全电离。
[例2]某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A==H++HA;HA-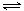 H++A2- 回答下列问题:
H++A2- 回答下列问题:
⑴Na2A溶液显 (填“酸性”,“中性”,或“碱性”)。理由是: (用离子方程式表示)
⑵在0.1mol·L-1的Na2A溶液中,下列微粒浓度关系式正确的是: 。
A. c(A2-) +c( HA-)+c( H2A) =0.1mol·L-1 B. c(OH-)=c(H+) +c( HA-)
C. c(Na+ )+ c(H+) =c(OH-)+ c( HA-)+2c(A2-) D. c(Na+ )= 2c(A2-) +2c( HA-)
⑶已知0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1 H2A溶液中氢离子的物质的量浓度可能是 0.11 mol·L-1(填“<”,“>”,或“=”),理由是:
⑷0.1mol·L-1 NaHA溶液中各种离子浓度由大到小的顺序是:
解析:由于“H2A==H++HA;HA-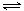 H++A2-”,因此在NaHA溶液中仅存在:
H++A2-”,因此在NaHA溶液中仅存在:
HA-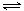 H++A2- 电离情况,没有HA-的水解过程。在H2A溶液中H2A第一步电离产生的H+,抑制了HA-的电离。理解上述内容,答案迎刃而解。
H++A2- 电离情况,没有HA-的水解过程。在H2A溶液中H2A第一步电离产生的H+,抑制了HA-的电离。理解上述内容,答案迎刃而解。
练习:某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:
H2A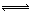 H++HA-;HA-
H++HA-;HA-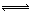 H++A2- 已知一级电离远大于二级电离,设有下列四种溶液:
A.0.01mol.L-1的H2A溶液 B.0.01mol.L-1的NaHA溶液( C(OH-)>C(H+) )
C.0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
D.0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
H++A2- 已知一级电离远大于二级电离,设有下列四种溶液:
A.0.01mol.L-1的H2A溶液 B.0.01mol.L-1的NaHA溶液( C(OH-)>C(H+) )
C.0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
D.0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
(1) B溶液中可能存在的等式关系有
D溶液中可能存在的等式关系有
(2) C(H+)最大的是______________________,最小的是______________________。
(3)C(H2A)最大的是______________________,最小的是______________________。 (4)C(A2-)最大的是______________________, 最小的是______________________。
※※关注隐含信息的发掘:
[例3]今有一混合物的水溶液,只可能含有以下离子中的若干种:
K+、NH4+、Cl-、Mg2+、Fe3+、CO32-、SO42-,现每次取100.00ml进行实验。
① 第一份加入AgNO3溶液有沉淀产生。
② 第二份加足量NaOH后加热,收集到气体0.896L(标准状态下)。
③ 第三份加足量BaCl2后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩2.33g。
试回答有关问题:
⑴判断K+、Cl-是否存在?K+ ;Cl- (填下列序号)。
A.一定存在 B.可能存在 C.一定不存在
⑵肯定存在的离子在原溶液中的物质的量浓度分别为: 。
解析:由①可知溶液中Cl-、CO32-、SO42-三种中至少含有其中一种;由②能确定含NH4+,且c(NH4+)=0.4mol·L-1,第③步可以确定c(SO42-)=0.1mol·L-1;c(CO32-)=0.2mol·L-1,由于含有CO32-、SO42-,所以溶液中肯定不含Mg2+、Fe3+;因为溶液中阴阳离子所带电荷相等(即溶液是电中性的,这也是该题目隐含的信息),由上述所求的已知阴阳离子的浓度看出,是不守恒的,因此溶液中一定存在K+,且c(K+)≥0.2mol·L-1,Cl-不确定。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com