
10. (天津市天津一中2010届高三第四次月考理科)已知抛物线 与双曲线
与双曲线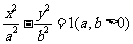 有相同的焦点
有相同的焦点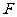 ,点
,点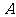 是两曲线的一个交点,且
是两曲线的一个交点,且 轴,若
轴,若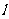 为双曲线的一条渐近线,则
为双曲线的一条渐近线,则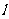 的倾斜角所在的区间可能是( D )
的倾斜角所在的区间可能是( D )
A.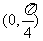 B.
B.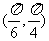 C.
C. D.
D.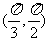
3.(天津市六校2010届高三第三次联考文科)已知双曲线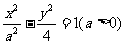 的右焦点与抛物线
的右焦点与抛物线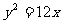 的焦点重合,则该双曲线的离心率为 ( B
)
的焦点重合,则该双曲线的离心率为 ( B
)
A.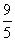 B.
B.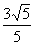 C.
C.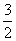 D.
D.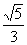
3.(天津市武清区2009-2010学年高三下学期第一次模拟文)若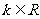 ,则方程
,则方程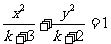 表示焦点在
表示焦点在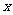 轴上的双曲线的充要条件是( A )
轴上的双曲线的充要条件是( A )
A.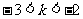 B.
B.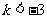
C.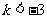 或
或 D.
D.
4.(天津市武清区2009-2010学年高三下学期第一次模拟理)若双曲线的焦点到其渐近线的距离等于实轴长,则该双曲线的离心率为( A )
A.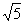 B.5
B.5
C.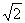 D.2
D.2
9.(天津十二区县重点中学2010年高三联考一理)已知抛物线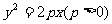 上一点
上一点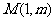
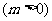 到其焦点的距离为
到其焦点的距离为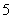 ,双曲线
,双曲线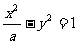 的左顶点为
的左顶点为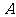 ,若双曲线一条渐近线与直线
,若双曲线一条渐近线与直线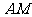 平行,则实数
平行,则实数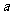 等于(A
)
等于(A
)
A.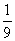 B.
B.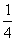 C.
C.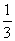 D.
D.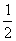
23.(8分)50mL密度为1.84g/cm3、质量分数为98%的浓H2SO4,其物质的量浓度为_____ ______;若将50mL该浓H2SO4稀释成密度为1.47g/cm3的溶液100mL,需水__________mL(ρ水=1g/cm3),稀释后溶液的质量分数为____________,物质的量浓度为____________。
贵州省兴义市龙盘中学2010届高三第一次月考
22.(6分)如图是医生为病人输液时用的一瓶质量分数为5 % 的葡萄糖(C6H12O6)注射液标签.请认真观察标签上所列的内容后填写:
(1).该溶液中还有水_________________g;
(2).该溶液的密度约为____________________g·mL-1 ;
(3).该溶液中溶质的物质的量浓度为________________mol/L。
21.(14分)实验室用固体烧碱配制500ml,0.1mol/LNaOH溶液
(1)需要称取__________g的烧碱固体,固体应放在__________中称量。
(2)配制的过程中不需要使用的仪器是__________(填标号字母)
A. 托盘天平 B.烧杯 C.玻璃棒
D.1000ml的容量瓶 E.碱式滴定管 F.胶头滴管
(3)根据实验的实际需要和(2)中所列出的仪器判断,完成该实验还缺少的玻璃仪器是 。
(4)在容量瓶内确定溶液体积的过程中,完成后期加入少量的水的操作方式是
。
(5)下列各项操作中,可能导致实际浓度偏高的是__________。(填选项字母)
A.称量NaOH固体时,砝码和物质的位置对调
B.向容量瓶中转移时,不慎洒出
C.NaOH溶解时放出大量的热,未及冷却立即配制溶液
D.定容时,仰视容量瓶的刻度线
E.定容时,加水超过刻度线,再用胶头滴管吸出多余的部分
(6).下图分别表示四种操作,其中有两处错误的是 ( )
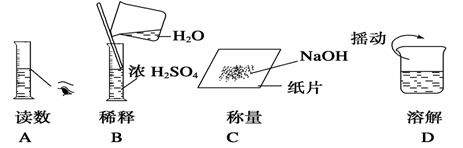
20.(8分)关于下面氧化还原反应方程式,完成相关问题:
__KClO3 + ___ HCl →___ Cl2 + ___ H2O + ___ KCl
(1)配平该反应方程式,并用双线桥法或单线桥法表示该反应的电子转移方向和数目:
(2)氧化剂__________,被氧化元素是____________ ;(填分子式,下同)
(3)HCl的作用是_________________,还原产物是_______________;
19. (7分)下列4组物质均有一种物质的类别与其它3种不同:
A.CaO、Na2O、CO2、CuO B.H2、C、P、Cu
C.O2、Fe、Cu、Zn D.HCl、H2O、H2SO4、H2CO3
(1)分别找出各组物质中与另外3种物质不同类的物质,它们是(填化学式):
A组___________;B组___________; C组___________;D组___________。
(2)这四种物质相互作用可生成一种新物质碱式碳酸铜[化学式Cu2(OH)2CO3],该反应 ______________ 氧化还原反应(填“是”或“不是”),原因是 _______________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com