
5.从长度为1,2,3,4,5的五条线段中,任取三条的不同取法共有n种,在这些取法中,以取出的三条线段为边可组成钝角三角形的个数为m,则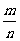 等于( )
等于( )
A.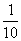 B.
B.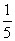 C.
C. D.
D.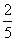







4.一个口袋里装有m个白球,n个黑球,从口袋中每次拿出一个球,不放回,第k次拿到黑球的概率是( )
A.
 B.
B.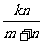 C.
C.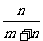 D.
D.

3. 对一组数据 ,如果将它们改变为
,如果将它们改变为 其中
其中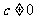 ,则下面结论正确的是( )
,则下面结论正确的是( )

A.平均数与方差均不变
B. 平均数变了,方差不变

C. 平均数不变,方差变了
D. 平均数与方差都变了 
2.
从2008名学生中选取50名学生参加数学竞赛,若采用下面的方法选取:先用简单随机抽样从2008人中剔除8人,剩下地2000人再按系统抽样的方法抽取50人,则在20008人中,每人入选的机会( )

A.不全相等
B. 均不相等

C. 都相等,且为 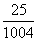 .
D. 都相等,且为
.
D. 都相等,且为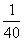 .
.
1.数据5,7,7,8,10,11的标准差是( )
A.8 B.4 C.2 D.1

二者的辩证关系是:化学键发生变化,物质不一定发生化学变化;物质发生化学变化时,化学键一定发生变化。物理变化中可能有化学键的断裂,也可以没有化学键的断裂。
化学变化的实质是:旧的化学键的断裂和新的化学键的形成。
化学变化的特点是:发生化学变化过程中有新物质生成。
例题1.关于范德华力的叙述中,正确的是( )
A.范德华力的实质也是一种电性作用,所以范德华力是一种特殊的化学键
B.范德华力与化学键的区别是作用力的强弱问题
C.任何分子间在任意情况下都会产生范德华力
D.范德华力非常微弱,故破坏范德华力不需要消耗能量
解析:范德华力是分子与分子之间的一种相互作用,其实质与化学键类似,也是一种电性作用,但两者的区别是作用力的强弱不同,化学键必须是强烈的相互作用(120-800KJ·mol-),范德华力只有几到几十千焦每摩尔,故范德华力不是化学键;虽然范德华力非常微弱,但破坏它时也要消耗能量;范德华力普遍地存在于分子之间,但也必须满足一定的距离要求,若分子间的距离足够大,分子之间也难产生相互作用。所以只有B正确。
例题2.下列关于范德华力影响物质性质的叙述中,正确的是( )
A.范德华力是决定由分子构成物质熔、沸点高低的唯一因素
B.范德华力与物质的性质没有必然的联系
C.范德华力能够影响物质的化学性质和物理性质
D.范德华力仅是影响物质部分物理性质的一种因素
解析:范德华力不能影响物质的化学性质,仅能影响由分子构成的物质的部分物理性质,如熔点、沸点及溶解性,并且不是唯一的影响因素。
例题3.H2O与H2S结构相似,都是V型的极性分子,但是H2O的沸点是100oC,H2S的沸点是-60.7 oC。引起这种差异的主要原因是( )
A.范德华力 B.共价键 C.氢键 D.相对分子质量
解析:水分子之间存在氢键和范德华力两种分子间作用力,而H2S分子之间只有范德华力,没有氢键,所以,H2O的沸点高。
例题4.金属的下列性质中,与金属键无关的是( )
A.良好的导电性 B.反应中易失电子 C.良好的延展性 D.良好的导热性
解析:根据金属具有的物理性质的通性知,大多数金属有金属光泽,硬度大,熔点高,不透明,良好的导电性、导热性、延展性等。而金属易失电子是金属性的化学性质。所以,B正确。
例题5、下列关于金属键的叙述中,不正确的是( )
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈的相互作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子的相互作用,故金属键无饱和性和方向性D.构成金属键的自由电子在整个金属内部的三维空间中做自由运动
解析:从基本构成微粒的性质看,金属键与离子键的实质类似,都属于电性作用,特征是都无方向性和饱和性,自由电子是由金属原子提供的,并且在这个金属内部的三维空间内运动,为整个金属的所有阳离子所共有,从这个角度看,金属键与共价键有类似之处,但是两者又有明显的不同。不正确是B.
4.金属键与金属的物理性质
金属键是在整个晶体的范围内起作用
(1)导电性与导热性:金属晶体中的自由电子在外加电场的作用下发生定向移动,形成电流;升高温度,导电性减弱;自由电子通过碰撞进行能量传递,使金属晶体具有良好的导热性;
(2)金属晶体的延展性:金属晶体通常采用密堆积方式,在锻压或捶打时,密堆积层的金属原子之间比较容易产生相对滑动,但是不会破坏密堆积的排列方式,而且在滑动的过程中自由电子能够维系整个金属键的存在,因此金属虽然发生了形变但是不致断裂,所以金属通常具有良好的延展性和可塑性。
(3)金属晶体的熔点、硬度取决于金属键的强弱,金属的价电子数越多,原子半径越小,金属键越强,晶体的熔点越高、硬度越大。因为金属键的强弱差别较大,金属晶体的熔点和硬度差别也较大。
3.金属键的强弱:与金属阳离子的半径大小和金属原子的价电子的多少有关。金属阳离子的
半径越小,金属原子的价电子越多,金属键越强。
2.金属键的特征:金属键没有方向性和饱和性,金属原子紧密的堆积在一起。
3.成键性质:电性作用。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com