
2.化学之“化”
风化--结晶水合物在自然条件下失去部分或全部结晶水的过程。
催化--能改变反应速率,本身参与化学反应,但质量和性质在反应前后都不改变。
歧化--同一物质中同一元素且为同一价态原子间发生的氧化还原反应。
酸化--向某物质中加入稀酸使之呈酸性的过程。(酸性高锰酸钾应用什么酸酸化?)
钝化--浓硫酸、浓硝酸在Fe Al等金属表面氧化生成一种致密的氧化膜从而起到保护Fe Al等金属的现象。
水化--物质与水作用的过程。
氢化(硬化)--液态油在一定条件下与H2发生加成反应生成固态脂肪的过程。
皂化--油脂在碱性条件下发生水解反应的过程。
老化--橡胶、塑料等制品露置于空气中,因受空气氧化、日光照射等作用而变硬发脆的过程。
硫化--向橡胶中加硫,以改变其结构来改善橡胶的性能,减缓其老化速度的过程。
裂化--在一定条件下,分子量大、沸点高的烃断裂为分子量小、沸点低的烃的过程。
酯化--醇与酸反应,生成酯和水的过程。
硝化(磺化)--苯环上的H被-NO2或-SO3H取代的过程。
[例2](2008·广东中山)古诗词是古人为我们留下的宝贵精神财富。下列诗句中只涉及物理变化的是( )
A.野火烧不尽,春风吹又生 B.千锤万出凿深山,烈火焚烧若等闲
C.只要工夫深,铁杵磨成针 D.春蚕到死丝方尽,蜡炬成灰泪始干
[解析]“野火烧不尽,春风吹又生”“ 春蚕到死丝方尽,蜡炬成灰泪始干”涉及到物质的燃烧,属于化学变化;“千锤万出凿深山,烈火焚烧若等闲”是指石灰石(CaCO3)受热分解,属于化学变化。
[答案]C
考点三 物质的分类
1.物理变化和化学变化的比较:
(1)特征:有无新物质生成
(2)本质:有无化学键的断裂和形成
(3)现象:物理变化→大小、形状、状态改变
化学变化→发光、发热、变色、析出沉淀等
(4)典型实例:
物理变化:⑴升华 ⑵萃取 ⑶分液 ⑷蒸馏(分馏) ⑸吸附 ⑹渗析 ⑺盐析
⑻胶体聚沉 ⑼电泳 ⑽金属导电 (11)焰色反应 (12)电离等
化学变化:⑴风化 ⑵裂化 ⑶硫化 ⑷老化 ⑸炭化 ⑹干馏 ⑺脱水 ⑻蛋白质变性 ⑼水解 ⑽同素异形体互变 (11)电解 (12)熔融盐导电
(13)电解质溶液导电 (14)水泥硬化等。
2.同位素与同素异形体:
|
|
同位素 |
同素异形体 |
|
定义 |
同种元素形成的不同种原子 |
同种元素形成的不同种单质 |
|
区别 |
是一种原子 |
是一种单质 |
|
联系 |
同位素原子在一定条件下以一定的方式可构成同素异形体 |
|
|
实例 |
16O 和18O ;12C 和 14C |
O2和O3
;金刚石和石墨 |
[例1](2008·山东潍坊)2006年2月17日,新加坡卫生暑公布,新加坡近期真菌性角膜炎患者激增。去年5月以来,当地主要医院收治的19名真菌性角膜炎患者中,18名曾使用博士伦公司生产的多功能隐形眼镜护理药水。多功能隐形眼镜护理药水的主要成分是双氧水(H2O2),下列有关双氧水的说法正确的是( )
A.它是由氢气和氧气组成
B.它由两个氢元素和两个氧元素组成
C.每个H2O2分子是由氢元素和氧元素组成
D.每个H2O2分子是由2个氢原子和2个氧原子构成
[解析]双氧水(H2O2)是分子,分子是由原子构成的;元素是宏观概念,不能论个数。
[答案]D
[知识规律]
物质到底是由分子、原子还是离子构成?这与物质所属的晶体类型有关。如金刚石(C)、晶体Si都属原子晶体,其晶体中只有原子;NaCl、KClO3属离子晶体,其晶体中只有阴阳离子;单质S、P4属分子晶体,它们是由原子形成分子,进而构成晶体的。具体地:
(1)由分子构成的物质(分子晶体):
①非金属单质:如H2、X2、O2、O3、N2、P4、S、C60、稀有气体等
②非金属氢化物:如HX、H2O、NH3、H2S等
③酸酐:如SO2、CO2、SO3、P2O5、N2O5 等
④酸类:如HClO4、HClO、H2SO4、H3PO4、H2SiO3等
⑤有机物:如烃类、烃的衍生物、糖类、氨基酸等
⑥其它:如NO、N2O4、Al2Cl6等
(2)由原子直接构成的物质(原子晶体):稀有气体、金刚石、晶体硅、二氧化硅、碳化硅、石墨(混合型晶体)等;
(3)由阴阳离子构成的物质(离子晶体):绝大多数盐、强碱、低价金属氧化物。
(4)由阳离子和自由电子构成的物质(金属晶体):金属单质、合金
考点二 物理变化和化学变化
1.离子与基团:
3.核素--具有一定数目的质子和一定数目的中子的一种原子
同位素--具有相同质子数和不同中子数的原子互称为同位素
同素异形体--同种元素形成的结构不同的单质
特别提醒:
|
|
离子 |
基团 |
|
定义 |
带电的原子或原子团 |
化学中对原子团和基的总称 |
|
区别 |
带有正电荷或负电荷 |
不带电,为缺电子物质,呈电中性 |
|
联系 |
两者通过得失电子可以互相转化 |
|
|
实例 |
OH- NO2- Cl- CH3+ |
-OH -NO2 -Cl -CH3 |
2.分子、原子、离子--微观概念,说明物质的微观构成。
(1)分子是保持物质化学性质的一种微粒。(单原子分子、双原子分子、多原子分子)
(2)原子是化学变化中的最小微粒。(不是构成物质的最小微粒)
(3)离子是带电的原子或原子团。(基:中性原子团)
1.元素--宏观概念,说明物质的宏观组成。
元素是质子数相同的一类原子的统称。质子数相同的微粒不一定是同一种元素,因为微粒的含义要比原子广泛。
1.熟练掌握概念的涵义,力求准确、严密。
 化学概念是反映物质及其变化的本质特征的思维形式。化学基本概念是化学基础知识的基础,掌握了基本概念就可以从本质上掌握物质的性质、变化、内在联系及其规律。要掌握一个概念就必须得弄清楚它应用的对象、前提条件、表达方法和它与其他概念的联系和区别。如气体摩尔体积,它应用的对象是气体,它对固体、液体就不适用;前提条件是标准状况。
2.在分析、理解概念的内涵时,还必须注意:
(1)要切实弄懂概念中的一些字和词的含义。例如电解质的定义:电解质是指在水溶液中或熔融状态下能够导电的化合物。“或”字意味着水溶液中、熔融状态下这两个条件只需具备其中之一就行了;“能够导电”是指该物质本身能够导电,而不是它发生反应后的生成物;“化合物”就指明了该物质不能是单质,更不能是混合物。
化学概念是反映物质及其变化的本质特征的思维形式。化学基本概念是化学基础知识的基础,掌握了基本概念就可以从本质上掌握物质的性质、变化、内在联系及其规律。要掌握一个概念就必须得弄清楚它应用的对象、前提条件、表达方法和它与其他概念的联系和区别。如气体摩尔体积,它应用的对象是气体,它对固体、液体就不适用;前提条件是标准状况。
2.在分析、理解概念的内涵时,还必须注意:
(1)要切实弄懂概念中的一些字和词的含义。例如电解质的定义:电解质是指在水溶液中或熔融状态下能够导电的化合物。“或”字意味着水溶液中、熔融状态下这两个条件只需具备其中之一就行了;“能够导电”是指该物质本身能够导电,而不是它发生反应后的生成物;“化合物”就指明了该物质不能是单质,更不能是混合物。
(2)要重视数量词在概念中的作用。有些概念如果忽略了数量词,就会失去原来的含义,它的内涵就变了。如"一个"、"几个"、"一种"、"全部"、"任何"、"多种"、"一部分"、"少数"、"多数"等等。 (3)不可忽视概念中的注释语。化学概念中的注语的形式是加括号,如具有相同的核电荷数(即质子数)的同一类原子总称为元素;两种或两种以上的金属(或金属跟非金属)融合而成的具有金属特性的物质,叫做合金。 (4)不仅要搞清概念的内涵,还必须搞清概念的外延,即了解概念的引申、联系和发展。 3.要注意分析概念之间的联系和区别。 例如质量百分比浓度(质量百分比浓度)、物质的量浓度都是表示溶液浓度的概念,这二种浓度中溶质、溶剂、溶液浓度三个之间的关系是相同的,这是二种浓度概念的共同点,但从二者具体表示方法来分析,他们又是不同的。溶质的质量分数(质量百分比浓度)和物质的量浓度可以进行相互间换算,反映了概念之间的联系。通过这样的比较分析及适当的计算练习,对这一组概念就会有比较明确的了解和有可能达到灵活地运用。有些容易混淆的概念,也可以通过对比搞清他们的区别和联系,从而达到加深和巩固的目的。
第1讲 物质的组成、性质和分类
★考情直播
考纲解读
|
考纲内容 |
能力要求 |
考向定位 |
|
了解分子、原子、离子等概念的含义。了解原子团的定义。 |
了解分子、原子、离子、元素、核素等概念的涵义;能区别原子、离子和基团。 |
理解物质的微粒组成(特别是同位素)、熟悉物质的分类形式、正确判断纯净物和混合物、物理变化和化学变化是历年高考的常见考点。高考试题中,本讲知识可以说是年年考,年年有新意。运用对比、归纳的方法辨析概念,利用分类原理将知识点连成线、织成网,形成网络;在运用中准确、严密掌握各概念的涵义是复习本讲的关键。 |
|
理解物理变化与化学变化的区别与联系。 |
能正确判断物理变化和化学变化,理解化学变化的本质。 |
|
|
理解混合物和纯净物、单质和化合物、金属和非金属的概念。 |
能区分混合物和纯净物、单质和化合物、金属和非金属;理解同位素的概念,能区分同位素、同素异形体、同系物、同分异构体。 |
|
|
理解酸、碱、盐、氧化物的概念及相互联系。 |
理解无机物和有机物、酸、碱、盐、氧化物的概念及相互联系。 |
考点整合
考点1 物质的组成
5.溶液与胶体
(1)了解溶液的含义。
(2)了解溶解度、饱和溶液的概念。
(3)了解溶液的组成。理解溶液中溶质的质量分数的概念,并能进行有关计算。
(4)了解配制一定溶质质量分数、物质的量浓度溶液的方法。
(5)了解胶体是一种常见的分散系。
知识网络

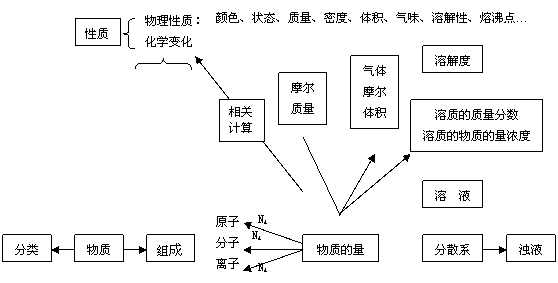
 |
|||
|
学法指导
4.离子反应和离子方程式
(1)了解离子反应的概念、离子反应发生的条件。了解常见离子的检验方法。
(2)能正确书写化学方程式和离子方程式,并能进行有关计算。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com