
1.分子式:用元素符号表示物质分子组成的式子。如乙酸的分子式为C2H4O2 , 过氧化氢的分子式为H2O2。(最简式)n = 分子式 。
3.原子结构示意图(以Cl为例):
|
|||
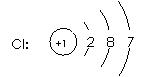 |
|||
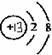
[例1](2008·杭州三模)右图是某粒子的结构示意图,下列说法不正确的是( )
 A.该元素原子的原子核外有2个电子层
A.该元素原子的原子核外有2个电子层
B.该粒子是阳离子
C.该元素是一种金属元素
D.该粒子具有稳定的结构
[解析]由所给的粒子的结构示意图知,该原子核内有13个质子,核外有10个电子,为铝离子,结构稳定。其原子的原子核外有3个电子层。
[答案] A
[方法技巧]
原子结构示意图和离子结构示意图的比较:以Cl和Cl-,Na和Na+为例
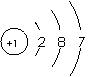
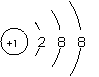
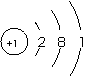
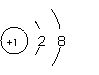
Cl Cl- Na Na+
考点二 表示物质结构的化学用语
2.离子符号:表示各种离子的符号。如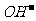 、
、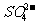 、
、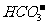 、
、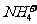 等等。
等等。
1.元素符号:人们确定了一套符号来表示各种元素,这种符号叫做元素符号。如C表示碳元素;Ca表示钙元素等等。元素符号不仅表示一种元素还可以表示这种元素的一个原子。
0.1 5V3 求出 V3==0.02L==20mL (沉淀完全溶解)
对应临界点的横坐标值为 60mL + 20mL + 20mL == l00mL
[答案](l) NH4+ Al3+ SO42-
(2)NH4 Al(SO4)2·12H2O [或(NH4)2SO4·A12 (SO4)3·24H2O]
(3)如图:
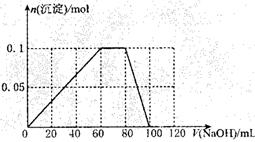
0.1 5V2 求出V2=0.02L=20mL
对应临界点的横坐标值为 60mL + 20mL = 80mL
根据Al(OH)3+ NaOH = NaAlO2 + 2H2O
1 l
0.1 5V1 求出V1=0.06L=60mL(沉淀达到最大值)
根据NH4+ + OH-=NH3·H2O
1 1
19.(2008·四川省高考调研考试) 某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为 45.3g 的该结晶水合物,分别制成溶液。向其中一份逐滴加人 NaOH 溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到 2.24L 该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加人 Ba (OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体 46.6g 。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是______和_________,阴离子是___________。
(2)试通过计算确定该结晶水合物的化学式。
(3)假设过程中向该溶液中加人的 NaOH 溶液的物质的量浓度为5mol·L一1,请在右图中画出生成沉淀的物质的量与加入 NaOH 溶液体积的关系示意图。
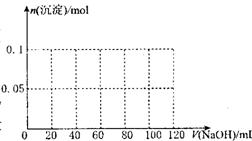
[解析](1)根据题意可以判断原物质中含有的离子是NH4+ Al3+ SO42-
(2)n (SO42-)==0.2mol n (NH4+)== ==0.1mol
根据离子化合物中阴、阳离子电荷守恒的原理:n (NH4+)+3n (Al3+)=2n (SO42-)可得:
n (Al3+)==(2×0.2mol-0.1mol)==0.1mol
n(H2O)=
=1.2mol
n (NH4+):n (Al3+):n (SO42-):n(H2O) = 0.1:0.1:0.2:1.2 = 1:1:2:12
该结晶水化物的化学式为:NH4 Al(SO4)2·12H2O [或(NH4)2SO4·A12 (SO4)3·24H2O]
(3)先分成三段进行计算,分别求出临界值,然后再作图像。
根据Al3+ + 3OH-=Al(OH)3↓
1 3
18.(2008·上海)在一定条件下,完全分解下列某化合物2g,产生氧气1.6g,此化合物是( )
A.1H216O B.2H216O C.1H218O D.2H218O
[解析]根据题意,2g化合物分解,产生氧气1.6g,因选项中都为水,由质量守恒定律知,产生的H2为0.4g,故答案为B。
[答案]B
17. (09年江苏化学·4)用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA
B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
答案:C
解析:A项,pH=13也就是意味着c(H+)=1×10-13mol·L-1,则c(OH-)=1×10-1mol·L-1,所以n(OH-)=n(OH-)×V=1×10-1mol·L-1×1L=0.1mol,所以N(OH-)=0.1NA;B项,发生的化学反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O(该反应为歧化反应),n(Cl2)=0.1mol,那么转移电子的数目应该为0.1NA;C项,乙烯和丁烯的最简式都是CH2,则n(CH2)=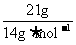 =1.5mol,所以n(C)=01.5mol,N(C)=1.5NA;D项,标准状况下,甲醇为液态,那么甲醇的物质的量就不是1mol,则所含有的氧原子个数也不为NA。
=1.5mol,所以n(C)=01.5mol,N(C)=1.5NA;D项,标准状况下,甲醇为液态,那么甲醇的物质的量就不是1mol,则所含有的氧原子个数也不为NA。
[考点分析]以阿伏伽德罗常数为载体考察如下知识点①考查22.4L/mol的正确使用;②考查在氧化还原反应中得失电子数的计算;③正确表示一定物质的量的某物质微粒所含某种微粒的个数;④考查在标准状况下一定体积的气体分子所含的分子数和原子数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com