
10.(2008·山东滨州一模)有两份溶液,其中所含溶质相同,设其摩尔质量为Mg/mol。根据下表信息,回答有关问题:
|
|
溶质的质量分数 |
溶液的密度(g·cm-3) |
|
第一份溶液 |
ω1 |
ρ1 |
|
第二份溶液 |
ω2 |
ρ2 |
(1)第一份溶液中,溶质的物质的量浓度为 。
(2)取等质量两份溶液混合,则所得混合液中溶质的质量分数ω3= 。
(3)若有ω1>ω2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为ω4,试比较ω3、ω4的相对大小? 。
[答案](1)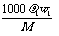 g/mol (2)
g/mol (2)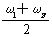
(3)①若ρ1>ρ2,ω4>ω3 ②若ρ1<ρ2,ω3>ω4
基础提升训练
9.(2006·全国)浓度均为0.1mol·L-1的三种溶液等体积混合,充分反应后没有沉淀的一组溶液是( )
A.BaCl2 NaOH NaHCO3 B.Na2CO3 MgCl2 H2SO4
C.AlCl3 NH3·H2O NaOH D.Ba(OH)2 CaCl2 Na2SO4
[解析]等体积混合后,A中刚好反应生成BaCO3沉淀;C中则有Al(OH)3 沉淀;D中有BaSO4沉淀。
[答案]B
8.(2007·鄂南高中)100mL 0.3mol·L-1Na2SO4溶液和50mL 0.2mol·L-1Al2(SO4)3溶液混合后,溶液中SO42-的物质的量浓度为( )
A.0.20mol·L-1 B.0.25mol·L-1 C.0.40mol·L-1 D.0.50mol·L-1
[解析]本题解题方法较多,通过元素守恒或电荷守恒法都很容易得出答案。
法一(SO42- 守恒):c(SO42-)=(0.3mol·L-1×0.1L+0.2mol·L-1×0.05L×3)/0.15L
= 0.40mol·L-1
法二(电荷守恒):根据c(Na+)×1+c(Al3+)×3=c(SO42-)×2,有:
100ml×0.3mol·L-1/(100mL+50mL)×1+50ml×0.2mol·L-1/(100mL+50mL)×3=c(SO42-)×2
解得:c(SO42*)= 0.40mol·L-1。
[答案]C
7.(2008·北大附中)将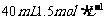 的
的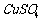 溶液与30mL 3mol/L的NaOH溶液混合,生成蓝色沉淀,假如溶液中
溶液与30mL 3mol/L的NaOH溶液混合,生成蓝色沉淀,假如溶液中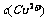 和
和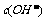 都已变得很小,可忽略,则生成沉淀的组成可表示为( )
都已变得很小,可忽略,则生成沉淀的组成可表示为( )
A.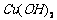 B.
B.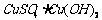
C.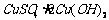 D.
D.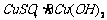
[解析]依据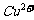 、
、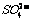 、
、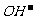 守恒即可解得。
守恒即可解得。
[答案]D
6.(2008·广州七区联考)实验室里需用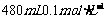 的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是( )
的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是( )
A.称取7.68g硫酸铜,加入500mL水 B.称取12.0g胆矾配成500mL溶液
C.称取8.0g硫酸铜,加入500mL水 D.称取12.5g胆矾配成500mL溶液
[解析]500ml容量瓶只能配制500mL溶液,所称取的硫酸铜或胆矾的质量应按配制500mL溶液的所需量来计算。
[答案]D
5.(2008·揭阳一模)用NaOH固体配制1.0 mol·L-1的NaOH溶液220mL,下列说法正确的是( )
A.首先称取NaOH固体8.8g
B.定容时仰视刻度线会使所配制的溶液浓度偏高
C.定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线
D.容量瓶中原有少量蒸馏水没有影响。
[解析]依题意,配制1.0 mol·L-1的NaOH溶液220mL要用250mL容量瓶来配制,经计算知,需要NaOH固体10.0g,故A不正确;定容时仰视刻度线或定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,又加少量水至刻度线,都会使所配制的溶液浓度偏低,故B、C都不正确。
[答案]D
4.(2003·广东)等体积硫酸铝、硫酸锌、硫酸钠溶液分别与足量的氯化钡溶液反应。若生成的硫酸钡沉淀的质量比为1︰2︰3,则三种硫酸盐溶液的物质的量浓度比为( )
A.1︰2︰3 B.1︰6︰9 C.1︰3︰3 D.1︰3︰6
[解析]据题意生成BaSO4的质量比为1∶2∶3,可推知A12(SO4)3、ZnSO4、NaaSO4三种溶液中所含SO42-的物质的量之比为1∶2∶3。设A12(SO4)3、ZnSO4、Na2SO4的物质的量浓度为c1、c2、c3,则3clV∶c2V∶c3V=1∶2∶3,解得c1∶c2∶c3=1∶6∶9
[答案]B
3.(2006·全国)某氯化镁溶液的密度为1.18g•cm-1 ,其中镁离子的质量分数为5.1%。300mL该溶液中Cl-离子的物质的量约等于( )
A. 0.37mol B. 0.63mol C. 0.74mol D. 1.5mol
[解析]已知Mg2+的量,求n(C1-),由氯化镁(MgCl2)的组成可知∶
n(C1-)=2n(Mg2+)=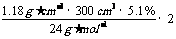 =1.5
mol
=1.5
mol
[答案]D
2.(2005·全国)相同质量的CuO和MgO粉末分别溶于相同体积的硝酸中,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为a mol·L-1和b mol·L-1。则a与b的关系为 ( )
A.a=b B.a=2b C.2a=b D.a=5b
[解析]n(CuO)∶n(MgO)=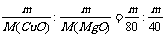 ==1∶2,体积相同时物质的量比等于物质的量浓度比,所以
==1∶2,体积相同时物质的量比等于物质的量浓度比,所以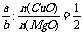 ,从而推出2a=b,故选C。
,从而推出2a=b,故选C。
[答案]C
1.(2009·广州七区联考)下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是 ( )
A.100mL 0.5mol/L MgCl2溶液 B.25ml 0.5mol/L HCl溶液
C.50ml 1mol/L NaCl溶液 D.50mL 0.5mol/L CaCl2溶液
[解析]Cl-的物质的量浓度与所给的溶液的体积无关,只与其相应的化学组成有关。故A、C、D中Cl-的物质的量浓度都为1mol/L,B中Cl-的物质的量浓度都为0.5mol/L。
[答案]B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com