
14.(2005ЁЄНЫе)ЕЊЛЏТС(AlN)ОпгаФЭИпЮТЁЂПЙГхЛїЁЂЕМШШадКУЕШгХСМаджЪЃЌБЛЙуЗКгІгУгкЕчзгЙЄвЕЁЂЬеДЩЙЄвЕЕШСьгђЁЃдквЛЖЈЬѕМўЯТЃЌЕЊЛЏТСПЩЭЈЙ§ШчЯТЗДгІКЯГЩЃКAl2O3+N2+3C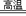 2AlN+3COЃЌЯТСаа№Ъіе§ШЗЕФЪЧ (ЁЁЁЁ )
2AlN+3COЃЌЯТСаа№Ъіе§ШЗЕФЪЧ (ЁЁЁЁ )
A.дкЕЊЛЏТСЕФКЯГЩЗДгІжаЃЌN2ЪЧЛЙдМСЃЌAl2O3ЪЧбѕЛЏМС
B.ЩЯЪіЗДгІжаУПЩњГЩ2mol AlNЃЌN2ЕУЕН3molЕчзг
C.ЕЊЛЏТСжаЕЊдЊЫиЕФЛЏКЯМлЮЊ-3Мл
D.ЕЊЛЏТСОЇЬхЪєгкЗжзгОЇЬх
[НтЮі]AжадкN2ЪЧбѕЛЏМСЃЌAl2O3УЛгаВЮМгбѕЛЏЛЙдЗДгІЃЛBжаУПЩњГЩ2mol AlNЃЌN2ЕУЕН6molЕчзгЃЛDжаЕЊЛЏТСОЇЬхЪєгкдзгОЇЬхЁЃ
[Д№АИ]C
13.(2008ЁЄНЮїН№ЬЋбєЕк6ДЮШЋЙњДѓСЊПМ)ФГЙЄГЇЕФЫсадЗЯЫЎжаКЌгаОчЖОЕФ ПЩМгШы
ПЩМгШы Г§ШЅ
Г§ШЅ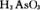 ВЂЛиЪеAsЃЌЗДгІЕФРызгЗНГЬЪНЮЊЃК
ВЂЛиЪеAsЃЌЗДгІЕФРызгЗНГЬЪНЮЊЃК ЃЌЯТСаЙигкИУЗДгІЕФЫЕЗЈжае§ШЗЕФЪЧ(ЁЁЁЁ )
ЃЌЯТСаЙигкИУЗДгІЕФЫЕЗЈжае§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎЛЙдМСЪЧ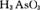 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
BЃЎЛЙдадЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
BЃЎЛЙдадЃК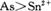
CЃЎMЮЊOH-ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎУПЩњГЩ7.5 g AsЃЌЛЙдМСЪЇШЅЕФЕчзгЮЊ0.3 mol
[НтЮі]ИљОнЮяжЪЫљКЌдЊЫиЕФЛЏКЯМлБфЛЏПЩжЊЃЌдкЗДгІжаЛЙдМСЮЊSn2+ЃЌ 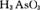 ЪЧбѕЛЏМСЃЌЛЙдадЃКSn2+ЃОAsЃЌЙЪAЁЂBВЛе§ШЗЃЛгЩжЪСПЪиКуЖЈТЩПЩжЊMЮЊH2OЃЌЙЪCВЛе§ШЗЁЃ
ЪЧбѕЛЏМСЃЌЛЙдадЃКSn2+ЃОAsЃЌЙЪAЁЂBВЛе§ШЗЃЛгЩжЪСПЪиКуЖЈТЩПЩжЊMЮЊH2OЃЌЙЪCВЛе§ШЗЁЃ
[Д№АИ]D
12.(2007ЁЄЙуЖЋ)ТШЦјЪЧвЛжжживЊЕФЙЄвЕдСЯЁЃЙЄвЕЩЯРћгУЗДгІдк3Cl2+2NH3ЃНN2+6HClМьВщТШЦјЙмЕРЪЧЗёТЉЦјЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧ(ЁЁ )
A.ШєЙмЕРТЉЦјгіАБОЭЛсВњЩњАзбЬЁЁЁЁЁЁЁЁЁЁ B.ИУЗДгІРћгУСЫCl2ЕФЧПбѕЛЏад
C.ИУЗДгІЪєгкИДЗжНтЗДгІЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.ЩњГЩ1molN2га6molЕчзгзЊвЦ
[НтЮі]гЩЗНГЬЪНжЊЃКШчNH3Й§СПдђЛсгыВњЮяHClЗДгІЩњГЩNH4ClЃЌЙЪAе§ШЗЃЛ ClЕФЛЏКЯМлгЩ0Ёњ -1ЃЌЙЪBЖдЃЛNгЩ-3 Ёњ 0ЃЌЪЇШЅЕФЕчзгзмЪ§ЮЊ2ЁС3 = 6ЃЌЙЪDе§ШЗЁЃ
[Д№АИ]C
11.ЯТСаИїзщЮяжЪжаЃЌУПжжЮяжЪЖММШФмБЛбѕЛЏгжФмБЛЛЙдЕФЪЧ(ЁЁ )
A.FeCl2ЁЂCl2ЁЂCuSO4ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.H3PO4ЁЂHNO2ЁЂH2SO4
C.H2SЁЂHClЁЂH2SO3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.Na2SЁЂNaClOЁЂNH4HCO3
[НтЮі]дЊЫиЕФЛЏКЯМлДІгкжаМфМлЬЌОЭМШФмБЛбѕЛЏгжФмБЛЛЙдЁЃ
[Д№АИ]C
10.(2007ЁЄНЫе)Ш§ОлЧшЫс[C3N3(OH)3]ПЩгУгкЯћГ§ЦћГЕЮВЦјжаЕФNO2ЁЃЦфЗДгІдРэЮЊЃК
ЁЁЁЁЁЁ C3N3(OH)3
 ЁЁ3HNCOЃЛЁЁЁЁ
8HNCO+6NO2
ЁЁ3HNCOЃЛЁЁЁЁ
8HNCO+6NO2  ЁЁ7N2+8CO2+4H2O
ЁЁ7N2+8CO2+4H2O
ЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
ЁЁA.C3N3(OH)3гыHNCOЮЊЭЌвЛЮяжЪЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁB.HNCOЪЧвЛжжКмЧПЕФбѕЛЏМС
ЁЁC.1 molNO2дкЗДгІжазЊвЦЕФЕчзгЮЊ4molЁЁЁЁЁЁ D.ЗДгІжаNO2ЪЧЛЙдМС
[НтЮі] C3N3(OH)3
 ЁЁ3HNCOЮЊЛЏбЇБфЛЏЃЌОЙ§ЗДгІЩњГЩСЫВЛЭЌЕФЮяжЪЃЌЙЪAВЛе§ШЗЃЛ8HNCO+6NO2
ЁЁ3HNCOЮЊЛЏбЇБфЛЏЃЌОЙ§ЗДгІЩњГЩСЫВЛЭЌЕФЮяжЪЃЌЙЪAВЛе§ШЗЃЛ8HNCO+6NO2
 ЁЁ7N2+8CO2+4H2OжаHNCOзїЛЙдМСЃЌNO2зїбѕЛЏМСЃЌЙЪBЁЂDВЛе§ШЗЁЃ
ЁЁ7N2+8CO2+4H2OжаHNCOзїЛЙдМСЃЌNO2зїбѕЛЏМСЃЌЙЪBЁЂDВЛе§ШЗЁЃ
[Д№АИ]C
ЛљДЁЬсЩ§бЕСЗ
9.ЭљXШмвКжаЭЈШыЙ§СПЕФCl2ЃЌдйЕЮМгBa(NO3)2КЭЯЁHNO3ШмвКЃЌШмвКжаЮіГіАзЩЋГСЕэЃЌXбЮПЩФмЪЧ(ЁЁЁЁ )
A.Na2SO3ЁЁЁЁЁЁЁЁЁЁЁЁ B.CaCl2ЁЁ ЁЁЁЁЁЁЁЁЁЁC.AgNO3ЁЁЁЁЁЁЁЁ D.Na2CO3
[НтЮі]гЩЬтвтжЊЃЌАзЩЋГСЕэгІЮЊAgClЛђBaSO4,ЙЪД№АИЮЊACЁЃбЁAЪЧвђЮЊNa2SO3БЛCl2бѕЛЏГЩСЫNa2SO4ЁЁЁЁ
[Д№АИ]AC
8.вЛЖЈЬѕМўЯТЯѕЫсяЇЪмШШЗжНтЕФЛЏбЇЗНГЬЪНЮЊЃК5NH4NO3ЃН2HNO3+4N2+9H2OЃЌдкЗДгІжаБЛбѕЛЏгыБЛЛЙдЕФЕЊдзгЪ§жЎБШЮЊ(ЁЁЁЁ )
A.5ЁУ3ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.5ЁУ4ЁЁЁЁЁЁЁЁЁЁЁЁ C.1ЁУ1ЁЁЁЁЁЁЁЁЁЁ D.3ЁУ5
[НтЮі]ЛЏбЇЗНГЬЪН5NH4NO3ЃН2HNO3+4N2+9H2OжаЃЌ8ИіNдзг(4N2)га5ИіРДздNH4NO3ЕФNH4+ЃЌга3ИіРДздNH4NO3ЕФNO3-ЃЌвВМДБЛбѕЛЏЕФЕЊЮЊ5ИіЃЌБЛЛЙдЕФЕЊЮЊ3Иі
[Д№АИ]A
7.ЮќНјШЫЬхФкЕФO2га2%зЊЛЏЮЊбѕЛЏадМЋЧПЕФЛюадбѕИБВњЮяЃЌШч 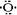 ЁЁЕШЃЌетаЉЛюадбѕФмМгЫйШЫЬхЫЅРЯЃЌБЛГЦЮЊЁАЖсУќЩБЪжЁБЁЃЮвЙњПЦбЇМвГЂЪдгУКЌЮјЛЏКЯЮяNa2SeO3ЯћГ§ШЫЬхФкЕФЛюадбѕЃЌдкЯћГ§ЛюадбѕЪБЃЌNa2SeO3ЕФзїгУЪЧ(ЁЁЁЁ )
ЁЁЕШЃЌетаЉЛюадбѕФмМгЫйШЫЬхЫЅРЯЃЌБЛГЦЮЊЁАЖсУќЩБЪжЁБЁЃЮвЙњПЦбЇМвГЂЪдгУКЌЮјЛЏКЯЮяNa2SeO3ЯћГ§ШЫЬхФкЕФЛюадбѕЃЌдкЯћГ§ЛюадбѕЪБЃЌNa2SeO3ЕФзїгУЪЧ(ЁЁЁЁ )
A.бѕЛЏМСЁЁЁЁЁЁ B.ЛЙдМСЁЁЁЁЁЁЁЁ C.МШЪЧбѕЛЏМСгжЪЧЛЙдМСЁЁЁЁЁЁ D.вдЩЯОљВЛЪЧ
[НтЮі]гЩЬтвтжЊЃЌЛюадбѕгаЧПбѕЛЏадЃЌЙЪЯћГ§ЛюадбѕгІМгШыЛЙдМСЁЃ
[Д№АИ]B
6.ФГШмвКжагаFe2+ЁЂCl-КЭI-ЙВДцЃЌвЊбѕЛЏГ§ШЅI-ЖјВЛгАЯьFe2+КЭCl-ЃЌПЩМгШыЕФЪдМСЪЧ(ЁЁ )
A.Cl2ЁЁЁЁЁЁЁЁЁЁЁЁ B.KMnO4ЁЁЁЁЁЁЁЁЁЁ C.FeCl3ЁЁЁЁЁЁЁЁЁЁ D.HCl
[НтЮі]ЗжЮіИїбЁЯюжЊЃЌDжаHClЮобѕЛЏадЃЛAжаЕФCl2КЭBжаKMnO4ФмбѕЛЏFe2+КЭI-ЁЃ
[Д№АИ]C
5.ЧтЛЏИЦПЩвдзїЮЊЩњЧтМС(CaH2жаЧтдЊЫиЮЊ-1Мл)ЃЌЗДгІЗНГЬЪНЮЊЃКCaH2+2H2O=Ca(OH)2+2H2ЁќЃЌЦфжаЫЎЕФзїгУЪЧ(ЁЁ )
A.МШВЛЪЧбѕЛЏМСвВВЛЪЧЛЙдМСЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.ЪЧбѕЛЏМС
C.ЪЧЛЙдМСЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁD.МШЪЧбѕЛЏМСгжЪЧЛЙдМС
[НтЮі]ИУЗДгІЕФБОжЪЪЧCaH2жаЕФH-КЭH2OЕчРыГіРДЕФH+НсКЯЩњГЩH2ЃЌЙЪЗДгІжаЫЎзїбѕЛЏМСЁЃ
[Д№АИ]B
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com