
6.现代化的社会为我们的出行提供了形形色色的交通工具,下列属于绿色交通工具的是
①火车 ②自行车 ③摩托车 ④汽车 ⑤人力帆船 ⑥雪橇 ⑦电动车 ⑧飞机
A.③⑥⑦ B.②⑤⑥ C.①④⑧ D.②③⑦
5.“儿行千里母担忧”,出门在外可能会遇到一些偶发事件,这时你可以很方便地打免费电话寻求帮助,下列电话与特殊车辆对应正确的是
A.110-警车;119-消防车;122-救护车
B.110-警车;119-消防车;120-救护车
C.114-警车;110-消防车;120-救护车
D.119-警车;911-消防车;122-救护车
4.框架结构中一个构件断裂,断点的两端分开,据此判断,这个构件所受的力是
A.拉力 B.剪切力 C.扭转力 D.压力
3.木工工艺中,不会用到的连接方式是
A.铆接 B.榫接 C.胶接 D.钉接
2.当前,对物质的研究和应用已延伸到分子或原子的微观领域,纳米技术就是微观领域的研究成果之一。1纳米=10-9米,即十亿分之一米。物质在纳米尺度有许多特殊的性质,所以纳米材料是一种新材料,纳米技术是21世纪科学技术的发展方向。纳米是
A.长度单位 B.新材料 C.新技术 D.水稻技术
1.卫生间的抽水水箱,当放水冲刷时,水箱水位下降,浮球也随之下沉,这时与浮球以杠杆相连接的活塞式进水阀门打开,开始注水。水位升高,浮球上升,进水阀门逐渐关小,浮球升到一定位置,进水停止。这种控制系统是
A.闭环控制系统 B.开环控制系统 B.浮球控制系统 D.活塞控制系统
21. (6分) Cu、Cu20和CuO组成的混合物,加入100mL0.6mol/LHNO3溶液恰好使混合物溶解,同时收集到224mLNO气体(标准状况)。求:
(1)产物中硝酸铜的物质的量。
(2)如混合物中含0.0lmoLCu,则其中Cu20、CuO的物质的量分别为多少?
(3)如混合物中Cu的物质的量为X,求其中Cu20、CuO的物质的量及X的取值范围。
山东省东营市胜利一中2010届高三上学期模块考试
20.(15分)某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验室按以下步骤进行:
①称量a g样品,置于烧杯中;
②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全;
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤,洗涤沉淀;
⑥将沉淀转移到坩埚内,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量;
⑦……
请根据上面叙述,回答:
(1)下图所示仪器中,本实验步骤①②③中必须用到的仪器是E和 (填字母)。

A B C D E F G
(2)写出步骤③中发生反应的离子方程式 。
(3)洗涤是洗去附着在沉淀上的 (写离子符号),洗涤沉淀的操作是 。
(4)第⑥步的操作中,将沉淀物加热,冷却至室温,称量其质量为m1g;再次加热并冷却室温称量其质量为m2g,且m1-m2=0.3,接下来的操作应当是 。
(5)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为
。(列出算式,不需化简)
(6)该兴趣小组中甲学生认为:实验步骤③中不加入氯水,其余步骤不变,仍可达到实验目的。你认为甲学生的观点是否正确? (填正确或错误);请说明理由:
。
19.(12分)已知X为中学化学中的一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的最高价氧化物是耐火材料,它的晶体硬度很大,常做手表的轴承;H为气体单质,D为无色气体,在空气中会出现红棕色。各物质的转化关系如下图(部分反应产物已略去)。
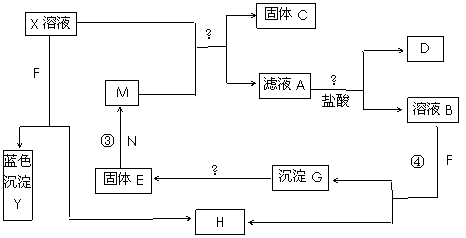
请回答下列问题:
(1)X的化学式为 。
(2)N在氧气中燃烧的实验现象是 。
(3)在反应①②③④中属于置换反应的是 (填序号)。
(4)反应②的离子方程式为 。
(5)X溶液与F反应的总化学方程式为 。
(6)若向100 mL 盐X的溶液中加入10 g金属单质M的粉末,充分搅拌后,过滤,烘干得10.16g固体C。则滤液A中溶质的物质的量浓度为 。
18. (10分)373w.w.w.k.s.5.u.
c.o.m343近年来,我国酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(10分)373w.w.w.k.s.5.u.
c.o.m343近年来,我国酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
⑴有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,流程如下: ( I )将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液。(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。(III)将盐酸加入NaHSO3溶液中得SO2气体回收,生成的NaCl循环利用。
① 写出步骤(I)反应的化学方程式:
② 写出步骤(III)反应的离子方程式:
⑵还有学者提出利用 Fe 2十、Fe3十等离子的催化作用,常温下将SO2氧化成SO42一而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42一的转化率。
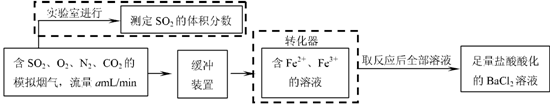 w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
① 该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是(填序号) 。
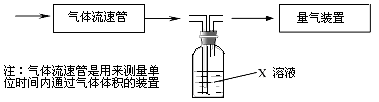
A.碘的淀粉溶液 B.酸性高锰酸钾溶液 C.氢氧化钠溶液 D.氯化钡溶液
② 若上述实验是在标准状况下进行的,X是已知体积和物质的量浓度的溶液,欲测定转化器中SO2氧化成SO42一的转化率,已知气体流速,还需测定的数据是
(3)新型氨法烟气脱硫技术采用氨吸收烟气中SO2生成亚硫酸铵和亚硫酸氢铵,再用一定量的磷酸进行反应,在反应回收SO2后的混合物中通入适量的氨气得到一种产品。该技术的优点是 。
(4)为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2。该方法涉及到的化学反应为:SO2+2CO=2CO2+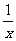 Sx 、
Sx 、
CO+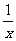 Sx=COS、2COS+SO2=2CO2+
Sx=COS、2COS+SO2=2CO2+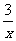 Sx 。其中COS中“C”化合价为
。
Sx 。其中COS中“C”化合价为
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com