
13.短周期元素A、B、C、D的原子序数依次增大,它们的原子序数之和为36,且原子最外层电子数之和为14;A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素。下列叙述正确的是
A.在地壳中,C元素的含量位于第一位
B.A、B、D三种元素形成的化合物一定是强酸
C.C元素位于元素周期表中的第3周期第ⅠA族
D.B元素与氢元素形成化合物的化学式一定为H2B
12. 常温下,向20 mL x mol·L-1 CH3COOH溶液中逐滴加入等物质的量浓度的NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如
常温下,向20 mL x mol·L-1 CH3COOH溶液中逐滴加入等物质的量浓度的NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如
右图所示(忽略温度变化)。下列说法中正确的是
A.上述 CH3COOH溶液中:c(H+)=1×10-3 mol·L-1
B.图中V1 >20 mL
C.a点对应的溶液中:c (CH3COO-)=c (Na+)
D.当加入Na OH溶液的体积为20 mL时,
溶液中:c (CH3COOH) + c (H+)>c (OH-)
11.右图是某研究小组进行化学能与电能相互转化的实验装置图。
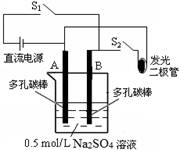 下列说法正确的是
下列说法正确的是
A.该装置中只存在2种形式的能量转化
B.只闭合S1时,A电极发生还原反应
C.闭合S1一段时间后断开,闭合S2,
A电极的反应式为:2H+ + 2e- = H2↑
D.闭合S1一段时间后断开,闭合S2,
溶液的pH升高
10.下列实验操作与预期实验目的或所得实验结论一致的是
|
选项 |
实验操作 |
实验目的或结论 |
|
A |
将某气体通入品红溶液中,溶液不褪色 |
该气体中无SO2 |
|
B |
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 |
研究浓度对反应速率的影响 |
|
C |
下层液体从分液漏斗下端管口放出后,关闭活塞,换一个接收容器,再将上层液体从下端管口放出 |
取出分液漏斗中的上层液体 |
|
D |
向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色 |
说明该溶液中一定含有Fe2+ |
9.下列有关用水杨酸和乙酸酐制备阿司匹林(乙酰水杨酸)的说法中不正确的是
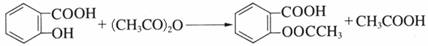
A.阿司匹林分子中有1个手性碳原子
B.水杨酸和阿司匹林都属于芳香族化合物
C.可用FeCl3溶液检验阿司匹林中是否含有未反应完的水杨酸
D.1 mol阿司匹林最多可与2 mol的NaOH溶液反应
8.下列叙述正确的是
A.电化学反应不一定是氧化还原反应
B.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同
C.2NO+2CO 2CO2+N2 的△H<0,则该反应一定能自发进行
2CO2+N2 的△H<0,则该反应一定能自发进行
D.用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3
7.下列装置或操作合理的是

① ② ③ ④
A.装置①可用于比较碳酸、苯酚酸性的强弱
B.装置②可用来进行浓硫酸的稀释
C.装置③可用于从食盐水中提取氯化钠
D.装置④可用于证明溴乙烷与NaOH乙醇溶液共热生成乙烯
不定项选择题:本题包括7小题,每小题4分,共计28分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
6.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.能使甲基橙变黄的溶液中:Na+、K+、SO42-、AlO2-
B.加铝粉放出大量H2的溶液中:Na+、NH4+、SO42-、CO32-
C.c(OH-) /c(H+)=10-12的溶液中:NH4+、Cu2+、NO3-、Cl-
D.0.1 mol·L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl-
5.设NA表示阿伏加德罗常数的值。下列说法正确的是
A.1.5 g CH3+含有的电子数为NA
B.电解精炼铜转移NA个电子时,阴极析出32 g铜
C.1 L 0.1 mol·L-1 氨水溶液中所含的离子和分子总数为0.1NA
D.标准状况下,11.2 L四氯化碳中含有的C-Cl 键的个数为2NA
4.下列有关物质的性质或应用正确的是
A.溴化银可用作感光材料和人工降雨
B.煤的干馏可以得到苯、甲苯和二甲苯
C.石油裂解和油脂皂化都是高分子转化为小分子的过程
D.误食氯化钡,应尽快用硫酸铜溶液给患者洗胃
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com