
16、今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+ 、Mg2+、Ba2+、Cl-、CO32 -、SO42 -,现取三份100 mL溶液进行如下实验: 
 (1)第一份加入AgNO3溶液有沉淀产生
(1)第一份加入AgNO3溶液有沉淀产生 
(2)第二份加足量NaOH溶液加热后,收集到气体0.07 mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是
A.100 mL溶液中含0.01 mol CO32 -
B.K+一定存在 
C.Ba2+一定不存在,Mg2+可能存在 D.Cl-一定存在 
15、将50g质量分数为ω1,物质的量浓度为C1的浓硫酸沿玻璃棒加入到VmL水中,稀释后得到质量分数为ω2,物质的量浓度为C2的稀溶液。下列说法中正确的是 
A.若C1=2C2,则ω1<2ω2,V<50mL B.若C1=2C2,则ω1<2ω2,V>50mL
C.若ω1=2ω2,则C1<2C2,V=50mL D.若ω1=2ω2,则C1>2C2,V<50Ml
14、下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)正确的是
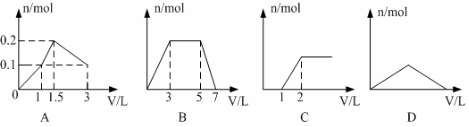

A.向1 L浓度均为0.1 mol/L 的Ba(OH)2、NaAl(OH)4混合液中加入0.1mol/L的稀H2SO4
(A图)
B.向1L含有0.1mol AlCl3和0.3mol NH4Cl的混合液中加入0.1 mol/L的NaOH溶液(B图)
C.向烧碱溶液中滴加明矾溶液(C图)
D.向KOH、Ca(OH)2的混合液中通入足量的CO2(D图)
13、在下列溶液中,各组离子可能大量共存的是
A.PH>7的溶液中:Na+、Cl-、SO42-、Fe3+
B.有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br-
C.由水电离的c(H+)=10-13 mol·L-1的溶液中:Al3+、K+、NO3-、SO42-
D.碳酸氢钠溶液中:K+、ClO-、Cl-、OH- 
11、下列离子方程式书写正确的是
A. 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:

3ClO-+2Fe(OH)3 =2 FeO42-+3Cl-+H2O+4H+
B.4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合
4AlO2-+7H++H2O=3Al(OH)3↓+Al3+
C.向NaAlO2 溶液中通入过量CO2 2AlO2-+CO2+3H2O = 2Al(OH)3↓+ CO32--
D. NaHSO4溶液中滴入Ba(OH)2溶液至中性:H++SO42-+Ba2+十OH-===BaSO4↓+H2O
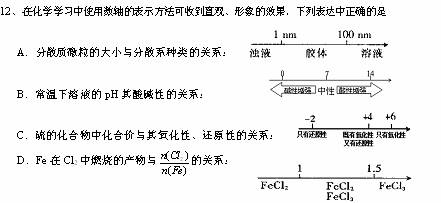
10. 下列说法正确的是
下列说法正确的是
 A. 实验室制备用盐酸制H2,可用排饱和碳酸氢钠溶液除氯化氢
A. 实验室制备用盐酸制H2,可用排饱和碳酸氢钠溶液除氯化氢
 B. 168O、188O为不同的核素,有不同的化学性质高
B. 168O、188O为不同的核素,有不同的化学性质高
 C. 漂白粉主要要成分是次氯酸钙
C. 漂白粉主要要成分是次氯酸钙
 D. Cl2具有很强的氧化性,但在化学反应中可能作还原剂
D. Cl2具有很强的氧化性,但在化学反应中可能作还原剂
9、某无色溶液中可能含有I-、Cu2+ 、SO32-、 NH4+ ,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-; ②肯定不含Cu2+ ③肯定含有SO32-; ④可能含有I-; 
⑤可能含有SO32-; 
A.①②③
B.②④⑤ C.①②⑤
D.②③④
8.实验是化学研究的基础,关于下列各装置图的叙述中,正确的是
A.装置①是一套实验室制气装置,用于发生、干燥和收集气体,如铜屑与稀硝酸
B.装置②中,a为正极,d为阳极 
C.装置③可用于收集H2、NH3、Cl2、HCl、NO2等
D.装置④能用于测量气体体积的装置
7、下列说法可以实现的是
①酸性氧化物在一定条件下均能与碱发生反应 
②弱酸与盐溶液反应可以生成强酸
③发生复分解反应,但产物既没有水生成,也没有沉淀和气体生成
④两种酸溶液充分反应后,所得溶液呈中性
⑤有单质参加的反应,但该反应不是氧化还原反应 
⑥两种氧化物发生反应有气体生成
A.①②③④⑤⑥
B.只有①②④⑤ 
C.只有③④⑤⑥
D.只有②④⑤

6、工业上以硫铁矿为原料制硫酸所产生的尾气中含有SO2,为便于监控,实施环境保护,下列适合测定硫酸尾气SO2含量的试剂是
A.品红溶液 B.碘水、淀粉溶液
C.氨水、酚酞试液 D.以上都能
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com