
1.一只雌鼠的一条染色体上某基因发生了突变,使野生型性状变为突变型性状。该雌鼠与野生型雄鼠杂交,F1的雌、雄中均既有野生型,又有突变型。若要通过一次杂交试验鉴别突变基因在X染色体还是在常染色体上,在F1中选择杂交的个体最好是
A.野生型(雄)×突变型(雌) B.野生型(雌)×突变型(雄)
C.野生型(雌)×野生型(雄) D.突变型(雌)×突变型(雄)
[命题意图] 考查常染色体遗传、X染色体隐性遗传的特点(分离定律的应用)及分析推理能力、归纳能力等。
[解析] 解答本题的步骤如下:
(1)分析推理突变型性状的显隐性。这是解题的切入点,否则,不可能正确推导出正确的答案。分析推理方法可运用假设--演绎法、反证法等。
具体分析过程:
假如显性基因用A表示,隐性基因用a表示。根据题干信息“该雌鼠与野生型雄鼠杂交,F1的雌、雄中均既有野生型,又有突变型”可知,该突变型雌鼠的基因型一定是杂合子(Aa)。可用反证法证明:即
若该突变型雌鼠为aa,则♀aa×♂AA→F1:Aa,即F1的雌、雄中均为野生型;或♀XaXa×♂XAY→F1:1/2 XAXa、1/2 XaY,即F1的雌鼠均为野生型、雄鼠均为突变型。这与题目所呈现的事实不符合,即假设不成立。
或者:
若该突变型雌鼠为AA,则♂AA×♀aa→F1:Aa,即F1的雌、雄中均只有突变型;或♀XAXA×♂XaY→F1:1/2 XAXa、1/2 XAY,即F1的雌、雄鼠均为突变型,这与题目所呈现的事实不符合,即假设不成立。
①.假设突变型性状为隐性,且突变基因位于常染色体上,则有:♀aa×♂AA→F1:Aa,即F1的雌、雄鼠中均只有野生型,这与题目所呈现的事实不符合,即假设不成立。
②.假设突变型性状为隐性,且突变基因位于X染色体上,则有:♀XaXa×♂XAY→F1:1/2 XAXa、1/2 XaY,即F1的雌鼠均为野生型、雄鼠均为突变型,这与题目所呈现的事实不符合,即假设不成立。
③.假设突变型性状为显性,且突变基因位于常染色体上,则有:♀Aa×♂aa→F1:1/2 Aa、1/2 aa,即F1的雌、雄中均既有野生型,又有突变型,这与题目所呈现的事实相符合,即假设成立。
④.假设突变型性状为显性,且突变基因位于X染色体上,则有:♀XAXa×♂XaY→F1:1/4 XAXa、1/4 XaXa 、1/4 XAY、1/4 XaY,即F1的雌、雄中均既有野生型,又有突变型,这与题目所呈现的事实相符合,即假设成立。
结论:突变型性状为显性,该突变型雌鼠的基因型是杂合子。
(2)确定用于杂交的对象(在F1中选择)。题目中的信息“在F1中选择杂交的个体最好是”已表明可能存在不同的杂交组合方式,需要从中选择出最简便的方法,这就需要进行逐一分析,最终确定哪种组合最佳。
①A选项:假如F1:♂aa×♀Aa→F2:1/2 Aa、1/2 aa,即F2的雌、雄中均既有野生型,又有突变型;或F1:♂XaY×♀XAXa→F2:1/4 XAXA、1/4 XAXa 、1/4 XAY、1/4 XaY,即F2的雌、雄中均既有野生型,又有突变型,这相当于重复了题目中所做的杂交实验,不能判断出突变基因是在X染色体还是在常染色体上。故A选项不符合题意。
②B选项:若F1:♀aa×♂Aa→F2:1/2 Aa、1/2 aa,即F2的雌、雄中均既有野生型,又有突变型,则可推断突变基因位于常染色体上;若F1:♀XaXa×♂XAY→F2:1/2 XAXa、1/2 XaY,即F2的雌鼠均为野生型、雄鼠均为突变型,则可推断突变基因位于X染色体上。故B选项符合题意。
③C选项:F1:♀aa×♂aa→F2:aa,即F2的雌、雄鼠中均只有野生型;或♀XaXa×♂XaY→F1:1/2 XaXa、1/2 XaY,即F2的雌、雄鼠均为野生型,这无法判断突变基因的存在位置。故C选项不符合题意。
④D选项:若F1:♀Aa×♂Aa→F2:3/4 A_、1/4 aa,即F2的雌、雄中均既有野生型,又有突变型,则可推断突变基因位于常染色体上;或F1:♀XAXa×♂XAY→F2:1/4 XAXA、1/4 XAXa、1/4 XAY、1/4 XaY,即F2的雌鼠均为突变型、雄鼠中既有野生型,又有突变型,则可推断突变基因位于X染色体上。故D选项符合题意。
归纳:在符合题意的B、D选项中,显然若出现“F2的雌鼠均为野生型,即与F1的雄鼠表现型相同,而雄鼠均为突变型,即与F1的雌鼠表现型相同,则可推断突变基因位于X染色体上”的现象,更容易被人所识别,应该属于最佳交配方式。
[答案] B
[点拨] ①解答本题需要具备一个基本的前期:即在一个自由交配的动物种群中,若只有一种性状表现(即只有一种表现型),则该种群的所有个体均为纯合子。
可用反证法证明:假设种群中存在杂合子,则在随机交配的情况下,可能出现杂交组合Aa×Aa→A_、aa,即F1的雌、雄中均既有野生型,又有突变型;或♀XAXa×♂XAY→1/4 XAXA、1/4 XAXa、1/4 XAY、1/4 XaY,子代雌鼠均为突变型、雄鼠中既有野生型,又有突变型。两种情况下,均可能出现隐性性状,显然不符合题意。
②性状的遗传与性别相关联的遗传现象属于伴性遗传,而性状的遗传与性别无关的遗传现象属于常染色体遗传。
[例2] 某种鼠中,黄鼠基因A对灰鼠基因a为显性,短尾基因B对长尾基因b为显性,且基因A或b在纯合时使胚胎致死,这两对基因是独立遗传的。现有两只双杂合的黄色短尾鼠交配,理论上所生的子代表现型比例为
A.2:1 B.9:3:3:1 C.4:2:2:1 D.1:1:1:1
[命题意图] 考查基因的自由组合定律及分析推理能力。
[解析] 可采用分解相乘的思想,即先单独分析,再按照乘法定律综合考虑。单独分析:杂合的黄色鼠交配,基因型为AA的受精卵,因胚胎致死而不能存活,结果子代鼠中,黄鼠(Aa)与灰鼠(aa)的比例为2:1;杂合的短尾鼠交配,基因型为bb的受精卵,因胚胎致死而不能存活,结果子代鼠中只有短尾鼠(BB、Bb)能够存活。综合考虑:子代鼠中黄色短尾鼠: 灰色短尾鼠= 2:1。
[答案] A


全 品中考网
化石燃料:从地下开采出的最主要的三种矿物燃料中,呈气态的燃料是______,主要成分的化学式为______;呈液态的燃料是______,主要含_____和______元素;呈固态的燃料是______,主要含有______元素。
 石油的炼制主要有分馏、裂化和裂解。
石油的炼制主要有分馏、裂化和裂解。
煤的综合利用煤的干馏、汽化和液化。
例49.下列变化是化学变化的是
A.石油蒸馏 B.煤干馏 C.干冰升华 D.煤燃烧
例50.环境污染已成为人类面临的重大威胁。下列名词与环境污染无关的是
①温室效应;②赤潮;③酸雨;④光化学污染;⑤臭氧空洞;⑥潮汐;⑦大脖子病;⑧富营养化。
A.②⑥ B.⑥⑦ C.①③⑤ D.④⑤⑧
2. 在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的足量试剂①是 Ca(OH)2 (填化学式)。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)
A.蒸馏 B.过滤 C.萃取 D.分液
(3)加入的足量试剂②是 HCl (填化学式)。
(4)写出由无水MgCl2制取金属镁的化学方程式 MgCl2(熔化) Mg+Cl2
Mg+Cl2
例48. 目前世界上60%的镁是从海水中提取的,下图是某工厂从海水中提取镁的主要步骤。学生就这个课题展开了讨论。
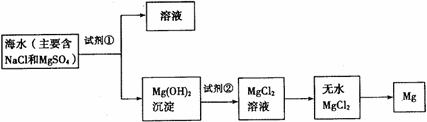
学生就这个课题提出了以下问题:
1. 在海水提镁的过程中如何实现对镁离子的富集 有三个学生提出自己的观点。
学生甲的观点:直接往海水中加入沉淀剂。
学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
通过分析比较你认为学生 丙 的观点正确(填学生序号),简述理由:
Mg2+离子浓度大,节约能源,便于过滤 。
金属活动顺序表中不同金属冶炼方法的选择
 K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
例47. 下列化学方程式,能用于工业上冶炼金属镁的是
A、2Na+MgCl2====2NaCl+Mg
B、MgCl2(熔化) Mg+Cl2
Mg+Cl2
C、2MgO 2Mg+O2
D、MgO+C
2Mg+O2
D、MgO+C MgO+C
MgO+C
24.火柴是人们常用的生活用品,某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下系列实验,并回答下列各题。
Ⅰ、火柴头中硫元素的实验证明
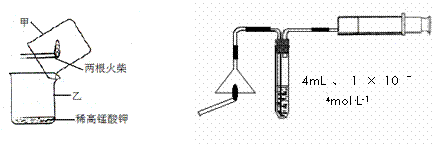
A B
⑴设计装置A中可观察到 的实验现象,即可证明火柴头上含有S元素。
⑵甲同学认为B装置中除了可选用稀高锰酸钾外还可选用:品红溶液、紫色石蕊溶液、滴有酚酞的NaOH溶液、溴水等,经大家分析后淘汰了紫色石蕊溶液和滴有酚酞的NaOH 溶液。你认为淘汰的原因可能是 。甲同学还认为在A装置中选用浓的高锰酸 钾酸性溶液更好,因为浓度越大反应速率越快,你认为对吗? (先判断再说明 原因)。
Ⅱ、火柴头中含有Cl元素的证明,设计了以下实验流程图:
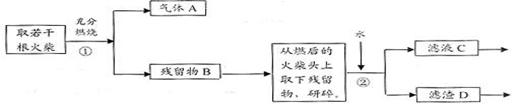 ⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是
。
⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是
。
⑵有学生提出检验火柴头上KClO3另一套实验方案:
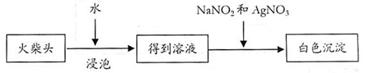
实验中发生的反应是 KClO3 + 3NaNO2 + AgNO3 = AgCl↓+ 3NaNO3 + KNO3,其中NaNO2 是 。剂,有人提出上述方法中出现白色沉淀并不能充分说明火柴头上 KClO3的存在,其理由是 。
Ⅲ、测定火柴头中KClO3的含量,设计了以下实验流程图:
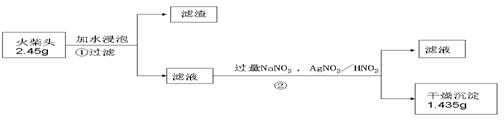
⑴步骤②的实验操作装置如下图所示,仪器a的名称为 ,装置B的作用是 。
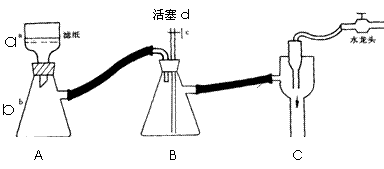 则当抽滤完毕或中途停止抽滤时,最佳的正确操作是
。
则当抽滤完毕或中途停止抽滤时,最佳的正确操作是
。
⑵得到的沉淀常用95%的酒精洗涤再抽滤,试问用酒精洗涤的原因 。(3)实验测 得火柴头中KClO3的质量分数为 ;未洗涤沉淀,测得KClO3的质量分数将 (填 “偏大”、“偏小”、或“无影响”,下同)。
23.某课外活动小组同学用下右图装置进行实验,试回答下列问题。
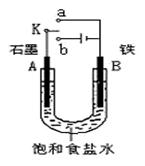 ⑴若开始时开关K与a连接,则B极的电极反应式为
⑴若开始时开关K与a连接,则B极的电极反应式为
。
⑵若开始时开关K与b连接,总反应的离子方程式
为 。
有关上述实验,下列说法正确的是(填序号) 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电
解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中
转移0.2 mol电子
⑶该小组同学模拟工业上用离子交换膜法制烧碱
的方法,那么可以设想用右图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽的阳极反应式为 。
此时通过阴离子交换膜的离子数 (填“大于”
或“小于”或“等于”)通过阳离子交换膜的离子数。
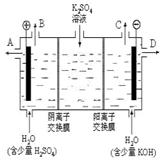 ②制得的氢氧化钾溶液从出口(填写“A”、“B”、
②制得的氢氧化钾溶液从出口(填写“A”、“B”、
“C”、“D”) 导出。
③通电开始后,阴极附近溶液pH会增大,请简述
原因 。
22.已知:向一体积为2L的密闭容器中加入0.1mol碘单质和足量的钨,当温度为943K时 存在:W(s)+I2(g)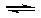 WI2(g)反应,反应达到平衡时碘单质的转化率为20%,
WI2(g)反应,反应达到平衡时碘单质的转化率为20%,
 (1)求943K时此反应的平衡常 数:K=_____________
(1)求943K时此反应的平衡常 数:K=_____________
(2)若起始时向此密闭容器中再加入0.1mol WI2 达平衡,此时容器中各气体的体积 比:___________,当同时加入等物质的量I2(g) 和WI2(g),平衡___________方向移动(填正反 应、逆反应或不移动)
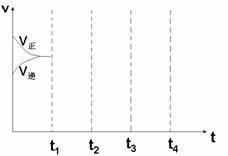
⑶画出W(s) + I2(g) 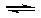 WI2(g) △H<0时 间-速率图。一定温度过量W 反应达 平衡, 到t1时降低温度,到t2时再加压,再到t3时加催化剂,到t4时加I2
WI2(g) △H<0时 间-速率图。一定温度过量W 反应达 平衡, 到t1时降低温度,到t2时再加压,再到t3时加催化剂,到t4时加I2
(4)一定温度下,向一容积不变的容器中加入足量钨和1molI2(g),使之反应: W(s) + I2(g) 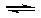 WI2(g) ΔH= -40.9KJ/mol,反应达平衡时气体平均摩尔质量增加 91.9g/mol,反应达平衡时放出的热量(已知钨的相对原子质量为183.8): ____________________.
WI2(g) ΔH= -40.9KJ/mol,反应达平衡时气体平均摩尔质量增加 91.9g/mol,反应达平衡时放出的热量(已知钨的相对原子质量为183.8): ____________________.
21.常温下将0.01molNH4Cl和0.002molNaOH溶于水配成1L溶液。
⑴用化学用语表示该溶液中的三个平衡关系是:
①______________________________________;
②______________________________________;
③______________________________________。
⑵这些微粒中浓度为0.01mol/L的是________,浓度为0.002mol/L的是_________。
⑶物质的量之和为0.01mol的两种微粒是_________________。
⑷ _________和________两种微粒数量之和比OH-多0.008mol。
20.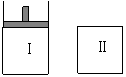 如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加 入3mol Z,起始时容器体积均为V L,发生反应并达到平衡(X、Y状态未知):aX(?) +2Y(?)
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加 入3mol Z,起始时容器体积均为V L,发生反应并达到平衡(X、Y状态未知):aX(?) +2Y(?) 3Z(g)。此时Ⅱ中X、Y、Z的物质的量之比为 3:2:2,则下列说法一定正确的是( )
3Z(g)。此时Ⅱ中X、Y、Z的物质的量之比为 3:2:2,则下列说法一定正确的是( )
A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
B.若X、Y不均为气态,则平衡时X的产率:Ⅰ>Ⅱ
C.若X、Y均为气态,则从起始到平衡所需时间:Ⅰ>Ⅱ
D.若X为固态,Y为气态,达平衡后若在Ⅱ中再加入1molZ,则新平衡时Z的体积分 数变大
Ⅱ 卷
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com