

3、(1)6-3-1-5-2-4; (2)21354 ;(3) CuSO4或NaOH溶液
3、电石中的碳化钙和水能完全反应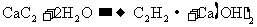 ,使反应产生的气体排水,测量出水的体积,可计算出标准状况下乙炔的体积,从而测定电石中碳化钙的含量:(1)若用下列仪器和导管组装实验装置:
,使反应产生的气体排水,测量出水的体积,可计算出标准状况下乙炔的体积,从而测定电石中碳化钙的含量:(1)若用下列仪器和导管组装实验装置:
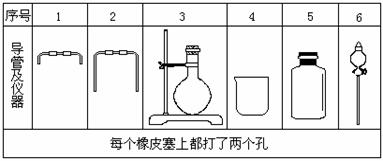
如果所制气体流向从左向右时,上述仪器和导管从从上到下,从左到右直接连接的顺序(填各仪器,导管的序号)是 接 接 接 接 接 。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次)
①称取一定量电石,置于仪器3中,塞紧橡皮塞
②检查装置的气密性
③在仪器6和5中注入适量水
④待仪器3恢复至室温时,量取仪器4中水的体积(导管2中水的体积忽略不计) ⑤慢慢开启仪器6 的活塞,使水逐滴滴下至不发生气体时,关闭活塞。
正确操作顺序(用操作编号填写)是
(3)若实验中产生的气体存在难闻的气味,且测定结果偏大,这是因为电石中含有杂质气体,可以用___________________(填试剂)加以除去。
2、下列除去杂质的方法正确的是
① 除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
② 除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤,分液、干燥、蒸馏;
③ 除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶;
④ 除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
A.① ② B.② ④ C.③ ④ D.② ③
答案:B
解析:①乙烷中混有少量乙烯应用溴水(或溴的四氯化碳溶液)进行洗气。若按题目叙述在光照条件下通入Cl2,不仅会引入新的杂质,而且会反应掉主要的物质乙烷。②因乙酸能与饱和碳酸钠溶液反应而乙酸乙酯在饱和碳酸钠溶液中的溶解度较小,因此②是正确的。因为CO2会与碳酸钠溶液反应CO2+H2O+Na2CO3=2NaHCO3,从而使主要物质CO2消耗,应用饱和碳酸氢钠溶液除去,因此③是错误的。若乙醇中混有少量的乙酸,加入生石灰后会反应掉在杂质乙酸和新生成的水而除去,再利用蒸馏可以得到纯净的乙醇,所以④是正确的。
1、下列有关试验操作的叙述正确的是
 A.实验室常用右图所示的装置制取少量的乙酸乙酯
A.实验室常用右图所示的装置制取少量的乙酸乙酯
 B.用50mL酸式滴定管可准确量取25.00mLKMnO4溶液
B.用50mL酸式滴定管可准确量取25.00mLKMnO4溶液
 C.用量筒取5.00mL 1.00mol·L-1盐酸于50mL容量瓶中,加水稀释至刻度,可配制0.100 mol·L-1盐酸
C.用量筒取5.00mL 1.00mol·L-1盐酸于50mL容量瓶中,加水稀释至刻度,可配制0.100 mol·L-1盐酸
 D.在苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出
D.在苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出
 答案:B
答案:B
解析:A项,导气管深入到饱和碳酸钠溶液中去了,这样容易产生倒吸,所以该装置不能用于制备乙酸乙酯;B项,准确量取一定体积的溶液,用的仪器室滴定管,滴定管有两种:酸式和碱式,具体使用范围是:酸式滴定管不得用于装碱性溶液,因为玻璃的磨口部分易被碱性溶液侵蚀,使塞子无法转动。碱式滴定管不宜于装对橡皮管有侵蚀性的溶液,如碘、高锰酸钾和硝酸银等。所以量取高锰酸钾溶液用酸式滴定管。C项,有两点错误之处,第一点量筒只能精确到小数点后一位,第二点在配制一定物质的量浓度的溶液时,溶解操作应在烧杯内溶解,不允许在容量瓶内溶解。D项,苯的密度比水小,飘在水上面,故有机层应该从上口倒出。
 [考点分析]常见实验的仪器组装,操作过程、注意事项要牢记;
[考点分析]常见实验的仪器组装,操作过程、注意事项要牢记;
 常见仪器的使用,以及在使用过程中所需要注意的地方(精确度)
常见仪器的使用,以及在使用过程中所需要注意的地方(精确度)
10、乙酸乙酯的水解
|
装置图 |
试剂 |
现象 |
结论 |
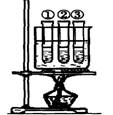 |
①乙酸乙酯+水 ②乙酸乙酯+稀硫酸 ③乙酸乙酯+氢氧化钠溶液 |
①酯层
②酯层 ③酯层 |
酯水解需要 、 催化,其中 催化较慢,反应 ; 催化较快,反应 |
|
方程式: ① 催化水解(可逆): ② 催化水解(不可逆): |
 [适应性训练]
[适应性训练]
9、乙酸的化学性质
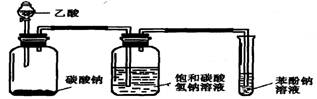
(1)乙酸、碳酸、苯酚的酸性比较
|
装饰图 |
 |
|
实验现象 |
①盛有碳酸钠固体的瓶中有
②盛有饱和碳酸氢钠溶液的瓶中有 ③盛有苯酚钠溶液的瓶中 |
|
化学方程式 |
① ② ③ |
|
结论 |
酸性:
﹥
﹥
|
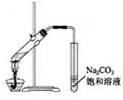
(2)乙酸和乙醇的酯化反应(乙酸乙酯的制取)
|
装置图 |
特别注意 |
 |
①试剂加入顺序:先
、再 、后 ②用小火加热,防止大量蒸出反应物 ③导管 (“能”或“否”)插入碳酸钠溶液中,防止 ④实验现象:有 色 状,比水 的 体生成 ⑤碳酸钠溶液可 乙酸乙酯中的乙酸, 乙醇,降低乙酸乙酯 |
8、醛基的检验
(1)银镜反应
|
实验操作 |
实验现象 |
结论及化学方程式 |
|
向1mL 2%的硝酸银溶液中滴加2%的稀氨水 |
先生成 色沉淀,后沉淀 得 |
|
|
向上述盛有银氨溶液的试管中加入3滴乙醛溶液, 加热 |
试管内壁
|
结论:乙醛中-CHO具有 |
(2)醛基被氢氧化铜氧化反应
|
实验操作 |
实验现象 |
结论及化学方程式 |
|
在试管中加入 的氢氧化钠溶液 mL,滴入 的硫酸铜溶液 滴,得到新制的请氧化铜,振荡 |
生成 色沉淀 |
|
|
加入乙醛溶液 mL, |
生成 色沉淀 |
结论:乙醛中-CHO具有 |
注:新制请氧化铜悬浊液中,氢氧化钠应 !
7、苯酚的化学性质及其检验
(1)苯酚的弱酸性
|
实验操作 |
实验现象 |
结论及化学方程式 |
|
①向盛有少量苯酚晶体的试管中加入少量水,振荡 |
|
苯酚在冷水中溶解度 |
|
②加入适量氢氧化钠溶液 |
|
苯酚 酸性 |
|
③再通入CO2 |
|
苯酚酸性比碳酸 |
(2)苯酚与溴水反应(苯酚的检验方法)
|
实验操作 |
实验现象 |
结论及化学方程式 |
|
向盛有少量苯酚稀溶液的试管中滴入饱和溴水,振荡 |
溴水 ,生成 |
|
注:苯酚与氯化铁显 色,也可以作为苯酚的检验方法。
6、乙醇的化学性质
(1)无水乙醇与金属钠反应
|
实验操作 |
实验现象 |
结论及化学方程式 |
|
向盛有无水乙醇的试管中加入一小块钠 |
金属钠
,有 ,反应比钠与水反应 ,反应生成的气体 点燃。 |
结论:乙醇中 上的H是活泼氢 |
(2)乙醇的催化氧化
|
实验操作 |
实验现象 |
结论和化学方程式 |
|
①在酒精灯上灼烧铜丝 |
铜丝表面
|
|
|
②将红热的铜丝插入到乙醇中 |
铜丝
|
(3)乙醇被强氧化剂氧化
|
实验操作 |
实验现象 |
结论 |
|
向少量重铬酸钾酸性溶液中滴加适量乙醇,振荡 |
溶液由 色变为 色 |
|
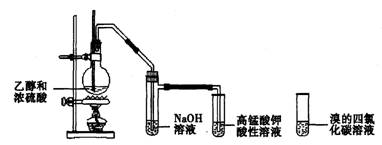
(4)乙醇的消去反应
|
装置图 |
 |
|
化学方程式 |
|
|
氢氧化钠溶液的作用 |
除去乙烯中可能存在的
和
杂质 |
|
实验现象 |
①将乙烯通入酸性高锰酸钾溶液,溶液
,乙烯被
②将乙烯通入溴的四氯化碳溶液,溶液 ,发生 反应 |
|
特别提示 |
①圆底烧瓶中加入
,向其中缓慢加入
,二者体积比约为 , ②温度计水银球要 ③烧瓶内要放入 ,防止 ④给混合液加热,使其温度迅速升至 |
5、溴乙烷中溴元素的检验
|
实验步骤 |
现象 |
结论及方程式 |
|
①取适量溴乙烷加入到 溶液中 |
|
溴乙烷 于水,比水 |
|
②加热充分反应 |
|
|
|
③加入
酸化 |
|
|
|
④加入
溶液 |
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com