
3.
2.
1.
4.忽视亚铁盐及Fe(OH)2易被空气中O2氧化成三价铁的化合物。
如某溶液中加入碱溶液后,最终得到红褐色沉淀,并不能断定该溶液中一定含有Fe3+,而也可能含有Fe2+。
[练习]铁及其重要化合物之间的转化关系,写出相应的化学方程式。
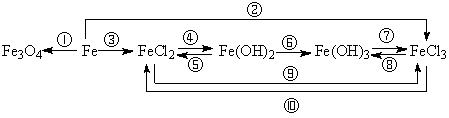
3.注意FeCl3、Fe2(SO4)3的水溶液蒸干所得剩余固体的区别。
FeCl3溶液加热浓缩时,因Fe3+水解产生HCl的挥发,得到的固体为Fe(OH)3,如灼烧后得到红色的Fe2O3固体。但Fe2(SO4)3溶液蒸干时,因硫酸是难挥发性酸,将不能得到Fe(OH)3固体,最终产物还是Fe2(SO4)3 。
2.过量的Fe与硝酸作用,或在Fe和Fe2O3的混合物中加入盐酸,要注意产生的Fe3+还可以氧化单质Fe这一隐含反应:Fe + 2Fe3+ === 3Fe2+。
|
|
Fe(OH)2 |
Fe(OH)3 |
|
物理性质 |
|
|
|
化学性质 |
(1)与非氧化性强酸反应 离子方程式: ; (2)与氧化性酸反应 与HNO3: ; (3)空气中放置被氧化 化学方程式: ; |
(1)与酸反应 离子方程式: ; (2)受热分解 化学方程式: ; |
|
制备 |
①
煮沸蒸馏水,赶走溶解的 ; ② 煮沸NaOH溶液,赶走溶解的 ; ③ 配制FeSO4溶液,加少量的 ; ④用长滴管将NaOH溶液送入FeSO4溶液 ,离子方程式 。 |
将NaOH溶液滴入Fe2(SO4)3溶液中 离子方程式: 。 |
[练习]下列物质中含有少量杂质,请在空格中填上适宜的试剂或方法将杂质除去:
|
物质 |
杂质 |
试剂或方法 |
化学(或离子)方程式 |
|
FeCl3溶液 |
FeCl2 |
|
|
|
FeCl2溶液 |
FeCl3 |
|
|
|
FeSO4溶液 |
CuSO4 |
|
|
|
Fe2O3 |
Al2O3 |
|
|
|
Fe2O3 |
Fe(OH)3 |
|
|
|
Fe(OH)3 |
Al(OH)3 |
|
|
注意:
1.NO3-与Fe2+在酸性条件下,不能共存。 ( 3Fe2+ + 4H+ + NO3- === 3Fe3+ + NO↑ +2H2O )
1.铁的氧化物的比较
|
铁的 氧化物 |
FeO |
Fe2O3 |
Fe3O4 |
||
|
俗称 |
|
|
|
||
|
色、态 |
|
|
|
||
|
铁的价态 |
|
|
|
||
|
水溶性 |
|
||||
|
稳定性 |
不稳定性 6FeO+O2=2Fe3O4 |
稳定 |
稳定 |
||
|
与酸反应 离子方程式 |
|
|
|
||
|
与还原性酸反应(HI) |
|
|
|
||
|
与氧化性酸反应(HNO3) |
|
|
|
||
|
与CO(H2、Al、C等)的反应 |
FexOy+ CO= Fe+ CO2 |
||||
|
制取 |
高温熔融,过量的铁与氧气反应 2Fe+O2=2FeO |
Fe(OH)3的分解 2Fe(OH)3=Fe2O3+3H2O |
铁在氧气中燃烧 3Fe+2O2=Fe3O4 |
||
6. )
从以上6各方面选取代表性物质书写方程式(每个方面至少写两个):
1.
2.
3.
4.
5.
6.
小结5: 常见铁的化合物的颜色状态
|
物质 |
Fe |
FeO |
Fe2O3 |
Fe3O4 |
Fe(OH)2 |
Fe(OH)3 |
Fe2+ |
Fe3+ |
Fe(SCN)2+ |
|
颜色 |
|
|
|
|
|
|
|
|
|
|
状态 |
|
|
|
|
|
|
|
|
|
5. )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com