
1.已知集合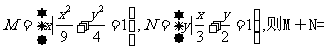 ( )
( )
A. 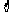 B.
B. 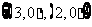 C.
C. 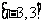 D.
D.
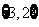
30、下图是一套制取并验证氯气部分化学性质的实验装置。
回答下列问题:反应的方程式:MnO2+4HCl(浓) MnCl2+2H2O+
Cl2↑
MnCl2+2H2O+
Cl2↑
(1)装置A中,仪器a的名称叫____________[“分液漏斗”或“长颈漏斗”选择],
该仪器中盛有的试剂为__ __。
(2)当Cl2气流通过一段时间后,装置B中溶液的pH值____7(填“>”“<”或“=”), 写出Cl2与水反应的方程式
[提示:氯气和水反应生成盐酸和HClO]
(3)当有少量Cl2气流通过后,观察到装置C中的溶液变为蓝色,这是因为氯气和碘化钾溶液反应产生________单质,能与____________溶液作用变蓝。
(4)装置E的作用是_____ ___。
(5) 请把MnO2+4HCl(浓) MnCl2+2H2O+
Cl2↑改写成离子方程式:
MnCl2+2H2O+
Cl2↑改写成离子方程式:
___________________________________________________________________
29、用化学用语完成下列填空
(1)H2SO4 电离方程式:__________________________________________________
(2)CH3COOH电离方程式: ______________________________________________
(3) 氨水和硫酸铝反应制氢氧化铝和硫酸铵的离子方程式:
_________________________________________________________________
23、 蛋白质是构成生命的基础物质。在鸡蛋、蔬菜、花生油等食物中,富含蛋白质的是 。"84消毒液”在日常生活中被广泛使用。该消毒液无色,对某些有色物质具有漂白作用,它的有效成分是 (填" KMnO4”或",NaClO")。
24下表是元素周期表的一部分,针对所给的10种元素,完成下列各小题。
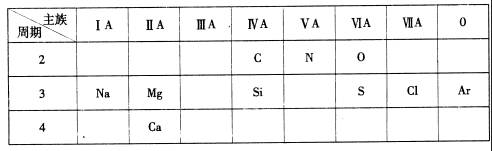 (1)金属性最强的元素是 (填元素名称);
(2)Ar原子结构示意图为 ;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是 (填化学式);
(4)C和N中,原子半径较小的是
;
(5)“高钙牛奶”中的钙是指
(填“元素”或“单质”);
(6)Si是带来人类文明的重要元素之一,其氧化物常用于制造 (填一种高性能的现代通讯材料的名称);
(7)镁是一种重要的金属材料,工业上采用电解熔融氯化镁获得金属镁,该反应的化学方程式为 ________________________________________________
;
(8)O(氧元素)元素形成的一种氢化物的化学式是
,该物质中H元素与0元
(1)金属性最强的元素是 (填元素名称);
(2)Ar原子结构示意图为 ;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是 (填化学式);
(4)C和N中,原子半径较小的是
;
(5)“高钙牛奶”中的钙是指
(填“元素”或“单质”);
(6)Si是带来人类文明的重要元素之一,其氧化物常用于制造 (填一种高性能的现代通讯材料的名称);
(7)镁是一种重要的金属材料,工业上采用电解熔融氯化镁获得金属镁,该反应的化学方程式为 ________________________________________________
;
(8)O(氧元素)元素形成的一种氢化物的化学式是
,该物质中H元素与0元
素的质量比 。(相对原子质量:H-1 0-16) 25(6分)
(1)氢氧化铝Al(OH)3是一种治疗胃酸(含盐酸)过多的药物,请用化学方程式表示该反应的原理: 。
(2)碳酸氢钠NaHCO3加热分解,请用化学方程式表示该反应的原理:
。
26从A.甲醛 B.葡萄糖 C.乙醇 D.乙酸 E.油脂 等五种有机物中选择合适的答案,将其标号填在空格内。
(1)工业上制备肥皂的主要原料是 。
(2)能用于除去热水瓶胆水垢(主要成分:CaCO3 ,Mg(OH)2)的是 。
(3)家居装修材料中散发出的有毒物质是
(4)常用做燃料和医药上消毒剂的是
(5)糖尿病人通常是指病人的尿液中 的含量高。
27 用C、Fe和Al组成的混合物进行如下图所示实验。

填写下列空白。
(1)气体X为 ,固体Z为 。
(2)写出铁和稀硫酸反应的方程式__________ _________ 。
(3)Y滤液中除有剩余的H+、Fe2+还有____________阳离子。
28

18、 实验室中配制250mL 0.20mo1·L-1NaOH溶液时,必须使用到的玻璃仪器是

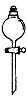
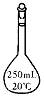 锥形瓶 试管 分液漏斗 容量瓶
A B C D
19、 不属于氧化还原反应的是
A、2Al+Fe2O3
锥形瓶 试管 分液漏斗 容量瓶
A B C D
19、 不属于氧化还原反应的是
A、2Al+Fe2O3 2Fe+Al2O3
B、2Mg+CO2
2Fe+Al2O3
B、2Mg+CO2 2MgO+C
C、N2+3H2
2MgO+C
C、N2+3H2 2NH3
D、SiO2+CaO
2NH3
D、SiO2+CaO CaSiO3
20、 在溶液中能大量共存的离子组是
A、H+、OH-、Na+ B、K+、NO3-、Cu2+
C、Ba2+、SO42-、Na+
D、Fe3+、OH-、NH4+
21、下列表达不科学的是
A.同周期元素,从左到右,原子半径逐渐减小,称有气体除外
CaSiO3
20、 在溶液中能大量共存的离子组是
A、H+、OH-、Na+ B、K+、NO3-、Cu2+
C、Ba2+、SO42-、Na+
D、Fe3+、OH-、NH4+
21、下列表达不科学的是
A.同周期元素,从左到右,原子半径逐渐减小,称有气体除外
B.酸性强弱:HClO4>H2SO4>H3PO4>H2SiO3 C.碱性强弱:NaOH <Mg(OH)2<Al(OH)3
D.同族元素,从上到下,原子半么逐渐增大 22、 下列四个试管中,过氧化氢分解产生氧气的反应速率最大的是
|
试管 |
温度 |
过氧化氢溶液浓度 |
催化剂 |
|
A |
常温 |
3% |
-- |
|
B |
水浴加热 |
3% |
-- |
|
C |
水浴加热 |
6% |
MnO2 |
|
D |
常温 |
6% |
-- |
[选择题答案填写处]
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
|
|
|
|
|
|
|
|
|
|
|
|
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
|
|
|
|
|
|
|
|
|
|
|
|
1、 党的十七大报告提出,促进国民经济又好又快发展,要加强能源资源节约和生态环境保护。以下做法与此精神相违背的是
A.控制高能耗企业上马
B.加大对污染企业的整治力度
C.无节制地开采煤、石油、天然气等矿物资源
D.倡导“绿色化学”理念,逐步实现化工企业零排放
2、 NA为阿伏加德罗常数,下列物质所含分子数最多的是
A.0.8 mol二氧化碳
B.标准状况下2.24L氨气
C.3.6g水(水的摩尔质量为18g·mol-1)
D.含NA个氢分子的氢气
3、 垃圾的再生利用是垃圾资源化的最佳途径。某垃圾箱上贴有
如右图所示标志,应向此垃圾箱中丢弃的垃圾是
A.废旧电池 B.厨余垃圾 C.危险废物
D.可回收物
4、 下列物质中,既有离子键,又有共价键的是
A.NaCl
B.Ca(OH)2
C.H2O
D.CH4
5、下列气态氢化物最稳定的的是
A. HCl B.HBr C.HI D.HF
6、 能用离子方程式“H++OH-===H2 O”表示的化学反应是
A、4HNO3 2H2O+4H2O↑+O2↑ B、NaOH+HCl=NaCl+H2O
C、Fe2O3+6HCl=2FeCl3+3H2O D、2H2+O2
2H2O+4H2O↑+O2↑ B、NaOH+HCl=NaCl+H2O
C、Fe2O3+6HCl=2FeCl3+3H2O D、2H2+O2 2H2O
7、 成人人体中缺某种微量元素时,会引起甲状腺肿大,该元素是
A.碘
B.氟 C.铁 D.锌
8、将一小块钠投入到NH4Cl溶液中,产生的气体是
A.氢气和NH3
B.只有氢气 C.只有NH3 D.氧气和氢气
9、 下列说法正确的是
A.等质量氢气和氯气所含分子数一样
2H2O
7、 成人人体中缺某种微量元素时,会引起甲状腺肿大,该元素是
A.碘
B.氟 C.铁 D.锌
8、将一小块钠投入到NH4Cl溶液中,产生的气体是
A.氢气和NH3
B.只有氢气 C.只有NH3 D.氧气和氢气
9、 下列说法正确的是
A.等质量氢气和氯气所含分子数一样
B.阿伏加德罗的精确值为6.02x1023mol-1
C.硫酸根的摩尔质量是96g/mol
D.二氧化碳的摩尔质量是44克
10、 日常生活中,常用到化学知识。下列说法不正确的是
A.某些铁盐溶于水生成的Fe(OH) 3胶体,可除去水中的悬浮颗粒等杂质
B.维生素C高温时容易被破坏,所以不宜热锅爆炒蔬菜
C.构成人体蛋白质的20多种氨基酸都能通过人体自身合成
D.可用燃烧的方法鉴别真丝围巾和合成纤维围巾
11、 下列物质互为同素异形体的是
A、612C和613C
B、金刚石和石墨
C、CH4和C2H6
D、CH3CH2CH2CH3和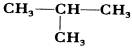 12、 下列关于能量转化的认识中,不正确的是
A.电解饱和食盐水时,电能转化为化学能
B.树木进行光合作用时,太阳能转化为化学能
C.汽油燃烧时,化学能转化为热能
D.电灯工作时,电能全部转化为光能
13、 右下图是某有机物的球棍模型,其中
12、 下列关于能量转化的认识中,不正确的是
A.电解饱和食盐水时,电能转化为化学能
B.树木进行光合作用时,太阳能转化为化学能
C.汽油燃烧时,化学能转化为热能
D.电灯工作时,电能全部转化为光能
13、 右下图是某有机物的球棍模型,其中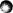 (代表氢原子,
(代表氢原子,
 代表碳原子,该有机物的名称是
代表碳原子,该有机物的名称是  A.乙烷[CH3CH3]
B.乙醇[CH3CH2OH] C.乙烯[CH2=CH2] D.乙酸[CH3COOH]
14、 暴露在空气中不易变质的是
A.钠 B.氧化钠 C.氯化钠 D.氢氧化钠
15、 随着科学技术的发展,新材料层出不穷。下列属于金属材料的是
A.生物陶瓷
B.钢化玻璃 C.钛合金
D.聚四氟乙烯
16、金属钠和纯水反应实验中,下列现象没有产生的是
A.产生气体
B.溶液充变红色
C.钠块熔化成银白色小球
D.银白色的小球浮在水面上
17、 下列各装置中,能构成原电池的是
A.乙烷[CH3CH3]
B.乙醇[CH3CH2OH] C.乙烯[CH2=CH2] D.乙酸[CH3COOH]
14、 暴露在空气中不易变质的是
A.钠 B.氧化钠 C.氯化钠 D.氢氧化钠
15、 随着科学技术的发展,新材料层出不穷。下列属于金属材料的是
A.生物陶瓷
B.钢化玻璃 C.钛合金
D.聚四氟乙烯
16、金属钠和纯水反应实验中,下列现象没有产生的是
A.产生气体
B.溶液充变红色
C.钠块熔化成银白色小球
D.银白色的小球浮在水面上
17、 下列各装置中,能构成原电池的是
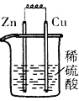
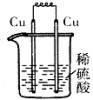
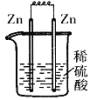
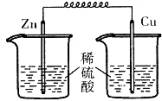 A B C D
A B C D
厦门市杏南中学高二文科化学月考试题
第II卷
22.(本小题满分12分)
设函数f(x)是定义在[-1,0)∪(0,1]上的奇函数,当x∈[-1,0)时,f(x)=2ax+ (a∈R).
(1)当x∈(0,1]时,求f(x)的解析式;
(2)若a>-1,试判断f(x)在(0,1]上的单调性,并证明你的结论;
(3)是否存在a,使得当x∈(0,1]时,f(x)有最大值-6.
21. (本小题满分14分)
设椭圆 =1(a>b>0)的焦点为F1、F2,P是椭圆上任一点,若∠F1PF2的最大值为 .
(1)求椭圆的离心率;
(2)设直线l与椭圆交于M、N两点且l与以原点为圆心,半径为短轴的圆相切.已知线段MN的长度最大值为4,求椭圆的方程与直线l的方程.
20.(本小题满分12分)
某家用电器厂根据其产品在市场上的销售情况,决定对原来以每件2000元出售的一种产品进行调价,并按新单价的八折优惠销售.结果每件产品仍可获得实际销售价20%的利润.已知该产品每件的成本是原销售价的60%.
(1)求调价后这种产品的新单价是每件多少元?让利后的实际销售价是每件多少元?
(2)为使今年按新单价让利销售后的利润总额不低于20万元,今年至少应销售这种产品多少件?(每件产品利润=每件产品的实际销售价-每件产品的成本价)
19.(本小题满分12分)
如图,正三棱柱ABC-A1B1C1中,E∈BB1,截面A1EC⊥侧面AC1.
(1)求证: ;
(2)若 ,求平面A1EC与平面A1B1C1所成二面角的平面角(锐角)的大小.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com