
18ЃЎ(1)двђЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
(2)
ЂйРызгЗНГЬЪНЮЊЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂкРызгЗНГЬЪНЮЊЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂлpHгІПижЦдкЁЁЁЁ ЁЁЁЁЁЁЁЁЗЖЮЇФкЁЃ
(3)ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
17ЃЎ(1) ФмЫЕУїЗДгІДяЕНЦНКтЕФЪЧЁЁЁЁ ЁЁЁЁЁЁЁЁЃЛ
ЁЁ(2) aКЭbЕФЙиЯЕЪЧЁЁЁЁ ЁЁЁЁЁЁЃЛ
ЁЁ(3) X=ЁЁЁЁ ЁЁЁЁЁЁЁЁ, Q1ЁЂQ2МфТњзуЕФЙиЯЕЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
16ЃЎ(1)BЁЂCЁЂDЁЂXбѕЛЏадДгЧПЕНШѕЕФЫГађЪЧЃК(гУЛЏбЇЪНЬюаД)
ЁЁЁЁЁЁЁЁ ___________________________________________________________ЁЃ
(2)BЕФЕчзгЪНЮЊЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ __________ЁЃ
(3)аДГіЗДгІЂкЕФЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ _______________________ЁЃ
(4)РызгЗНГЬЪНЃК
Ђй_________________________________________________________________ЃЛЁЁ Ђо_________________________________________________________________ЁЃ
15ЃЎ(1)МйЩш1ЃКШмвКГЪЛЦЩЋВЛЪЧЗЂЩњЛЏбЇЗДгІЫљжТЃЌЪЧШмвКжаЁЁЁЁЁЁЁЁЁЁ в§Ц№ЕФ(ЬюЮЂСЃЕФЛЏбЇЪНЃЌЯТЭЌ)ЁЃ
ЁЁЁЁ МйЩш2ЃКШмвКГЪЛЦЩЋЪЧЗЂЩњЛЏбЇЗДгІЫљжТЃЌЪЧШмвКжаЁЁЁЁЁЁЁЁЁЁЁЁ в§Ц№ЕФЁЃ
ЁЁЁЁЁЁ [ЩшМЦЪЕбщЗНАИ]
ЁЁЁЁ МйЩш1ЗНАИЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁЁЁ МйЩш2ЗНАИЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ФуШЯЮЊЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАМйЩш1ЁБЛђЁАМйЩш2ЁБ)ЕФЭЦЖЯЪЧе§ШЗЕФЃЛШєбЁгУЕэЗлЕтЛЏМиШмвКбщжЄФуЕФМйЩшЪЧЗёПЩаа?_ЁЁЁЁЁЁЁЁ (ЬюЁАааЁБЛђЁАЗёЁБ)ЃЌРэгЩЪЧЃК___________________ЁЁЁЁЁЁЁЁ ___ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
21ЃЎ(ЮяжЪНсЙЙгыаджЪ)ЕЊЪЧЕиЧђЩЯМЋЮЊЗсИЛЕФдЊЫиЁЃ
(1)Li3NОЇЬхжаЕЊвдN3-ДцдкЃЌЛљЬЌN3-ЕФЕчзгХХВМЪНЮЊЁЁЁЁ ЁјЁЁЁЁ ЁЃ
(2)NЁдNЕФМќФмЮЊ942 kJЁЄmol-1ЃЌN-NЕЅМќЕФМќФмЮЊ247 kJЁЄmol-1ЃЌМЦЫуЫЕУїN2жаЕФ
ЁЁЁЁ
ЁјЁЁ МќБШЁЁЁЁ ЁјЁЁЁЁ МќЮШЖЈ(ЬюЁА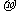 ЁБЛђЁА
ЁБЛђЁА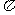 ЁБ)ЁЃ
ЁБ)ЁЃ
(3)(CH3)3NH+КЭAlCl-4ПЩаЮГЩРызгвКЬхЁЃРызгвКЬхгЩвѕЁЂбєРызгзщГЩЃЌШлЕуЕЭгк100ЁцЃЌЦфЛгЗЂадвЛАуБШгаЛњШмМСЁЁЁЁ ЁјЁЁ (ЬюЁАДѓЁБЛђЁАаЁЁБ)ЃЌПЩгУзїЁЁЁЁ ЁјЁЁ (ЬюДњКХ)ЁЃ
aЁЂжњШММСЁЁЁЁЁЁЁЁЁЁ bЁЂЁАТЬЩЋЁБШмМС
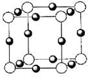 cЁЂИДКЯВФСЯЁЁЁЁЁЁ dЁЂОјШШВФСЯ
cЁЂИДКЯВФСЯЁЁЁЁЁЁ dЁЂОјШШВФСЯ
(4)X+жаЫљгаЕчзге§КУГфТњKЁЂLЁЂMШ§ИіЕчзгВуЃЌЫќгыN3-аЮГЩ
ЕФОЇЬхНсЙЙШчЭМЫљЪОЁЃXЕФдЊЫиЗћКХЪЧЁЁ ЁјЁЁЁЁ ЃЌгыЭЌвЛИі
N3-ЯрСЌЕФX+гаЁЁ ЁјЁЁ ИіЁЃ
(5)2008ЕФЧяЬьЃЌЖОФЬЗлЪТМўе№ОЊШЋЙњЃЌетжївЊЪЧФЬЗлжаКЌгагаЖОЕФШ§ОлЧшАЗЁЁЁЁ (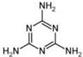 )ЁЃ
)ЁЃ
ЯТСаЙигкШ§ОлЧшАЗЗжзгЕФЫЕЗЈжае§ШЗЕФЪЧЁЁ ЁјЁЁЁЁ ЁЃ
ЁЁAЃЎЫљгаЬМдзгВЩгУsp2дгЛЏЃЌЫљгаЕЊдзгВЩгУsp3дгЛЏ
ЁЁBЃЎвЛИіЗжзгжаЙВКЌга15ИіІвМќ
ЁЁCЃЎЪєгкМЋадЗжзгЃЌЙЪМЋвзШмгкЫЎ
ЁЁDЃЎаЮГЩЕФОЇЬхШлЕуНЯИп



 ОфШнИпМЖжабЇ2010НьИпШ§12дТЕїбаВтЪд
ОфШнИпМЖжабЇ2010НьИпШ§12дТЕїбаВтЪд
ЛЏбЇД№ОэжН
зЂвтЃКНЋвЛЁЂЖўЯюбЁдёЬтД№АИЬюЭПЕНД№ЬтПЈЩЯ
20ЃЎШЁm gЬњЗлгыКЌга0.8molHNO3ЕФЯЁЯѕЫсЗДгІЃЌЗДгІКѓЯѕЫсКЭЬњОљЮоЪЃгрЃЌЧвЯѕЫсЕФЛЙдВњЮяжЛгаNOЁЃ
(1)ШєЗДгІКѓЕФШмвКжаЕЮМгKSCNШмвКВЛБфКьЩЋЃЌдђmЃНЁЁЁЁ ЁјЁЁЁЁ ЃЛ
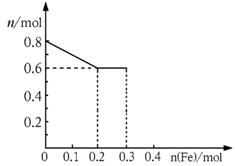 (2)ШєНЋЬњЗлТ§Т§МгШыЕНЯЁЯѕЫсжаЃЌВЂНСАшЃЌЗДгІЙ§ГЬжаШмвКРяFe3+ЁЂFe2+ЁЂNO3-Ш§жжРызгжаЕФФГРызгЕФЮяжЪЕФСПЕФБфЛЏЧњЯпШчЭМЫљЪОЃЌдђИУЧњЯпБэЪОЕФЪЧ_ Ёј _ЮяжЪЕФСПБфЛЏЃЌЧыФудкДЫЭМжадйЛГіСэЭт2жжРызгЕФЮяжЪЕФСПЕФБфЛЏЧњЯпВЂзЂУїРызгжжРрЁЃ
(2)ШєНЋЬњЗлТ§Т§МгШыЕНЯЁЯѕЫсжаЃЌВЂНСАшЃЌЗДгІЙ§ГЬжаШмвКРяFe3+ЁЂFe2+ЁЂNO3-Ш§жжРызгжаЕФФГРызгЕФЮяжЪЕФСПЕФБфЛЏЧњЯпШчЭМЫљЪОЃЌдђИУЧњЯпБэЪОЕФЪЧ_ Ёј _ЮяжЪЕФСПБфЛЏЃЌЧыФудкДЫЭМжадйЛГіСэЭт2жжРызгЕФЮяжЪЕФСПЕФБфЛЏЧњЯпВЂзЂУїРызгжжРрЁЃ
(3)дк(2)ЗДгІКѓЕФШмвКжаМгШыКЌ0.1molH2SO4ЕФЯЁСђЫсЃЌМЦЫуЛЙФмВњЩњЕФЦјЬхЕФЬхЛ§(БъПіЯТ)ЁЃ
19ЃЎ(1)ФГвЛЗДгІЬхЯЕжаЕФЮяжЪгаЃКHClЁЂSnCl2ЁЂH2SnCl6ЁЂAsЁЂH3AsO3ЁЂH2OЃЌвбжЊЃКHClЪЧЗДгІЮяжЎвЛЁЃ
ЂйаДГіВЂХфЦНИУЗДгІЕФЛЏбЇЗНГЬЪНЃКЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁјЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкдкИУЗДгІжаЃЌЕУЕчзгЕФЮяжЪЪЧЁЁЁЁЁЁ ЁјЁЁЁЁЁЁ ЃЌБЛбѕЛЏЕФдЊЫиЪЧЁЁЁЁ ЁјЁЁЁЁ ЁЃ
ЂлдкЗДгІжаЃЌУПзЊвЦ1 molЕчзгЃЌЯћКФHClЁЁЁЁЁЁ ЁјЁЁЁЁЁЁ molЁЃ
(2)НЋ2.5gЬМЫсФЦЁЂЬМЫсЧтФЦКЭЧтбѕЛЏФЦЕФЙЬЬхЛьКЯЮяЭъШЋШмНтгкЫЎЃЌжЦГЩЯЁШмвКЃЌШЛКѓЯђИУШмвКжаж№ЕЮМгШы1molЁЄLЃ1ЕФбЮЫсЃЌЫљМгШыбЮЫсЕФЬхЛ§гыВњЩњCO2ЕФЬхЛ§(БъзМзДПі)ЙиЯЕШчЯТЭМЫљЪОЃК
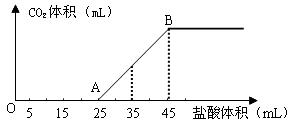
ЂйаДГіOAЖЮЫљЗЂЩњЗДгІЕФРызгЗНГЬЪН______________________________________ЁЃ
ЂкЕБМгШы35mLбЮЫсЪБЃЌВњЩњCO2ЕФЬхЛ§ЮЊ___________mL(БъзМзДПі)ЁЃ
18ЃЎИѕ(Cr)ЪєгкжиН№ЪєдЊЫиЃЌКЌИѕЗЯЫЎКЭЗЯдќХХЗХБиаыОЙ§ДІРэДяЕНгаЙиЕФАВШЋБъзМЁЃ
(1)КЌИѕЗЯЫЎХХЗХЕНКгЫЎжавЛЖЈХЈЖШЛсЪЙгуРрЕШЫЎЩњЖЏЮяЫРЭіЕФдвђЪЧЁЁ ЁјЁЁЁЁ ЃЛ
(2)ИѕдЊЫивдCr2O72-РызгЕФаЮЪНДцдкгкЫсадЗЯЫЎжаЃЌГЃгУFeSO4НЋЦфЛЙдЮЊCr3+РызгЃЌдйгУГСЕэЗЈНјааЗжРыЁЃ
вбжЊЃК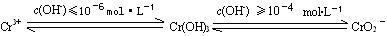
Ђй FeSO4ЛЙдCr2O72-ЕФРызгЗНГЬЪНЮЊЁЁЁЁ ЁјЁЁЁЁ ЁЃ
Ђк Cr2 (SO4) 3ШмвКжаМгШыЙ§СПNaOHХЈШмвКЃЌЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁ ЁјЁЁЁЁ ЁЃ
Ђл ГСЕэЗЈЗжРыЗЯЫЎжаЕФCr3+РызгЃЌpHгІПижЦдкЁЁЁЁ ЁјЁЁЁЁ ЗЖЮЇФкЁЃ
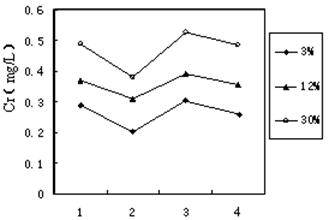 (3)ИѕвБСЖЙЄвЕЕФЗЯдќЗлЫщКѓВєШыУКэЗЪЏОЙ§ИпЮТДІРэПЩвджЦзЉЃЌЮЊСЫЬНОПЦфжаЕФИѕдЊЫидкЪЙгУЙ§ГЬжаЪЧЗёЛсжиаТЮлШОЛЗОГЃЌбаОПзщдквЛЖЈЬѕМўЯТНўШмзЉбљЃЌМьВтНўГівКжаCrдЊЫиХЈЖШЃЌНсЙћШчЭМЃК
(3)ИѕвБСЖЙЄвЕЕФЗЯдќЗлЫщКѓВєШыУКэЗЪЏОЙ§ИпЮТДІРэПЩвджЦзЉЃЌЮЊСЫЬНОПЦфжаЕФИѕдЊЫидкЪЙгУЙ§ГЬжаЪЧЗёЛсжиаТЮлШОЛЗОГЃЌбаОПзщдквЛЖЈЬѕМўЯТНўШмзЉбљЃЌМьВтНўГівКжаCrдЊЫиХЈЖШЃЌНсЙћШчЭМЃК
ЁЁЫЕУїЃК1--гУеєСѓЫЎНўШмЃЌЁЁ 2--гУЯЁСђЫсНўШмЃЌ3--ЖГШкКѓгУеєСѓЫЎНўШмЃЌ4--ЦиЩЙКѓгУеєСѓЫЎНўШмЃЛ3%ЕШ--жЦзЉЪБКЌИѕЗЯдќВєШыЕФБШР§ЁЃ
вбжЊЮвЙњЙцЖЈ ЁАЙЬЬхЗЯЦњЮяНўГіБъзМжЕКЌИѕВЛЕУГЌЙ§10 mgЁЄLЃ1ЁБЁЃЗжЮіЭМБэЃЌПЩЕУГіЖрИіНсТлЃК
Ђй ЪЕбщШЁгУЕФзЉбљЗћКЯЩЯЪіБъзМЃЛ
Ђк ЛЙФмЕУГіЕФЦфЫќНсТлЪЧ(аДГі2ЬѕМДПЩ)ЁЁЁЁ ЁјЁЁЁЁ ЃЛЁЁЁЁ ЁјЁЁЁЁ ЁЃ
17ЃЎ(8Зж)ШчЯТЭМЫљЪОЃЌдквЛЖЈЮТЖШЯТЃЌдквЛИіШнЛ§ЮЊ4LЕФУмБеШнЦїжаЃЌзѓЪвМгШыX molSO3ЃЌгвЪвМгШы2 molSO2КЭ1 molO2ЃЌжаМфЪЧИіПЩвЦЖЏЕФИєАхKЃЌдкЩйСПДпЛЏМСДцдкЯТЗжБ№ЗЂЩњЗДгІЃКЁЁЁЁ
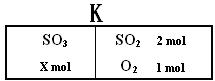
зѓЪвЃК2SO3(g)
 ЁЁ2SO2(g) + O2(g)ЁЁ гвЪвЃК2SO2(g)
+ O2(g)
ЁЁ2SO2(g) + O2(g)ЁЁ гвЪвЃК2SO2(g)
+ O2(g)  ЁЁ2SO3(g)ЁЁ ЁїH=Ѓ197kJ/mol
ЁЁ2SO3(g)ЁЁ ЁїH=Ѓ197kJ/mol
ЛиД№ЯТСаЮЪЬтЃК
(1) ФмЫЕУїЗДгІДяЕНЦНКтЕФЪЧЁЁЁЁ ЁјЁЁЁЁ ЃЛ
AЁЂИєАхВЛдйвЦЖЏЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЁЂзѓгвЖўЪвSO2КЭO2ЮяжЪЕФСПжЎБШЯрЕШ
CЁЂзѓгвСНБпSO2ЕФЮяжЪЕФСПЯрЕШЁЁЁЁЁЁ DЁЂзѓгвСНБпSO3ЕФЬхЛ§ЗжЪ§ЯрЕШ
(2) ЕБX=0.5ЪБЃЌЦНКтКѓгвЪвSO2ЕФЬхЛ§ЗжЪ§ЮЊaЃЛX=1ЪБЃЌЦНКтКѓгвЪвSO2ЕФЬхЛ§ЗжЪ§ЮЊbЃЌдђaКЭbЕФЙиЯЕЪЧЁЁЁЁ ЁјЁЁЁЁ ЃЛ
ЁЁ AЁЂa>bЁЁЁЁЁЁЁЁЁЁЁЁ BЁЂa=bЁЁЁЁЁЁЁЁЁЁ CЁЂa<bЁЁЁЁЁЁЁЁЁЁ DЁЂЮоЗЈШЗЖЈ
(3) ШєЦНКтЪБИєАхдкжабыЃЌдђX=ЁЁЁЁ ЁјЁЁ , зѓЪвЮќЪеЕФШШСПЮЊQ1 kJЃЌгвЪвЗХГіЕФШШСПЮЊQ2 kJЃЌдђQ1ЁЂQ2МфТњзуЕФЕШЪНЙиЯЕЪЧЁЁ ЁјЁЁЁЁ ЃЛ
16ЃЎ(10Зж)вбжЊA-FЪЧжабЇЛЏбЇжаГЃМћЮяжЪЃЌЦфжаAЁЂCЁЂEЁЂFЮЊЦјЬхЃЌBЁЂDЮЊвКЬхЃЌDЕФЯћЗбСПГЃзїЮЊвЛИіЙњМвЙЄвЕЗЂДяЫЎЦНЕФвЛжжБъжОЃЌFЕФХЈШмвКгыXЙВШШЭЈГЃгУгкЪЕбщЪвжЦБИЕЅжЪCЃЌXЪЧвЛжжКкЩЋЗлФЉЃЌBЗжзгжага18ИіЕчзгЁЃЗДгІжаВПЗжЩњГЩЮявбТдШЅЁЃЪдЛиД№ЯТСаЃК
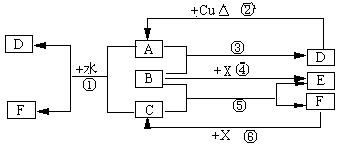
(1)ИљОнЭМжааХЯЂЃЌBЁЂCЁЂDЁЂXбѕЛЏадДгЧПЕНШѕЕФЫГађЪЧЃК(гУЛЏбЇЪНЬюаД)
ЁЁЁЁЁЁ ____________Ёј_____________________________________________ЁЃ
(2)BЕФЕчзгЪНЮЊЃК_____Ёј__ЁЁЁЁЁЁЁЁЁЁ __
(3)аДГіЗДгІЂкЕФЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁ ЁЁЁЁЁЁ ЁјЁЁЁЁЁЁЁЁЁЁЁЁ _______ЁЃ
(4)аДГіЗДгІЂйЁЂЂоЕФРызгЗНГЬЪНЃК
Ђй_________________ЁЁ ЁјЁЁЁЁЁЁЁЁЁЁ ________ЃЛ
Ђо_______________ЁЁЁЁ ЁјЁЁЁЁЁЁ __________ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com