
4.在体积为V升的密闭容器中通入a摩NO2和b摩O2.反应后容器内氮原子数和氧原子数之比为
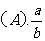
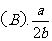
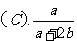
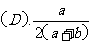
3.有五瓶溶液分别是:①l0mL0.60mol•L-1 NaOH水溶液,②20mL0.50 mol•L-1H2SO4。③30mLO .4 mol•L-1 HCl④40mL0.30 mol•L-1HAc水溶液,⑤50mL0.20 mol•L-1蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是
A.①>②>③>④>⑤ B.②>①>③>④>⑤
C.②>③>④>①>⑤ D.⑤>④>③>②>①
2.设nA代表阿伏加德罗常数(NA)的数值,下列说法正确的是
A.22.4 L Cl2中含有nA个C12分子
B.1 L
0.1 mol·L-1 Na2SO4溶液中有0.1
nA个Na+
C.1 mol H2与1 mol C12反应生成nA个HCl分子
D.1 mol Ca变成Ca2+时失去的电子数为2 nA
1.用NA表示阿伏加德罗常数,下列叙述中正确的是
A.0.1mol·L-1稀硫酸100mL中含有硫酸根个数为0·1NA
B.1mol CH3+(碳正离子)中含有电子数为10NA
C.2.4g金属镁与足量的盐酸反应,转移电子数为2NA
D. 12.4g白磷中含有磷原子数为O.4NA
2.判断下列操作对最终结果的影响。
(1)配制氯化钠溶液中,定容摇匀后发现液面较低,又加水定容一次。 (2)用浓盐酸配制一定物质的量浓度的稀盐酸,量取浓盐酸时仰视读数。 (3)配制一定浓度的NaOH溶液时,称量的NaOH中混有Na2O。
(4)定容时仰视刻度线。
[学习小结]
[达标检测]
1.实验室用固体烧碱配制500 mL 0.1 mol·L―1的NaOH溶液。
(1)需称量________g的烧碱固体,它应该盛放在________中进行称量。 (2)配制过程中,不需要使用的仪器是(填写代号)________。 A.烧杯 B.量筒 C.1000 mL容量瓶 D.托盘天平
E.药匙 F.500 mL容量瓶 G.胶头滴管 H.漏斗 (3)除上述可使用的仪器,还缺少的仪器是_________,它在实验中的作用为
__________________________。 (4)叙述定容过程中的操作_______________________________________________。 (5)要配制浓度约为2 mol·L―1 NaOH溶液100 mL,下列操作正确的是________。 ①称取8 g NaOH固体,放入250 mL烧杯中,用100 mL量筒量取100 mL蒸馏水,
加入烧杯中,同时不断搅拌至固体溶解。
②称取8 g NaOH固体,放入100 mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL。
③称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加水至刻度线,塞好瓶塞,反复摇匀。
④用100 mL量筒量取40 mL 5 mol·L―1 NaOH,倒入250 mL烧杯中,再用同一量筒量取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中。
3.有三种不同浓度的稀硫酸、体积比为3:2:l,它们分别与等物质的量的K2CO3、KHC03、Al恰好完全反应。这三种硫酸的浓度之比是
A.1:l:l B.6:2:3 C.4:3:18 D.2:l:3
C级4.下列溶液中氯离子浓度与50mL 1mol/L氯化铝溶液中的氯离子浓度相等的是
A、150mL 1mol/L氯化钠溶液 B、75mL 2mol/L的氯化铵溶液
C、75mL 3mol/L的氯化钾溶液 D、75mL 1mol/L的氯化铁溶液
D级5.在硫酸铝、硫酸钾和明矾的混合溶液中,如果c(SO42-)=O.2 mol•L-1,当加等体积的O.2 mol•L-1的KOH溶液时,生成沉淀恰好溶解,则原混合物中K+的浓度是
A.0.2 mol•L-1 B.O.25 mol•L-1 C.O.45 mol•L-1 D.O.225 mol•L-1
知识点四:一定物质的量浓度溶液的配制
1.将标准状况下的aLHCl(气)溶于l000g水中,得到的盐酸密度为bg·cm-3,则该盐酸的物质的量浓度是
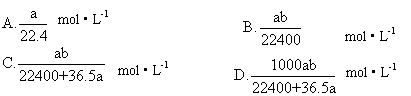
B级2.300mL某溶液的NaOH溶液中含有60g溶质。现欲配制lmol·L-1NaOH溶液,应
取原溶液与蒸馏水的体积比约为
A.1:4 B.1:5 C.2:l D.2:3
2.在同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为 ,物质的量之比为 ,原子总数之比为 ;质量之比为 ,密度之比为 。
C级3.(08海南)在两个密闭容器中,分别充有质量相同的甲乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小
D.甲的相对分子质量比乙的相对分子质量小
知识点三:物质的量浓度
A级 物质的量浓度的概念:___________________________________________________
3.气体摩尔体积的概念:______________________________________________
B级 1.下列有关气体的体积叙述正确的是
A、1mol任何气体的体积都约为22.4L
B、非标准状况下,1mol 任何气体的体积都不可能为22.4L
C、标准状况下,1molH2和1molH2O所占的体积都约为22.4L
D、在温度和压强相同的状况下,相同质量的一氧化碳和氮气体积相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com