
7.下列分子结构中,原子的最外层电子不能都满足8电子稳定结构的是
A.CH4 B.PCl3 C.CO2 D.BF3
[学习小结]
[达标检测]
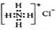 1.(09江苏卷2
1.(09江苏卷2 )下列有关化学用语使用正确的是
)下列有关化学用语使用正确的是
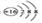 A. 硫原子的原子结构示意图:
B.NH4Cl的电子式:
A. 硫原子的原子结构示意图:
B.NH4Cl的电子式:
 C.原子核内有10个中子的氧原子:
C.原子核内有10个中子的氧原子:
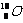
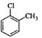
 D.对氯甲苯的结构简式:
D.对氯甲苯的结构简式:
5.关于化学键的下列叙述中,正确的是
A.离子化合物中可能含有共价键 B.共价化合物中可能含有离子键
C.离子化合物中只含离子键 D.共价键只能存在于化合物中
D级6.下列化合物中既存在离子键,又存在极性键的是
A.H2O B.NH4Cl C.NaOH D.Na2O2
3.下列所述性质中能证明化合物微粒间一定存在离子键的是
A.易溶于水 B.具有较高的熔点
C.熔融状态下能导电 D.溶于水能电离出离子
C级4.根据原子序数,下列各组原子能以离子键相结合的是
A.2与8 B.6与16 C.8与14 D.9与11
2.下列说法正确的是
A. 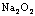 与
与 反应的过程中,同时有离子键、非极性键、极性键的断裂和生成
反应的过程中,同时有离子键、非极性键、极性键的断裂和生成
B. 1mol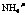 微粒中含有共价键数目的物质的量为3mol
微粒中含有共价键数目的物质的量为3mol
C. 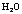 的沸点高于
的沸点高于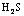 的沸点,是由于H-O共价键强于H-S共价键
的沸点,是由于H-O共价键强于H-S共价键
D. 离子化合物中一定含有金属元素
10.A、B、C、D四种元素在周期表中分别处于元素X的四周(如图)已知
元素X最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原
子半径是它们所处的同族元素中最小的。
(1)写出各元素的名称:A B C D X 。
(2)写出C、D、X气态氢化物最高价氧化物对应水化物的化学式,其酸性由强到弱的顺序为 。
(3)写出A、B、X气态氢化物的化学式,其稳定性由强到弱的顺序为 。
知识点三:化学键
|
键型 |
离子键 |
共价键 |
|
概念 |
|
|
|
成键微粒 |
|
|
|
形成条件 |
|
|
|
用电子式表示形成过程 |
|
|
A级
写出下列微粒或物质的电子式:
Al_________ Na+______ Cl-________ N2_________ CO2__________
H2O_________ NH3______ Na2O__________ KOH_________ MgCl2__________
NH4Cl____________ Na2O2____________ CCl4_____________
B级1.下列微粒的电子式书写正确的是
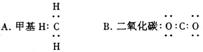
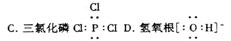
9.短周期的三种元素分别为X、Y和Z,已知X元素的原子最外层只有一个电子,Y元素原子的M电子层上的电子数是它的K层和L层电子总数的一半,Z元素原子的L电子层上电子数比Y元素原子的L电子层上的电子数少2个,则这三种元素所组成的化合物的分子式不可能是
|
|
B |
|
|
A |
X |
C |
|
|
D |
|
A.X2YZ4 B.XYZ3 C.X3YZ4 D.X4Y2Z7
8. (09山东卷11)元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是
(09山东卷11)元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是
A.同一元素不可能既表现金属性,又表现非金属性
 B.第三周期元素的最高正化合价等于它所处的主族序数
B.第三周期元素的最高正化合价等于它所处的主族序数
 C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
 D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
7.(09海南卷2)同一短周期的元素W、X、Y、Z的原子序数依次增加,下列叙述正确的是
A.单质的化学活泼性:W<X<Y<Z B.原子最外层电子数:W<X<Y<Z
C.单质的氧化能力:W<X<Y<Z D.元素的最高化合价:W<X<Y<Z
5.x、y为短周期元素,x原子K、L、M各电子层的电子数之比为1:4:1,它比y原子多3个电子,下列叙述正确的是
A.x离子半径大于y离子半径 B.x单质在空气中燃烧可生成两种化合物
C.x、y形成的化合物与浓硫酸共热可在烧瓶中进行
D.电解x、y形成的化合物的水溶液可得到y单质
D级6.(09北京卷7)W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
A.金属性:Y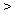 Z
B.氢化物的沸点:
Z
B.氢化物的沸点:
C.离子的还原性: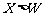 D.原子及离子半径:
D.原子及离子半径: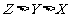
4.根据中学化学教材所附元素周期表判断,下列叙述不正确的是
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com