
3、原电池、电解池的工作原理,常见的电极反应、电池方程式书写
[学习指导]
探究、合作、交流、自主学习
[知识链接]
回忆必修二和选修四第一章、第四章相关内容
[学习内容]
知识点一: 化学反应中的能量变化
A级 1.化学反应的本质是什么?什么是放热反应?什么是吸热反应?常见的吸、放热反应有哪些?
2、运用盖斯定律进行反应热的计算
1、热化学方程式的含义
5、常见化学电源的种类及其工作原理
[重点难点]
4、能记住原电池、电解池的工作原理,写出常见的电极反应、电池方程式
3、能用盖斯定律进行反应热的计算
2、知道热化学方程式的含义
1、能说出化学能与热能、电能之间的相互转化,能记住吸热反应、放热反应、反应热(燃烧热、中和热)、原电池、电解池、电镀的概念
20.将N2和H2按一定比例混合,在相同状况下其密度是H2的3.6倍,取0.5mol该混合气体通入密闭容器内,使之发生反应,并在一定条件下达到平衡,已知反应达到平衡后容器内压强是相同条件下反应前压强的0.76倍。试求:
(1)反应前混合气体的N2和H2的体积比;
(2)达平衡时混合气体中氨的物质的量;
30.⑴用系统命名法命名下列烷烃:
其名称为: 。
⑵2001年诺贝尔化学奖获得者的研究内容与手性碳原子有关。在有机物分子中,若某个碳原子连接四个不同的原子或原子团,则这种碳原子称为“手性碳原子”;若同一个碳原子形成2个碳碳双键(如C=C=C)时,不能稳定存在。
现有链烃C7H10,在其众多的同分异构体中:
①处于同一平面上的碳原子最多有 (填字母代号)。
A.4个 B.5个 C.6个 D.7个
②含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的有5种,它们的结构简式除了以下三种外,还有 、 。
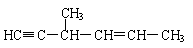


③含有“手性碳原子”,但与足量H2发生加成反应后,不再具有“手性碳原子”的同分异构体的结构简式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com