
18.(09宁夏卷 27)(15分)下图表示有关物
27)(15分)下图表示有关物
质(均由短周期元素形成)之间的转化关系,
其中A为常见的金属单质,B为非金属单质
(一般是黑色粉末),C是常见的无色无味液
体,D是淡黄色的固体化合物。(反应条件图
中已省略。)



 (1)A、B、C、D代表的物质分别为
(1)A、B、C、D代表的物质分别为
、 、 、
(填化学式);
 (2)反应①中的C、D均过量,该反应的化学方程式是
;
(2)反应①中的C、D均过量,该反应的化学方程式是
;
 (3)反应②中,若B与F物质的量之比为4∶3,G、H分别是 、 (填化学式);
(3)反应②中,若B与F物质的量之比为4∶3,G、H分别是 、 (填化学式);
 (4)反应③产物中K的化学式为
;
(4)反应③产物中K的化学式为
;
 (5)反应④的离子方程式为
。
(5)反应④的离子方程式为
。
17.某河道两旁有甲、乙两厂,它们排放的工业废水中,共含六种离子:K+、Fe3+、Ag+、
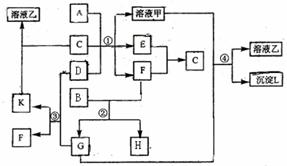
OH-、 NO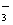 、Cl-。
、Cl-。
(1)甲厂的废水明显呈碱性,故甲厂废水中含有的三种离子是 、 、 。
(2)乙厂的废水中含有另外三种离子。如果加一定量 (选填:活性炭、硫酸亚铁、铁粉),可以回收其中的金属 (填写金属元素符号)。
 (3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的
(填写离子符号)转化为沉淀。经过滤后的废水主要含
,可用来浇灌农田。
(3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的
(填写离子符号)转化为沉淀。经过滤后的废水主要含
,可用来浇灌农田。
16.(09海南卷 15)(9分)
15)(9分) Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。
 请回答下列问题:
请回答下列问题:
 (1)电池的负极材料为
,发生的电极反应为
;
(1)电池的负极材料为
,发生的电极反应为
;
 (2)电池正极发生的电极反应为
;
(2)电池正极发生的电极反应为
;
 (3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是
,反应的化学方程式为
;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是
,反应的化学方程式为
;
 (4)组装该电池必须在无水、无氧的条件下进行,原因是
。
(4)组装该电池必须在无水、无氧的条件下进行,原因是
。
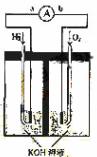
15.(09天津卷 10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
 (1)氢氧燃料电池的能量转化主要形式是 ,在导线中
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中
电子流动方向为
 (用a、b 表示)。
(用a、b 表示)。
 (2)负极反应式为 。
(2)负极反应式为 。
 (3)电极表面镀铂粉的原因为
。
(3)电极表面镀铂粉的原因为
。
 (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
 Ⅰ.2Li+H2
Ⅰ.2Li+H2
 2LiH
2LiH Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
 ①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
 ②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
 ③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
14.呼吸面具中Na2O2可吸收CO2放出O2,若用超氧化钾(KO2)代替Na2O2也可起到同样的作用。
(1)写出K02与CO2的反应方程式
(2)lkgNa2O2和lkgKO2,分别和CO2反应,生成的O2体积比(同温同压下)为 。
 (3)等物质的量的CO2分别与足量的Na2O2,KO2反应生成的O2体积比(同温同压下)为 。
(3)等物质的量的CO2分别与足量的Na2O2,KO2反应生成的O2体积比(同温同压下)为 。
(4)你认为选用 作补氧剂更为合适,理由是
13.(09浙江卷 10)已知:25°C时,
10)已知:25°C时, ,
,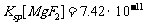 。下列说法正确的是
。下列说法正确的是
 A.25°C时,饱和
A.25°C时,饱和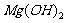 溶液与饱和
溶液与饱和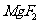 溶液相比,前者的
溶液相比,前者的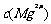 大
大
 B.25°C时,在
B.25°C时,在 的悬浊液加入少量的
的悬浊液加入少量的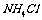 固体,
固体,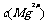 增大
增大
 C.25°C时,
C.25°C时,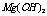 固体在20mL0.01 mol·
固体在20mL0.01 mol· 氨水中的
氨水中的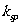 比在20mL0.01mol·
比在20mL0.01mol·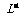
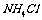 溶液中的
溶液中的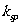 小
小
 D.25°C时,在
D.25°C时,在 的悬浊液加入少量的NaOH固体,
的悬浊液加入少量的NaOH固体,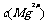 减小
减小
12.(09江苏卷 5)化学在生产和日常生活中有着重要的应用。下列说法不正确的是
5)化学在生产和日常生活中有着重要的应用。下列说法不正确的是
 A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
 B. 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
B. 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
 C.
C. 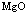 的熔点很高,可用于制作耐高温材料
的熔点很高,可用于制作耐高温材料
 D. 电解
D. 电解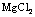 饱和溶液,可制得金属镁
饱和溶液,可制得金属镁
11.重金属离子有毒性。实验室有甲、乙两种废液,均有一定毒性。甲废液经化验呈碱性,主要有毒离子为Ba2+,如将甲、乙两废液按一定比例混合,毒性明显降低。乙废液中可能含有的离子是
A.Cu2+和SO42- B.Cu2+和Cl- C.K+和SO42- D.Ag+和NO3-
10.已知铍(Be)的原子序数为4。下列对铍及其化合物的叙述中,正确的是
A.铍的原子半径小于硼的原子半径 B.氯化铍分子中铍原子的最外层电子数是8
C.氢氧化铍的碱性比氢氧化钙弱 D.单质铍跟冷水反应产生氢气
9.将钠、镁、铝各0.3mol分别放入 足量盐酸中,同温同压下产生气体的体积比是
A.1∶2∶3 B.6∶3∶2 C.3∶1∶1 D.1∶1∶1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com