
3.甲烷和氢气燃烧的热化学方程式分别如下:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1 ,2H2(g)
+O2(g)==2H2O(g)△H2, 2H2(g)+O2(g)=2H2O(l)△H3 常温下取体积为4:1的甲烷和氢气混合
气体11.2L(标况),完全燃烧后恢复常温,放出热量为
A.0.4△H1+0.05△H3 B.0.4△H1+0.05△H2 C.0.4△H1+0.1△H3 D.0.4△H1+0.2△H3
2.下列关于燃料充分燃烧的说法,不正确的是
A.空气量越多越好 B.应通入适量空气
C.固体燃料燃烧前要粉碎 D.液体燃料燃烧时可以以雾状喷出
1.石油、煤、天然气等在地球上的蕴藏量是有限的,为缓解能源危机:①可以利用电解水的方法得到氢
气做能源;②可用酒精做能源;③砍伐树木做能源;④应开发太阳能、核能等新能源。上述说法正确的是
A. 只有① B. ①和④ C. ②和④ D. ④
30.⑴用系统命名法命名下列烷烃:
其名称为: 。
⑵2001年诺贝尔化学奖获得者的研究内容与手性碳原子有关。在有机物分子中,若某个碳原子连接四个不同的原子或原子团,则这种碳原子称为“手性碳原子”;若同一个碳原子形成2个碳碳双键(如C=C=C)时,不能稳定存在。
现有链烃C7H10,在其众多的同分异构体中:
①处于同一平面上的碳原子最多有 (填字母代号)。
A.4个 B.5个 C.6个 D.7个
②含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的有5种,它们的结构简式除了以下三种外,还有 、 。
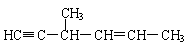
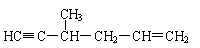
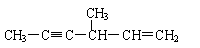
③含有“手性碳原子”,但与足量H2发生加成反应后,不再具有“手性碳原子”的同
分异构体的结构简式是 。
29.(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准)。
|
烯类化合物 |
相对速率 |
|
(CH3)2C=CHCH3 |
10.4 |
|
CH3CH=CH2 |
2.03 |
|
CH2=CH2 |
1.00 |
|
CH2=CHBr |
0.04 |
据表中数据,总结烯类化合物加溴时,反应速率与C=C上取代基的种类、个数间的关系:
①_______________________②_ ③ __。
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是______________(填代号)。
A.(CH3)2C=C(CH3) 2 B.CH3CH=CH CH3
 C.CH2=CH2
D.CH2=CHCl
C.CH2=CH2
D.CH2=CHCl
28.已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
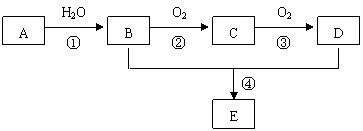
请回答下列问题:
(1)写出A的结构简式 。
(2)B、D分子中的官能团名称分别是 、 。
(3)物质B可以被直接氧化为D,需要加入的试剂是 。
(4)写出下列反应的化学方程式:
① ;
反应类型: 。
④反应类型: 。
27. 近年来用合成方法制备了多种新奇的有机物, 例如分子具有如图所示立体结构的环状化合物. 有人认为下述有机物中, ①立方烷、棱晶烷可以看作是烷烃的同系物;②盆烯是单烯烃; ③棱晶烷、盆烯是苯的同分异构体.上述看法正确的是
A. ①②③ B. 除①外都正确 C. 只有① D. 只有③

26. 据报道,1995年化学家合成了一种分子式为C200H200的含多个碳碳叁键的链状烃,其分子中含碳碳叁键最多可以是
A.49个 B.50个 C.51个 D.100个
25.一定体积的甲烷在一定量O2中燃烧后得到的产物为CO、CO2和水蒸气,测得混合气体的质量为49.6g ,将混合气体缓慢经过无水CaCl2时,CaCl2增重25.2g,则原混合气体中CO2的质量为
A.12.5 g B.13.2g C.19.7g D.24.4g
24.现有一组可能由CH4、NH3、、H2、CO、CO2 和HCl组成的无色混合气体,善思的李聪进行了以下实验:①将此混合气体通过浓硫酸,②再通过过量的澄清石灰水,③剩余气体经干燥后可在氧气中燃烧。得到的实验现象依次为:①中气体总体积基本不变,②中未见浑浊,但气体体积减少,③中燃烧产物不能使无水硫酸铜变色。据此确定原混合气体的组成为
A.CO和HCl B.CH4和NH3 C.CH4和HCl、 D.H2和CO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com