
6. 有学者认为:偌大的清帝国不亡于洪、杨,而亡于孙文,原因之一是如图的三把利剑,三剑一击,清王朝就玩完了。其史论、史观和史料反映出
①三民主义基本符合当时中国社会发展的趋势
②英雄创造历史
③民族矛盾非常突出
④领导阶级的先进与否,是革命事业成功的关键因素之一
A.①②③④ B.①②③ C.①③④ D.①②④
5. 洪仁玕在太平天国运动失败后的“供词”中说:“我朝祸害之源,即洋人助妖之事……如洋人不助敌军,则吾人断可长久支持。”对此理解准确的是
A.谴责列强干涉中国内政 B.推卸失败的责任
 C.正确总结了失败的主观原因 D.正确总结了失败的客观原因
C.正确总结了失败的主观原因 D.正确总结了失败的客观原因
4. 《上海县竹枝词》有诗云:“卅年求富更求强,造炮成船法仿洋。海面未收功一战,总归虚牝掷金黄。”与上述内容有关的历史事件是
A.第二次鸦片战争 B.中法马尾海战
C.中日甲午战争 D.八国联军侵华
3. 某地边疆危机,消息上报朝廷后,皇帝一方面交待兵部尽速调兵迎敌;另一方面责成户部尽速调度粮草,备部队急用。幕僚根据皇帝旨意,草拟诏书,经皇帝确认无误后,直
接送至兵部、户部等单位执行。这一现象发生在
A.秦朝 B.唐朝 C.宋朝 D.明朝
2. 一考古队在某地发掘出古代石刻石碑一块,石碑上刻有:“追念乱世,分土建邦,乃
今皇帝,一家天下,兵不复起。”这块石碑应属于下列哪个朝代
A.秦朝 B.汉朝 C.隋朝 D.元朝
1. “先王之法,立天子不使诸侯疑(拟)焉,立诸侯不使大夫疑(拟)焉,立嫡子不使庶孽疑(拟)焉。疑(拟)生争,争生乱。是故诸侯失位则天下乱,大夫无等则朝廷乱。”这表明西周嫡长子继承制的目的是
A.确立嫡长子的最高地位
B.防止内部纷争,强化君主专制
C.解决权位和财产的继承与分配,稳定统治秩序
D.保证贵族血统的纯正
26.(7分)美国计划2015年再次登陆月球,继而在月球上建立基地,给人类登陆火星作准备。为了早日实现梦想,1992年美国进行了第一次利用实际的月球岩石――玄武岩(FeTiO3,钛酸亚铁)来制造氧气的试验。已知FeTiO3被H2还原后,生成Fe、TiO2和水,被C还原后生成Fe、TiO2和CO2。请参与探究,并回答下列问题:
Ⅰ.理论分析
(1)写出FeTiO3在加热时被H2还原的化学方程式: 。该反应中氧化剂为 ,氧化产物为 。
Ⅱ.实验探究
为了测定钛铁矿中可提取氧的质量分数,某研究性学习小组分别设计了以下两套实验装置:
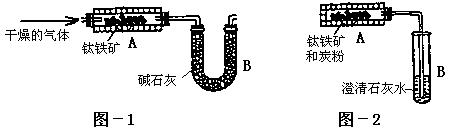
(2)学生甲设想用图-1装置(A为电加热装置)从钛铁矿中提取氧,请写出最简便的实验步骤:__________________________(选填下列数字编号)。
①通入N2;②停止通N2;③通入H2;④停止通H2;⑤加热;⑥停止加热;⑦称取装置B的质量。
(3)学生乙设想用图-2装置(A为电加热装置)从钛铁矿中提取氧,并且认为该方案的意义在于:反应产生的CO2可通过绿色植物的光合作用转化为营养物质,同时产生氧气:6CO2+6H2O
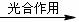 C6H12O6(葡萄糖)+6O2。实验过程中,称得反应前装置A中钛铁矿的质量为ag,炭粉的质量为bg,反应后装置B中产生CaCO3的质量为cg,则钛铁矿中可提取氧的质量分数的表达式为:_______________________。
C6H12O6(葡萄糖)+6O2。实验过程中,称得反应前装置A中钛铁矿的质量为ag,炭粉的质量为bg,反应后装置B中产生CaCO3的质量为cg,则钛铁矿中可提取氧的质量分数的表达式为:_______________________。
(4)经专家评审后,认定两个方案都很有意义,但实验设计方面还存在不足之处,例如图-2装置在加热时,生成的CO2不可能全部被澄清石灰水吸收,同时钛铁矿和炭粉在加热时还会产生CO,给实验带来误差。请提出对图-2所示装置应采取的改进措施:_______________________。改进后,实验自始至终需持续向图-2装置A中通入N2的目的是__________________________。
贵州省兴义市精华中学2010届高三第一次月考
25.(7分)某钠盐溶液可能含有阴离子NO3-、CO32-、SO32-、SO42-、Cl-、
Br-、I-。为了鉴别这些离子,分别取少量溶液进行以下实验:
①所得溶液呈碱性;
②加HCl后,生成无色无味的气体。该气体能使饱和石灰水变浑浊。
③加CCl4,滴加少量氯水,振荡后,CCl4层未变色。
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量的盐酸,沉淀不能完全溶解。
⑤加HNO3酸化后,再加过量的AgNO3,溶液中析出白色沉淀。
(1)分析上述实验①,写出这一实验鉴定离子的结论与理由。
_______________________________________ 。
(2)由以上5个实验分析一定存在的离子是: 。
(3)上述5个实验不能确定是否的离子是___________________。
24.(13分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e→NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:__________________________________________________________________
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生0.2mol气体,则转移电子的总数是 ;反应中被还原的硝酸的物质的量是 ;消耗的Cu2O质量是 。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是______________________________________。
23.(8分)砷酸铅可用作杀虫剂。已知①在砷酸铅中,砷处于最高价态,铅处于稳定价态;②砷酸铅是正砷酸对应的盐,1 mol正砷酸分子中含有8 mol原子。请回答以下问题:
(1)砷的元素符号是_____________。
(2)砷的最高价氧化物的化学式为_______________;铅的最高价氧化物的化学式为________________。
(3)砷酸铅的化学式为___________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com