
5.在数列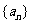 中,
中,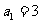 ,
,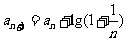 ,则
,则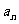 =
=
A.3+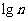 B.
B.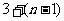 C.
C.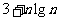 D.2+
D.2+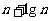
4.若函数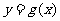 的图像与函数
的图像与函数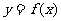 的图像关于直线
的图像关于直线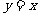 对称,则函数
对称,则函数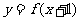 的反函数是
的反函数是
A.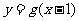 B.
B.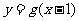
C.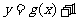 D.
D.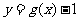
3.设 的内角A、B、C所对的边长分别为a、b、c,且
的内角A、B、C所对的边长分别为a、b、c,且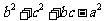 =0,则角
=0,则角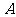 等于
等于
A. B.
B.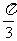 C.
C.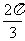 D.
D.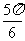
2.已知函数 的最大值为M,最小值为m,则
的最大值为M,最小值为m,则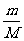 的值为
的值为
A.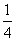 B.
B.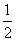 C.
C.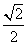 D.
D.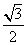
1.定义集合运算: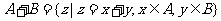 ,设
,设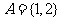 ,
,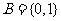 则集合
则集合 的所有元素之和为
的所有元素之和为
A.4 B.6 C.7 D.8
28.(本小题满分11分)
某无色透明溶液X中可能存在如下几种离子: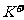 、
、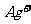 、
、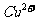 、
、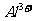 、
、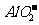 、
、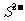 、
、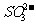 、
、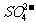 ,现取该溶液进行有关实验,结果如下
,现取该溶液进行有关实验,结果如下
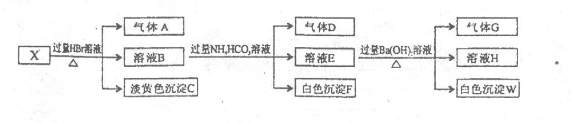
(1)沉淀C是 ,写出生成沉淀C的离子方程式 ;
(2)写出由溶液B生成气体D和沉淀F的离子方程式 ;
(3)气体A是 或 ;
(4)沉淀w中肯定有 ,可能有 ;
(5)溶液X中肯定含有离子有 。


27. (10分)
(10分)
如右下图所示,“中和热的测定”实验步骤如下
①准备反应装置如图;
②用一个量筒量取50mL0.5mol·L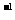 盐酸,倒入
盐酸,倒入
小烧杯中,并用温度计测量盐酸的温度,记录。
然后把温度计上的酸用水冲洗干净;
③用另一个量筒量取50mL0.55mol·L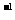
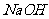 溶液,并用温度计测量
溶液,并用温度计测量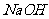 溶液的温度,记录;
溶液的温度,记录;
④把量筒中的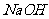 溶液一次倒入小烧杯(注意不要洒到外面),轻轻搅动溶液,并准确读取混合溶液的最高温度。
溶液一次倒入小烧杯(注意不要洒到外面),轻轻搅动溶液,并准确读取混合溶液的最高温度。
⑤……
⑥根据实验数据取平均值计算中和热。
请回答下列问题:
(1)从装置图中看,尚缺少一种玻璃仪器是 。
(2)补上第⑤步 。
(3)第②步如果冲洗时把冲洗液直接倒入烧杯中,则测得的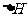 (选填“偏大”、“偏小”或“无影响”),如果不将温度计冲洗干净就去量
(选填“偏大”、“偏小”或“无影响”),如果不将温度计冲洗干净就去量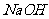 溶液的温度,则测得的
溶液的温度,则测得的
(选填“偏大”、“偏小”或“无影响”)。
(4) (选填“能”或“不能”)直接用浓硫酸代替50mL 0.50mol·L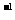 盐酸。
盐酸。
(选填“能”或“不能”)直接用浓硫酸代替50mL0.50mol·L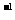 醋酸代替盐酸。
醋酸代替盐酸。
(5)近似认为50mL0.50mol·L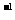 盐酸和50
盐酸和50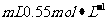
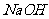 溶液的密度都是1g·
溶液的密度都是1g·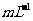 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容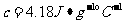 ,起始平均温度为20.4
,起始平均温度为20.4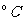 ,反应后最高温度平均值为23.8
,反应后最高温度平均值为23.8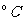 ,则中和热
,则中和热 H=
。
H=
。
(6)若改用60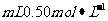 盐酸和50
盐酸和50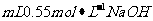 溶液进行实验,与原实验相比,所放出的热量 (选填“增多”“相同”或“减少”),所测得的
溶液进行实验,与原实验相比,所放出的热量 (选填“增多”“相同”或“减少”),所测得的 H值
H值
(选填“相等”或“不等”)
26.(12分)
如图所示,接通电源电解10min钟后,a极上增重12.8g。
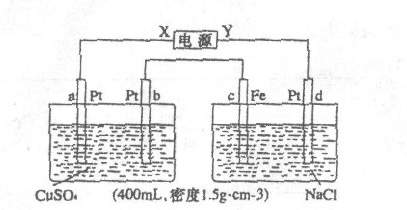
(1)写出电极名称:X ,C 。
(2)写出电极反应式:b c
(3)写出电解离子方程式:甲
乙
(4)要使乙中溶液复原应加入 (填物质名称) mol
(5)电解后忽略溶液体积的变化甲中溶液的pH= 。甲中硫酸的质量分数为 。
25.(本小题满分8分)
(1)请将5种物质: 哦、
哦、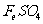 、
、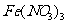 、
、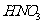 和
和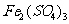 分别填入下面对应的横线上,组成一个未配平的化学方程式。
分别填入下面对应的横线上,组成一个未配平的化学方程式。
+
→
+
+
+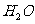
(2)反应物中发生氧化反应的物质是 被还原的元素是
(3)反应中1mol氧化剂 (填“得到”或“失去”) mol电子。
(4)请将反应物的化学式及配平后的化学计量数填入下列相应的位置中:
□ +□ →
24. (本小题满分7分)
制备氢氧化铁胶体的相关性质实验,回答下列问题。
(1)取一个烧杯,加入20mL蒸馏水,加热至沸腾,然后向废水中滴加 1mL~2mL,继续煮沸,待
后,停止加热,即制得的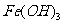 胶体,反应方程式为
胶体,反应方程式为
。
(2)在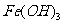 胶体中,逐滴加入HI稀溶液,会出现一系列变化。
胶体中,逐滴加入HI稀溶液,会出现一系列变化。
①先出现红褐色沉淀,原因是 ;
②随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式 ;
③ 最后溶液颜色加深,此反应的离子方程式是 ;
④用稀盐酸代替HI稀溶液,能出线上述那些相同的变化现象 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com