
7.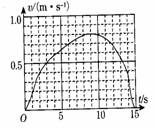 利用速度传感器与计算机组合,可以自动作出物体运动的图像,某同学在一次实验中得到的运动小车的v-t图像如图所示,由此即可以知道( )
利用速度传感器与计算机组合,可以自动作出物体运动的图像,某同学在一次实验中得到的运动小车的v-t图像如图所示,由此即可以知道( )
A.小车先做加速运动,后做减速运动
B.小车运动的最大速度约为0.8m/s
C.小车的最大位移为6m
|
|
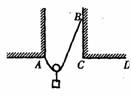 8.如图所示,将一根不可伸长的、柔软的轻绳左、右两端分别系于A, B两点上,一物体用动滑轮悬挂在轻绳上,达到平衡时,两段绳子间的夹角为θ1,绳子张力为F1;将绳子右端移至C点,待系统达到平衡时,两段绳子间的夹角为θ2,绳子张力为F2;将绳子右端再由C点移至D点,待系统达到平衡时,两段绳子间的夹角为θ3,绳子张力为F3,不计摩擦,并且BC为竖直线,则
8.如图所示,将一根不可伸长的、柔软的轻绳左、右两端分别系于A, B两点上,一物体用动滑轮悬挂在轻绳上,达到平衡时,两段绳子间的夹角为θ1,绳子张力为F1;将绳子右端移至C点,待系统达到平衡时,两段绳子间的夹角为θ2,绳子张力为F2;将绳子右端再由C点移至D点,待系统达到平衡时,两段绳子间的夹角为θ3,绳子张力为F3,不计摩擦,并且BC为竖直线,则
A. θ1=θ2<θ3, B.θ1=θ2=θ3 C. Fl>F2>F3 D.Fl=F2=F3
第Ⅱ卷(非选择题60分)
6.竖直放置在水平面上的轻质弹簧上放着质量为2kg的物体A,处于静止状态。若将一个质量为3kg的物体B竖直向下轻放在A上的一瞬间,则A与B之间的作用力大小为(取g=10m/s2)( )
A.30N B.0 C.15N D.12N
4.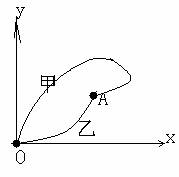 甲、乙两小分队进行代号为“猎狐”的军事演习,指挥部通过现代通讯设备,在屏幕上观察到两小分队的行军路线如图所示。两小分队同时从同一处O出发,最后同时捕“狐”于A点,则( )
甲、乙两小分队进行代号为“猎狐”的军事演习,指挥部通过现代通讯设备,在屏幕上观察到两小分队的行军路线如图所示。两小分队同时从同一处O出发,最后同时捕“狐”于A点,则( )
A.两队行军路程 >
>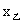
B.两队行军位移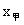 >
>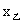
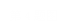 C.两队平均速度
C.两队平均速度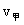 =
=
D.两队平均速度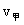 >
>
|
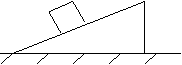 5.如图所示,物体A在斜面上与斜面一起水平向左做匀加速直线运动,关于物体A受力情况下列说法正确的是:( )
5.如图所示,物体A在斜面上与斜面一起水平向左做匀加速直线运动,关于物体A受力情况下列说法正确的是:( )
A. 物体A一定受三个力的作用
|
C. 物体A所受到的合外力的方向一定水平向左
D.物体A对斜面作用力的方向一定垂直斜面向下
3.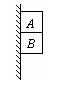 如图A、B两物体叠放在一起,用手托住,让它们静靠在竖直墙边,然后释放,它们同时沿墙面向下滑,已知mA>mB,则物体B ( )
如图A、B两物体叠放在一起,用手托住,让它们静靠在竖直墙边,然后释放,它们同时沿墙面向下滑,已知mA>mB,则物体B ( )
A.只受一个重力
B.受到重力和一个摩擦力
|
D.受到重力、一个摩擦力和两个弹力
2. 如图所示,2008北京奥运会上中国举重选手曹磊毫无悬念地以总成绩282kg轻取金牌。
赛前曹磊在一次抓举训练中举起125kg的杠铃时,两臂成120°,此时曹磊沿手臂向上撑的力F及曹磊对地面的压力N的大小分别是(假设她的体重为75kg,g取10m/s2)( )
如图所示,2008北京奥运会上中国举重选手曹磊毫无悬念地以总成绩282kg轻取金牌。
赛前曹磊在一次抓举训练中举起125kg的杠铃时,两臂成120°,此时曹磊沿手臂向上撑的力F及曹磊对地面的压力N的大小分别是(假设她的体重为75kg,g取10m/s2)( )
A.F =1250N N =2000N B.F =1250N N =3250N
|
1.关于自由落体运动,下列说法正确的是( )
A.物体竖直向下的运动就是自由落体运动
B.加速度等于重力加速度的运动就是自由落体运动
C.在自由落体运动过程中.不同质量的物体运动规律相同
D.物体做自由落体运动位移与时间成反比
20、(20分)实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液。 应量取盐酸体积________mL ,应选用容量瓶的规格________mL。 除容量瓶外还需要的其它仪器___________________________。
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)________________
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(3) 操作A中,将洗涤液都移入容量瓶,其目的是_______________________________。
溶液注入容量瓶前需恢复到室温,这是因为__________________________________。
(4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响)?
a.没有进行A操作___________ ; b.加蒸馏水时不慎超过了刻度______________ ;
c.定容时俯视________________。
(5)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度 ?__________________
21(12分)(1)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e- → NO+2 H2O
在下列四种物质KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质(甲)中滴加少量稀硝酸能使上述还原过程发生。
① 写出并配平该氧化还原反应的方程式, 用双线桥标出电子转移的方向和数目
②被还原的元素______,还原剂是 。
③反应生成0.3mol H2O,则转移电子的数目为 个。
(2)向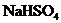 溶液中,逐滴加入
溶液中,逐滴加入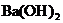 溶液至中性,写出发生反应的离子方程式:___________________________
_________.
溶液至中性,写出发生反应的离子方程式:___________________________
_________.
在以上中性溶液中,继续滴加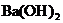 溶液,写出此步反应的离子方程式:
溶液,写出此步反应的离子方程式:
________________________________________.
22(4分)(1)向25mL 2mol·L-1稀硫酸中加入25mL 1mol·L-1的BaCl2溶液,充分反应后,溶液中H+物质的量浓度为(设稀溶液相混后总体积为原分体积之和) mol/L
(2)质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水.得到的溶液每毫升质量为q g,物质的量浓度为c.则溶质的相对分子质量为 。
班级 姓名 考号 考场
19.(10分)储氢纳米碳管的研制成功体现了科技的进步。用电孤法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应中的反应物和生成物有C、CO2、H2SO4 、K2Cr2O7 、K2SO4、Cr2(SO4)3 、H2O七种物质。
(1)请用上述物质填空,并配平化学方程式:
□C+□ H2SO4 →□ +□ +□Cr2(SO4)3 +□H2O
(2)上述反应中氧化剂是(填化学式) 。被氧化的元素是(填元素符号) 。 (3)H2SO4在上述反应中表现出来的性质是(填选项编号)___________。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为 。
18.用NA表示阿伏加德罗常数,下列说法正确的是( )
①18g D2O含有的电子数为10NA ②同温、同压下,相同体积的氧气和氩气所含的原子数相等
③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA④在标准状况下,22.4LSO3的物质的量为1mol⑤100℃时6.72L的水所含的原子总数为0.9NA⑥0.1molOH-含0.1NA个电子⑦1mol Na2O2与水完全反应时转移电子数为2NA
A.③⑤⑥⑦ B.③⑤ C.①②④⑦ D.③④⑤⑥
第Ⅱ卷(非选择题 共46分)
17.将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为
( )
A.NO2 B.N2O2 C.N2O D.N2O4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com