
22.(17分)
(1)(4分)电磁打点计时器接“6V,50HZ”交流电源,它的打点周期是 s。现在用它研究匀变速直线运动,通过打点的纸带测出物体的加速度,但实验时电路中交流电的频率低于50HZ,而在实验过程中仍按频率等于50Hz进行计算,则计算出的加速度值比物体实际的加速度值将 (填“偏大” 、“偏小”或“不变”)
(2)(4分)如图是打点计时器打出的纸带,图中A、B、C、D、E、F等是按时间顺序先后打出的记数点(每两个计数点间有三个实验点未画出)。用刻度尺量出AB、EF之间距离分别为2.40cm和0.84cm,那么小车的加速度大小是 m/s2(结果保留两位有效数字),方向是 。(填“水平向左”或“水平向右”)

(3)(9分)在研究性学习中,某同学设计了一个测量导电纸的导电膜厚度的实验,该同学从资料上查得导电纸导电膜导电材料的电阻率为ρ,并利用下列器材完成了这个实验:
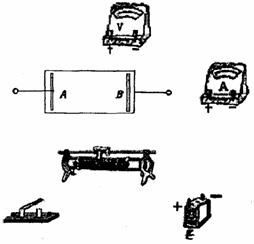 A.电源E(电动势为12V,内阻不计)
A.电源E(电动势为12V,内阻不计)
B.木板N(板上放有导电纸一张,导电膜
向上),两个金属条A、B(平行放置
在导电纸上,与导电纸接触良好,用
作电极).
C.滑线变阻器R(其总阻值小于两平行电
极间导电纸的电阻).
D.毫米刻度尺.
E.电压表V(量程为6V,内阻约3kΩ)
F.电流表A(量程为0.6A,内阻忽略不计)
G.开关K,导线若干。
①.请在图示实物图中完成实物连线。
②.实验中应测定的物理量是: 。
③.计算导电膜厚度h的公式是: 。(用ρ和测得物理量的符号表示)
21.如图所示,水平面上的轻弹簧一端与物体相连,另一端
固定在端上P点,已知物体的质量为m=2.0kg,物体
与水平面问的动摩擦因数μ=0.4,弹簧的劲度系数
k=200N/m现用力F拉物体,使弹簧从处于自然状态
的O点由静止开始向左移动10cm,这时弹簧具有弹性势能Ep=1.0J,物体处于静止状态。若取g=10m/s,则撤去外力F后 ( )
A.物体回到O点时速度最大
B.物体向右滑动的距离可以达到12.5cm
C.物体向右滑动的距离一定小于12.5cm
D.物体到达最右端时动能为0,系统机械能不为0
第Ⅱ卷(非选择题,共174分)
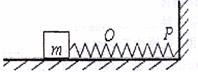
20.图中的实线表示电场线,虚线表示只受电场力作用的带
正电粒子的运动轨迹,粒子先经过M点,再经过N点,
可以判定 ( )
A.M氧的电势低于N点的电势
B.M点的电场强度大丁N点的电场强度
C.粒子在M点具有的电势能大于在N点具有的电势能
 D.粒子在M点受到的电场力大于在N点受到的电场力
D.粒子在M点受到的电场力大于在N点受到的电场力
19.一列简谐横波沿x轴正方向传播,振幅为A.t=0时,平衡位置在x=0处的质元位于y=0处,且向y轴负方向运动;此时,平衡位置在x=0.15m处的质元位于y=A处,该波的波长可能等于 ( )
 A.0.60m B.0.20m C.0.12m D.0.086m
A.0.60m B.0.20m C.0.12m D.0.086m
16.一定质量的气体经历-缓慢的绝热膨胀过程。设气体分子间的势能可忽略,则在此过程中 ( )
A.外界对气体做功,气体分子的平均动能增加
B.气体对外界做功,气体分子的平均动能增加
C.外界对气体做功,气体分子的平均动能减少
D.气体对外界做功,气体分子的平均动能臧少
 17.如图所示,一物体自倾角为θ的固定斜面顶端沿水平方向抛出后落在斜面上,物体与斜面接触时速度与水平方向的夹角
17.如图所示,一物体自倾角为θ的固定斜面顶端沿水平方向抛出后落在斜面上,物体与斜面接触时速度与水平方向的夹角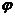 满足 ( )
满足 ( )
A.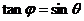 B.
B.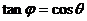
C.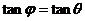 D.
D.
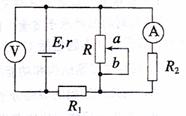 18.电动势为E、内阻为r的电源与定值电阻R1、R2及滑动变阻器R连接成如剧所示的电路,当滑动变阻器的触头由中点滑向b端时,下列说法正确的是 ( )
18.电动势为E、内阻为r的电源与定值电阻R1、R2及滑动变阻器R连接成如剧所示的电路,当滑动变阻器的触头由中点滑向b端时,下列说法正确的是 ( )
A.电压表和电流表读数都增大
B.电压表和电流表读数都减小
C.电压表读数增大,电流表读数减小
D.电压表读数减小,电流表读数增大
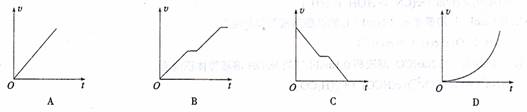
15.如图是一娱乐场的喷水滑梯,若忽略摩擦力,人从滑梯
顶端滑下直到入水前,速度大小随时间变化的关系最接
近图 ( )
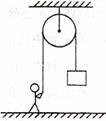
14.建筑工人用图所示的定滑轮装置运送建筑材料。质量为70kg的
工人站在地面上,通过定滑轮将20.0kg的建筑材料以0.5m/s。
的加述度拉升,忽略绳子和定滑轮的质量及定滑轮的摩擦,则
工人对地面的压力大小为(g取10m/s2) ( )
A.510N B.490N
 C.890N D.910N
C.890N D.910N
13.在下列条件下,一定能大量共存的离子组是 ( )
A.在硫酸铝溶液中 Na+、NH+4、HCO-3、Mg2+
B.在水电离出的c(H+)=1×l0-13mol L-1的溶液中:Na+、NH+4、NO-3、CH3COO-
C.含有大量Fe2+的溶液:Na+、Mg2+、NO-3、SO2-4
D.在c(H+)/c(OH-)的比值为1014的溶液:K+、I-、SO2-3、S2-
 二、选择题(本题共8小题。在每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选剥的得6分,选对但不全的得3分,有选错的得0分)
二、选择题(本题共8小题。在每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选剥的得6分,选对但不全的得3分,有选错的得0分)
12.下列离子反应方程式正确的是 ( )
①四氧化三铁溶于稀硝酸中:Fe3O4+8H+=2Fe3++Fe2++4H2O
②将过量SO2气体通入氨水中:SO2+NH3·H2O==NH+4+HSO-3
|
③两极均用铁屯报电解饱和食盐水:2Cl-+2H2O====2OH-+H2↑+Cl2↑
④向醋酸溶液中滴加少量碳酸氢钠溶液
H++HCO-3 ==H2O+ CO2↑
⑤制铁发生吸氧腐蚀正极的电极反应:2H2O+O2+4e-=4OH-
⑥硝酸铁溶液中滴加足量HI溶液:
Fe3++3NO-3+12H++10I-=Fe2++5I2+3NO↑+6H2O
A.②⑤⑥ B.①②③⑤ C.①②④⑥ D.②③④⑤⑥
11. 在高温和催化剂存在下,向容积为2 L的密闭容器甲加入0 2molCO和0.2 mol H2O,发生如下反应CO(g)+H2O(g) CO2(g)+H2(g),△H=-akJ/tool(a>0)。
在高温和催化剂存在下,向容积为2 L的密闭容器甲加入0 2molCO和0.2 mol H2O,发生如下反应CO(g)+H2O(g) CO2(g)+H2(g),△H=-akJ/tool(a>0)。
反应达到平衡后,测得c(CO):c(CO2)=3:2。下列说法正确的是 ( )
A.反应放出的热量为0.2a kJ
B.若升高温度,v(正)减慢,v(逆)加快,平衡逆向移动
C.若将容器的体积压缩为1L,H2的体积分数变为40%
D.平衡时H2O的转化率为40%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com