
4-1.试确定该晶胞的碳原子个数。
4-2.写出晶胞内各碳的原子坐标。
4-3.已知石墨的层间距为 334.8 pm,C-C键长为 142 pm,计算石墨晶体的密度。
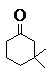 ;
;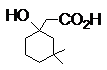 ;
; 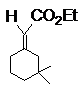 ;
;
A B C
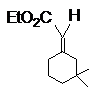 ;
; 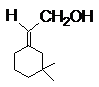 ;
;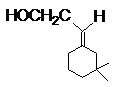 ;
;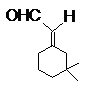
D E G H
评分标准:
1. 每个结构式或结构简式2分,共14分,有错不给分。
* 注:C和D在LiAlH4作用下可分别生成E和G,但也有可能分别生成单环萜烷醇。本题只要求写出E和D, 若选手应答时写出在写出E和D的同时写出单环萜烷醇,不扣分。
第七题:
(1)将8´式(2)+9´式(3)-式(1)得
8C(石墨)+9H2(g)→C8H18(g)
DrHmy= 8D2Hmy+9D3Hmy-D1Hmy = –207.8 kJ·mol–1
DrSmy= SnBSmy (B) = –757.252J·K-1·mol–1
DrGmy = DrHmy - T´DrSmy = 17.861kJ·mol–1
Kpy = exp(–DrGmy/RT) = 7.36´10–4
(2)∵ Kx=Kpy (p/py)–Dn,Dn= –8
当压力不高时,Kpy为常数,Kx随总压的增加而增大,故有利于正辛烷的生成。
(3) DrHmy<0,Kpy随温度升高而减小,
∴ 升高温度不利于正辛烷的生成。
(4)若x(C8H18)=0.1,
则Qp=[p(C8H18)/py] / [p(H2)/py]9=0.258>>Kpy=7.36´10-4
故x(C8H18)不能达到0.1
(5)若使x(C8H18)=0.5,
Kpy=Kx(p/py)-8=7.36´10-4
求得p=499 kPa
以上每小题各2分
第八题
(1) 根据上述实验事实,设反应的实验速率方程为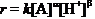 ,
,
由于在缓冲溶液中反应,[H+] 为常数,故可简化上式为:
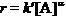 ,
,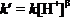
令a=1,可得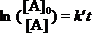 , (3分)
, (3分)
又[A]0µP¥ ,[A]µP¥-P,且温度一定,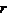 比例系数一定,可得
比例系数一定,可得
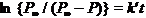
与实验事实相符,可见,a=1是对的;
又据准一级反应,可得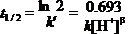
取对数,
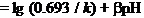 (3分)
(3分)
已知 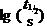 -pH直线斜率=-1,故b = –1,则有
-pH直线斜率=-1,故b = –1,则有
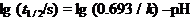
与实验事实相符,由此可得该反应实验速率方程为
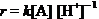 (1分)
(1分)
(2) 由上述反应机理知:
 (1)
(1)
应用稳态近似,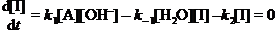
\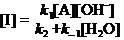 (2)
(2)
将(2)式代入(1)式得:
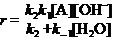 (3)
(3)
当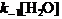 >>
>>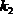 时,则
时,则
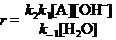
又 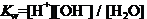 (4)
(4)
将(4)式代入(3)式,经整理得:
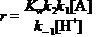
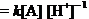 ,
, 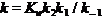 (3分)
(3分)
可见与实验事实相符。
3. 能从普通的百分含量算式转化为药片含量(g/片)的计算
第五题:
 (2分)
(2分) (2分)
(2分)
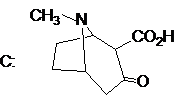 (2分)
(2分) 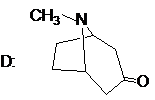 (2分)
(2分)
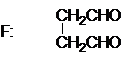 (2分)
(2分)
注:
(1) A→D的结构写成平面结构,只要对,都给2分。
(2) 结构式中, 碳架标氢时, 氢的数目不对, 每处扣0.5分;都不标氢不扣分。
2. 在一定条件(pH)下,两反应物之间的化学计量关系(1:2)
1. 酸碱离解平衡的概念及应用离解算式进行简单计算的能力。
2.
(5分) 由于水杨酸的pKa2 =13.1,而酚酞终点pH=9.0,可见终点时产物为
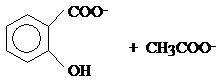 ,因此在测定中,每一摩尔的乙酰水杨酸消耗2摩尔的NaOH。 (2分)
,因此在测定中,每一摩尔的乙酰水杨酸消耗2摩尔的NaOH。 (2分)
含量(g/片)= (3分)
(3分)
注:考核点
1. (5分)
根据离解平衡:HA H++A- ,
H++A- ,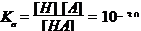
\在胃中  (2分)
(2分)
即 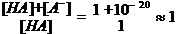
而在血浆中,\HA的离解增大
\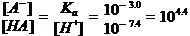
即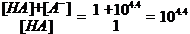 (2分)
(2分)
则总药物之比:
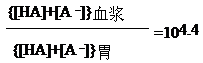 或2.5´104 (1分)
或2.5´104 (1分)
3. 共6分,每小题2分
①缓冲剂,控制酸度,抑制放H2,水解,沉淀等。 (2分)
②配合剂,降低[Cu2+](即电位下降),阻止与新生态Cu反应。 (2分)
③抗氧剂,抑制氧化反应。 (2分)
④稳定剂,防止累积的Fe2+对铜的沉积产生不良影响和减缓Fe2+氧化为Fe3+。 (2分)
第三题
(1)(4分)
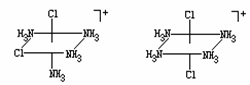
A: [Co(CO3)(NH3)4]Cl;(0.5分) C中配离子的立体结构 D中配离子的立体结构
B: C和D的混合物;(0.5分) (1分) (1分)
C: cis-[CoCl2(NH3)4]Cl·0.5H2O; (0.5分)
D: trans-[CoCl2(NH3)4]Cl·HCl·H2O;(0.5分 )
(2) (3分)
8NH4+ + 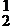 O2 + 2CoCO3 = 2[Co(CO3)(NH3)4]+
+ 6H+ + H2O
(1分)
O2 + 2CoCO3 = 2[Co(CO3)(NH3)4]+
+ 6H+ + H2O
(1分)
[Co(CO3)(NH3)4]Cl
+ 2HCl  cis-[CoCl2(NH3)4]Cl·0.5H2O(主产物) +CO2 +
cis-[CoCl2(NH3)4]Cl·0.5H2O(主产物) +CO2 + 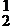 H2O (1分)
H2O (1分)
cis-[CoCl2(NH3)4]Cl·0.5H2O + HCl +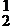 H2O
H2O
trans-[CoCl2(NH3)4]Cl·HCl·H2O (1分 )
(3) (2分)
由C与D中配离子的立体结构可知,由于前者中各个M-L键的极性不能相互抵消,C中相应的配离子具有极性(1分);而在后者中各个M-L键的极性可相互抵消,D中相应的配离子没有极性(1分)
(4) (1分)
用少量冷水洗涤B是为了除去D (0.5分)
浓盐酸起沉淀剂的作用 (0.5分)
(5) (1分)
C与D之间的转化属于顺-反异构化反应 (1分)
(6) (1分)
答案一:[CoCl2(en)2]+可被拆分的几何异构体形式应为顺式异构体(1分),经类比推测未知紫色化合物C为顺式构型。
或答案二:由题给条件推测紫色化合物在一定温度和浓盐酸条件下容易转化为绿色化合物D(1分) 第(6)题只要写出一种答案即给分。
第四题
2. 共8分
①Cu2++Cu+2H2O==2CuOH↓+2H+ (2分)
②CuOH+H++e==Cu+H2O j-=0.287V (2分)
Cu2++H2O+e==CuOH+H+ j+=0.314V (2分)
E = 0.027V > 0 正方向自发 (2分)
或 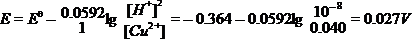 (6分)
(6分)
1. 共8分(每个方程式1分,杂质1分)
①CuO或Cu(OH)2 Cu2++2H2O == Cu(OH)2↓+2H+
②Cu2O或CuOH Cu++H2O == CuOH↓+H+
③FeO或Fe(OH)2 Fe2++2 H2O == Fe(OH)2↓+2H+
④Fe2O3或Fe(OH)3 2Fe(OH)2+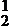 O2+H2O == 2Fe(OH)3↓
O2+H2O == 2Fe(OH)3↓
·写出Cu2+与Fe得到Cu+等等反应者,只要正确,不扣分。
·方程式未配平或配平错误均不得分。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com