
17.已知甲、乙、丙是三种常见的单质,且组成它们的三种元素的核电荷数之和为35,A到H是八种常见化合物。上述各物质间的相互关系见下图所示(反应条件省略):



 产物之一
产物之一


 甲 丙 B 丙 E 水 丙
甲 丙 B 丙 E 水 丙


|



 A
D G
②
A
D G
②






 乙 丙
C 丙 ① F 水 H溶液
乙 丙
C 丙 ① F 水 H溶液
试回答:
(1)与丙互为同素异形体的单质是__________________(写化学式)
(2)从A到H八种化合物中摩尔质量相同的是___ _______(写化学式)
(3)写出①②两步的化学方程式:
①________________________________________
②___________________________________ _
16.120℃、101Kpa时,有2LH2O(g),2LCO,1LCO2,0.5LO2和1LH2组成的混合气体.现将混合气体通过分别放有足量铜粉、碳粉和氧化铜粉的三个灼热的反应管。假设气体通过每个反应管都充分反应,且不论三个反应管以何种顺序排列,则( )
A.原气体中O2不可能再存在于尾气中 B.尾气不可能是单一气体
C.原气体中H2O、CO2肯定存在于尾气中 D.尾气不可能是CO、H2
15.有下列四种判断:①两种弱酸相互反应生成两种强酸;②两种弱酸盐相互作用后生成两种强酸盐;③一种弱酸和一种盐溶液作用后,得到一种强酸和一种盐;④两种酸溶液混合后,溶液的酸性减弱。其中有具体例证的是( )
A、①② B、②③ C、②③④ D、①②③④
14.浅绿色的Fe(NO3)2溶液中,存在水解平衡:Fe2++2H2O≒Fe(OH)2+2H+。若在此溶液中加入盐酸,则溶液颜色 A、绿色变深 B、绿色变浅 C、变黄 D、不变
13.下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
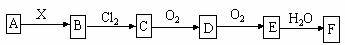
下列说法中正确的是( )
A. 当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B. 当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C. B和Cl2的反应是氧化还原反应
D. 当X是强酸时,C在常温下是气态单质
12.有机物A由于其特殊的电子结构,一直受到理论化学家的注意,由于缺乏有效的合成途径,一度延缓对其反应的研究,直到1993年出现了可以大量制备的方法。已知A是非极性分子,化学式是C6H8,核磁共振表明分子中所有的氢原子都等价。下列关于A的说法正确的是( )
A.A的不饱和度为4
B.A的二氯取代产物的位置异构有4种(不考虑顺反异构和对映异构)
C.A的结构中一定有两个双键
D.A可以发生加成、取代反应
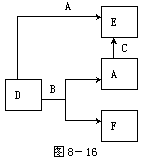
11.A、B、C分别是元素甲、乙、丙的 单质,它们都是常见的金属或非金属。D、E、F是常见的三种氧化物,且有如图所示转化关系:则下列说法不正确的是( )
A.D、E中一定都含有A的元素
B.单质B肯定是氧化剂
C.A、B、C中一定有一种是氧元素的单质
D.若A是非金属,则B一定为金属
10.甲、乙、丙、丁各是Na2SO3、AgNO3、HCl、BaCl2四种无色溶液中的一种,它们两两反应后的现象如下:
甲+乙→沉淀 甲+丙→沉淀 乙+丙→沉淀
丙十丁→沉淀 乙+丁→无色刺激性气味气体,
则甲、乙、丙、丁依次是( )
A Na2SO3 HCl AgNO3 BaCl2
B BaCl2 Na2SO3 HCl AgNO3
C BaCl2 Na2SO3 AgNO3 HCl
 D AgNO3 HCl
BaCl2 Na2SO3
D AgNO3 HCl
BaCl2 Na2SO3
9.现有Na2CO3、H2SO4、Ba(OH)2三种物质的量浓度与体积都相等的溶液,若以不同顺序将它们中的两种混合起来,出现沉淀后过滤,再将滤液与第三种溶液混合起来,最终所得的溶液( )
A.一定呈酸性 B.可能呈碱性 C.可能呈中性 D.一定呈中性
8.若原子核外电子排布的基本规律为最外层电子数不超过5个,次外层电子数不超过10个,倒数第三层电子数不超过15个,而各电子层电子的最大容量仍为2n2,则元素周期表中第三,四,五周期含有的元素分别有
A.5种,10种,15种 B.8种,18种,18种
C.5种,9种,10种 D.9种,19种,29种
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com