
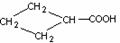
27.已知:①乙醛甲基上的氢原子都是a氢原子,活性较大,都可以与甲醛中的醛发生加成反应,如HCHO+CH3CHO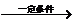 HO-CH2-CH2-CHO;②CH2(COOC2H5)2
HO-CH2-CH2-CHO;②CH2(COOC2H5)2
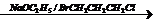
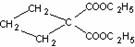
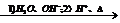
|
|
|
|
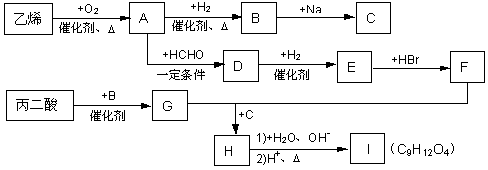
请回答下列问题:
(1) 写出下列物质的结构简式:E ▲ ;H ▲ ;I ▲ 。
(2)写出A→D化学方程式: ▲ 。
26.Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备并分析Na2CO3的纯度。下面是他的实验过程:
实验一:Na2CO3制备:
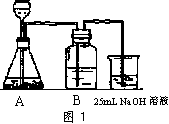 用50mL
NaOH溶液吸收CO2气体制备Na2CO3。为防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:(i)用25mL
NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;(ii)小心煮沸溶液1~2分钟;(iii)在得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合。
用50mL
NaOH溶液吸收CO2气体制备Na2CO3。为防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:(i)用25mL
NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;(ii)小心煮沸溶液1~2分钟;(iii)在得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合。
(1)他能否制得较纯净的Na2CO3? ▲ 。理由是 ▲ 。
(2)按他的设计,第(i)步实验装置如图1:
①装置A使用的试剂是石灰石和盐酸溶液。可否使用
纯碱代替石灰石? ▲ 。原因是 ▲ 。
②装置B使用的试剂是 ▲ ,作用是 ▲ 。
③为了后续的煮沸、混合等实验,装NaOH溶液的容器还可使用 ▲ 。(填实验仪器)
 ④有人认为实验步骤(ii)、(iii)的顺序对调,即先混合,再煮沸,更合理,你认为对吗?
▲
,为什么? ▲
。
④有人认为实验步骤(ii)、(iii)的顺序对调,即先混合,再煮沸,更合理,你认为对吗?
▲
,为什么? ▲
。
实验二:Na2CO3纯度分析:
|
|
 某同学用图3测定Na2CO3试样的纯度(杂质不与水反应),其中A容器中盛有Na2CO3样品10.0g,分液漏斗内盛有稀H2SO4,B容器内为碱石灰固体。他利用碱石灰的增重求出纯净的Na2CO3质量,再求纯度。他重复正确操作了三次,结果数据出现了较大偏差(设原容器中CO2气体的含量可忽略不计,各容器内反应完全,下同)
某同学用图3测定Na2CO3试样的纯度(杂质不与水反应),其中A容器中盛有Na2CO3样品10.0g,分液漏斗内盛有稀H2SO4,B容器内为碱石灰固体。他利用碱石灰的增重求出纯净的Na2CO3质量,再求纯度。他重复正确操作了三次,结果数据出现了较大偏差(设原容器中CO2气体的含量可忽略不计,各容器内反应完全,下同)
(3)请你分析出现较大偏差的原因 ▲ 。
通过仔细分析,该同学重新设计了一套实验装置(见图4),并回答有关问题:(实验室中可供选择的试剂和药品还有Zn片、浓H2SO4、NaOH溶液、CaCO3固体、蒸馏水)
|

(4)该同学新设计的装置是否已完整,如有必要,可在B、D虚框内画出合适的装置简图,如要用到药品或试剂,应在右下角注明 ▲ 。
(5)A装置中分液漏斗所盛液体为 ▲ ;U形管内盛有 ▲ ;A装置在整套装置中的作用 ▲ ;F装置的作用是 ▲ 。
(6)如果B、D内部不设计任何装置而直接连通ACE,则实验结果将 ▲ (偏高、偏低、无影响)。
(7)如果实验后E装置质量增重3.96g,则该Na2CO3试样的纯度为 ▲ 。
25.据2000年4月出版的《参考消息》报道:美国硅谷已成功开发出分子计算机,其中主要器件为分子开关和分子导线。
美国Gokel教授研制了氧化还原型电控分子开关--蒽醌套索醚电控开关。它是通过电化学还原使冠醚“胳膊”阴离子化,从而加强对流动阳离子的束缚力,达到“关”的作用;再借助氧化反应使其恢复到原来的“开启”状态,使阳离子顺利流动:
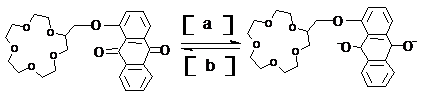
A B
(1)在括号中填写反应类型(填氧化反应、还原反应):a ▲ 反应,b ▲ 反应。
(2)若分子计算机中分子开关处于A状态,则计算机处于 ▲ 状态,若分子计算机中分子开关处于B状态,则计算机处于 ▲ 状态(填“开启”或“关闭”)。
24.在烃的分子结构中,若每减少2个氢原子,则相当于碳碳间增加一对共用电子。试回答下列问题:
(1)分子式为CnH2n+2的烃分子中碳碳间共用电子对数为 ▲ ;
(2)分子式为CnH2n-6的烃分子中碳碳间共用电子对数为 ▲ ;
(3)Cx可看作是烃减氢后的产物,若某物质分子中碳碳间的共用电子对数为160,则符合该条件的碳单质的分子式为 ▲ ;符合该条件的单烯烃的分子式为 ▲ 。
(4)目前,化学家们已经找到十余种富勒烯家族的Cx,它们分子结构中都由正五边形和正六边形构成的封闭的凸多面体,C60就是其中的一种富勒烯,其结构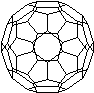 见右图。第(3)小题中的Cx也是其中一种富勒烯。则第(3)小题中Cx结构中五边形和六边形的个数分别是 ▲
和 ▲
。
见右图。第(3)小题中的Cx也是其中一种富勒烯。则第(3)小题中Cx结构中五边形和六边形的个数分别是 ▲
和 ▲
。
(5)下列物质不属于富勒烯家族的有 ▲ 。
A、C18 B、C44 C、C72 D、C83
23.有A、B、C、D四种短周期元素。已知一个B原子的原子核受到a粒子的轰击得到一个A原子的原子核和一个C原子的原子核,又知C、D元素同主族,且能发生下面两个反应。
A、B 化合物 + B、C 化合物
 B单质 + A、C 化合物
B单质 + A、C 化合物
A、D 化合物
+
D、C 化合物
 D单质 + A、C 化合物
D单质 + A、C 化合物
请回答:
(1)比较B、C原子半径大小 ▲ ;画出D离子的结构示意图 ▲ 。
(2)分别写出上述两个反应方程式 ▲ ; ▲ 。
22.水具有很高的热稳定性,即使加热到2000K也只有0.588%的水分解成氢气和氧气。科学家已经找到了一种方法,分三步可使水在500℃以下分解:首先在500℃下加热FeCl2水溶液,将生成的Fe3O4在HCl介质中与Cl2在1000C时反应,最后将生成的固体物质在300℃时加热分解。则该三步方程式分别是:(1) ▲ ;(2) ▲ ;(3) ▲ 。
21.(SN)n是最早发现的无机高分子化合物(相对分子质量很大的化合物),n是一个很大的整数。由许许多多(SN)n分子组成的晶体,有各向异性的结构特点。最典型的是,从晶体两个相互垂直的方向上,室温下测定其导电率,其相差竟在2个数量级上。回答下列问题:
(1)已知(SN)n由S2N2聚合而生成,在S2N2中,S和N的化合价数值视为相同,则S2N2分子结构是(请画出) ▲ 。
(2)上述晶体属于 ▲ (填晶体类型),理由是 ▲ 。
(3)(SN)n分子的几何形状,是平面型,立体型,还是线型? ▲ ,理由是 ▲ 。
19.已知25%氨水的密度为0.91g/cm3,5%氨水的密度为0.98g/cm3,若将上述两溶液等体积混合,所得氨水溶液的质量分数是
A、等于15% B、大于15% C、小于15% D、无法判断
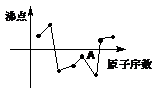 20.右图中曲线表示原子序数在前20号中的某些元素的原子序数(按递增顺序连续排列)和单质沸点的关系,其中A点表示的元素是
20.右图中曲线表示原子序数在前20号中的某些元素的原子序数(按递增顺序连续排列)和单质沸点的关系,其中A点表示的元素是
A、Si B、Al C、F D、S
18.CH4分子为正四面体结构,若CH4分子中的氢原子能被F、Cl、Br、I四种卤原子取代,那么所得卤代烃有多少种?
A 、68 B、69 C、70 D、71
17.SF6是一种无色气体,具有很强的稳定性,可用于灭火。SF6的分子结构如右图所示,呈正八面体型。如果F元素有两种稳定的同位素,则SF6的不同分子种数为
A、6种 B、7种 C、10种 D、12种
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com