
14.(09年山东理综·29)(12分)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是 。电池工作时,电子流向 (填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
。欲除去Cu2+,最好选用下列试剂中的 (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是 。若电解电路中通过2mol电子,MnO2的理论产量为 。
答案:(1)Zn(或锌) 正极
(2)Zn与Cu2+反应生成Cu,Zn与Cu构成原电池,加快反应速率 b
(3)2H++2e-=H2↑ 87g
 解析:(1) 负极上是失电子的一极 Zn失电子有负极经外电路流向正极。(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀。除杂的基本要求是不能引入新杂质,所以应选Zn将Cu2+
置换为单质而除去。(3)阴极上得电子,发生还原反应, H+得电子生成氢气。因为MnSO4-MnO2-2 e-,通过2mol电子产生1molMnO2,质量为87g。
解析:(1) 负极上是失电子的一极 Zn失电子有负极经外电路流向正极。(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀。除杂的基本要求是不能引入新杂质,所以应选Zn将Cu2+
置换为单质而除去。(3)阴极上得电子,发生还原反应, H+得电子生成氢气。因为MnSO4-MnO2-2 e-,通过2mol电子产生1molMnO2,质量为87g。
 [考点分析] 原电池原理和电解原理综合运用
[考点分析] 原电池原理和电解原理综合运用
1 5.(09年天津理综·10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
5.(09年天津理综·10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
 (1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示)。
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示)。
 (2)负极反应式为
。
(2)负极反应式为
。
 (3)电极表面镀铂粉的原因为
。
(3)电极表面镀铂粉的原因为
。
 (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2
 2LIH
2LIH
 Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
 ①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是
。
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是
。
 ②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
。
 ③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
答案:(1)由化学能转化为电能 由a到b
(2)2H2+4OH--4e-=4H2O或H2+2OH--2e-=2H2O
(3)增大电极单位面积吸附H2、O2分子数,加快电极反应速率
(4)①Li H2O ②或8.71×10-4 ③32
解析:本题考查电化学知识。(1)原电池的实质为化学能转化成电能。总反应为2H2 + O2 =2H2O,其中H2从零价升至+1价,失去电子,即电子从a流向b。(2)负极为失去电子的一极,即H2失电子生成H+,由于溶液是碱性的,故电极反应式左右应各加上OH-。(3)铂粉的接触面积大,可以加快反应速率。(4)I.Li从零价升至+1价,作还原剂。II.H2O的H从+1降至H2中的零价,作氧化剂。由反应I,当吸收10molH2时,则生成20molLiH,V=m/ρ=20×7.9/0.82 ×10-3L=192.68×10-3L。V(LiH)/v(H2)= 192.68×10-3L/224L=8.71×10-4。20mol LiH可生成20mol H2,实际参加反应的H2为20×80%=1.6mol,1molH2转化成1molH2O,转移2mol电子,所以1.6molH2可转移3.2mol的电子。
13.(12分)(08年山东理综·29)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)=CH4(g)+HC
 CH(g)+H2(g) △H1=156.6
kJ·mol-1
CH(g)+H2(g) △H1=156.6
kJ·mol-1
CH3CH
 CH2(g)=CH4(g)+HC
CH2(g)=CH4(g)+HC
 CH(g ) △H2=32.4 kJ·mol-1
CH(g ) △H2=32.4 kJ·mol-1
则相同条件下,反应C3H8(g)=CH3CH
 CH2(g)+H2(g) 的△H= kJ·mol-1。
CH2(g)+H2(g) 的△H= kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时CO32-移向电池的 (填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5
mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是 (用离子方程式和必要的文字说明)。
答案:
(1)124.2
(2)C3H8+5O2=3CO2+4H2O 负
(3)4.2×10-7 mol·L-1
(4)> HCO3-+H2O=CO32-+H3O+(或HCO3-=CO32-+H+)、HCO3-+H2O=H2CO3+OH-,HCO3-的水解程度大于电离程度
解析:(1)将第2个方程式颠倒反写,然后与第1个方程式相加,即得所求的反应C3H8(g)====CH3CH=CH2 (g)+H2(g),△H也随方程式的变化关系进行求算:△H=-△H2+△H1=124.2kJ.mol-1。
(2)以丙烷为燃料制作的新型燃料电池,其电池反应方程式为C3H8十502=3C02+4H20,因电子从电池的负极经导线流入了电池的正极,故电池的正极是电子富集的一极,故带负电荷的离子C032-在电解质溶液中应移向电池的负极而不是正极。
(3)根据电离平衡常数公式可知:
K1=c(H+)c(HCO3-)/c(H2CO3)=10-5.60×10-5.60/l.5×10-5=4.2×10-7mol. L-1。
(4)0.1 mol L-1NaHCO3溶液的pH大于8,说明溶液呈碱性,即c(OH-)>c(H+),因在NaHCO3溶液中存在着两个平衡:电离平衡HCO3-
 CO32-+H+,水解平衡: HC03-+H20
CO32-+H+,水解平衡: HC03-+H20 
 H2CO3-+OH-
,其余部分水的电离忽略不计,由c(OH-)>c(H+),说明水解过程大于电离过程,从而推出c(H2CO3)>c(CO32-)
。
H2CO3-+OH-
,其余部分水的电离忽略不计,由c(OH-)>c(H+),说明水解过程大于电离过程,从而推出c(H2CO3)>c(CO32-)
。
12.(07年广东化学·24)(10分)
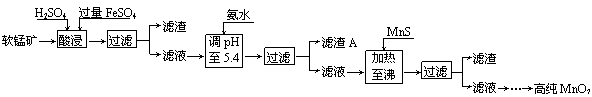 二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
某软锰矿的主要成分为MnO2,还含有Si(16.72%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
CuS |
ZnS |
MnS |
FeS |
|
pH |
5.2 |
3.2 |
9.7 |
10.4 |
6.7 |
8.0 |
≥–0.42 |
≥2.5 |
≥7 |
≥7 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为 。
(2)滤渣A的主要成分是 。
(3)加入MnS的目的是除去 杂质。
(4)碱性锌锰电池中,MnO2参与的电极反应方程式为 。
(5)从废旧碱性锌锰电池中可以回收利用的物质有 (写出两种)。
答案:
(1)MnO2+2FeSO4+2H2SO4=MnSO4+Fe2(SO4)3+2H2O
(2)Fe(OH)3 Al(OH)3
(3)Cu2+ Zn2+
(4)MnO2+H2O+e-=MnOOH+OH-(或2MnO2+H2O+2e-=Mn2O3+2OH-)
(5)锌、二氧化锰
解析:考查学生对元素化合物的主要性质的掌握、书写电极反应方程形式的能力以及学生能够从试题提供的新信息中,准确地提取实质内容,并与已有知识模块整合,重组为新知识模块的能力。由反应流程可知:在酸性条件下二氧化锰将Fe2+氧化为Fe3+,将Cu氧化成Cu2+,此外溶液中的还有Zn2+和Al3+,当调pH至5.4时,只有Al(OH)3 和Fe(OH)3会完全沉淀,故滤渣A的主要成分是Fe(OH)3和Al(OH)3。加入MnS后因为酸性条件下CuS 、ZnS更难溶所以会转化为CuS 、ZnS沉淀而除去Cu2+ Zn2+。
11.(09年广东文基·68)下列说法正确的是
A.废旧电池应集中回收,并填埋处理
B.充电电池放电时,电能转变为化学能
C.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
D.所有燃烧反应都是放热反应,所以不需吸收能量就可以进行
答案:C
解析:A项废旧电池应集中回收但不能填埋处理因为电池里的重金属会污染土地,人吃了这些土地里的蔬菜后,,就会引发疾病;B项充电电池放电时,化学能转变为电能;D项有的燃烧反应是需要吸收一定热量才可以反应的比如碳的燃烧。
9.(09年广东理基·34)下列有关电池的说法不正确的是
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
答案:B
解析:手机上用的锂离子电池可以反复充放电,属于二次电池,A选项正确。锌比铜活泼,因此构成原电池时,锌失电子做负极,电子眼外电路流向正极铜,所以B选项错误。
 1
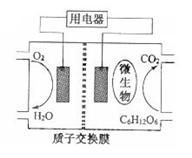
1 0.(09年江苏化学·12)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
0.(09年江苏化学·12)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
 A.该电池能够在高温下工作
A.该电池能够在高温下工作
 B.电池的负极反应为:C6H12O6+6H2O-24e-
B.电池的负极反应为:C6H12O6+6H2O-24e- 6CO2↑+24H+
6CO2↑+24H+

 C.放电过程中,H+从正极区向负极区迁移
C.放电过程中,H+从正极区向负极区迁移
 D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体
D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体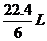
 答案:B
答案:B
 解析:A项,高温条件下微生物会变性,所以A错;B项,负极是葡萄糖失电子生成二氧化碳,所以B对;C项,原电池内部阳离子应向正极移动,所以C错;D项,消耗1mol氧气生成1mol二氧化碳,标准状况下体积是22.4L,D错。
解析:A项,高温条件下微生物会变性,所以A错;B项,负极是葡萄糖失电子生成二氧化碳,所以B对;C项,原电池内部阳离子应向正极移动,所以C错;D项,消耗1mol氧气生成1mol二氧化碳,标准状况下体积是22.4L,D错。
8.(09年广东化学·14)可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为点解液,铝合金为负极,空气电极为正极。下列说法正确的是
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4OH-
B.以NaOH溶液为电解液时,负极反应为:Al+3OH--3e=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
答案:A
解析:无论是NaOH还是NaCl,在正极上都是O2得到电子被还原,A正确;生成的Al(OH)3是两性氢氧化物,在碱溶液中发生反应生成AlO2-,B错误;生成的Al(OH)3与NaOH反应生成NaAlO2,消耗电解质中的NaOH,使pH减少,C错误;原电池中,电子在外电路的负极流向正极,D错误。
7.(08年江苏化学·5)镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O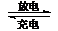 Cd(OH)2
+ 2Ni(OH)2。有关该电池的说法正确的是
Cd(OH)2
+ 2Ni(OH)2。有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2 -e- + OH- == NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
答案:A
解析:由充电时方程式中的Cd和Ni的化合价的变化可知,Ni(OH)2作阳极,电解质溶液为KOH,所以电极反应式为:Ni(OH)2-e- +OH-===NiOOH+H2O;Cd(OH)2作阴极,Cd(OH)2+2e- ===Cd+2OH-;充电的过程是将电能转化为化学能,放电时,Cd作负极,Cd-2e-+2OH- ===Cd(OH)2,Cd周围的c(OH-)下降,OH-向负极移动。
6.(08年海南化学·7)关于铅蓄电池的说法正确的是
A.在放电时,正极发生的反应是 Pb(s) +SO42-(aq)= PbSO4(s) +2e-
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO4(s)+2e-= Pb(s)+ SO42-(aq)
答案:B
解析:铅蓄电池的充放电反应为:Pb+PbO2+2H2SO4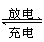
 PbSO4+2H2O,放电时Pb作负极:Pb-2e-+SO42- ===PbSO4,在正极上:PbO2+2e-+4H++SO42- ===PbSO4+2H2O;充电时,H2SO4的浓度不断增大,阳极上发生的是氧化反应,是失去电子而不是得到电子。
PbSO4+2H2O,放电时Pb作负极:Pb-2e-+SO42- ===PbSO4,在正极上:PbO2+2e-+4H++SO42- ===PbSO4+2H2O;充电时,H2SO4的浓度不断增大,阳极上发生的是氧化反应,是失去电子而不是得到电子。
5.(08年广东理基·20)电池是人类生产和生活中重要的能量来源。各式各样电池的发明是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池可将热能直接转变为电能
C.氢氧燃料电池工作时氢气在负极被氧化
D.太阳能电池的主要材料是高纯度的二氧化硅
答案:C
解析:A. 锌锰干电池的碳棒为负极,不会被消耗;
B. 燃料电池将燃料的化学能转化为电能和部分热能散失;
C. 燃料电池燃料是被氧化的,永远做负极;
D. 太阳能电池的主要材料是硅而非二氧化硅。
4.(08年广东化学·16)LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li
 LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是
A.可加入硫酸以提高电解质的导电性
B.放电时电池内部Li+向负极移动.
C.充电过程中,电池正极材料的质量减少
D.放电时电池正极反应为:FePO4+Li++e-=LiFePO4
答案:CD
解析:放电时,负极:Li -- e- ==Li+,正极:FePO4 + Li+ + e- == LiFePO4;充电时,阳极:LiFePO4 -- e- == FePO4 + Li+ 阴极:Li+ + e- == Li,所以易知C.D正确。
若加入硫酸,与Li单质(固体)发生反应,所以A错;放电时,Li+应(正电荷)在电池内部(电解质中)向正极移动,故B错。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com