
5、关于秦朝设郡的数目,学术界有不同的看法。如王国维《秦郡考》考证共有48郡,谭其骧《秦郡新考》推定为46郡。某同学在考证秦郡数目时,收集到以下几个方面的资料,其中最可信的应是
A、《史记》的记载 B、民间的传说
C、史家的研究论文 D、秦简的记载
4、“六字炳千秋,十四县民命食天,尽是此公赐予;万流归一汇,八百里青城沃野,都从太守得来”,此对联中的“太守”是指:
A、郑国 B、苏轼 C、李冰 D、欧阳修
3、《春秋繁露》曰:“天子受命于天,天下受命于天子,一国则受命于君。君命顺,则民有顺命;君命逆,则民有逆命。”材料主张的思想是
A、君权神授 B、天人感应 C、天人合一 D、大一统
2、西周时期,选拔官吏的基本方法是
A、推荐 B、分科考试 C、自荐 D、血缘世袭
1、《左传•昭公》曰:“昔武王克殷,成王靖四方,康王息民,并建母弟,以番屏周。”材料反映西周的主要政治意图是
A、灭亡殷商 B、巩固疆域 C、镇压叛乱 D、恩及兄弟
22.(10分)向amol NaOH溶液中逐滴加入bmol AlCl3溶液,试回答:
 (1)依次写出溶液中发生反应的化学方程式。
(1)依次写出溶液中发生反应的化学方程式。
 (2)若a+b=1,当a取不同值时,生成物可能有以下情况:
(2)若a+b=1,当a取不同值时,生成物可能有以下情况:
 ①全部是Al(OH)3时,a的取值范围是
。
①全部是Al(OH)3时,a的取值范围是
。
 ②全部是NaAlO2时,a的取值范围是 。
②全部是NaAlO2时,a的取值范围是 。
 ③部分是NaAlO2,部分是Al(OH)3,a的取值范围是 。反应所生成的Al(OH)3的物质的量为
mol,反应所生成的各物质的总物质的量(包括水)为 mol(用含b的式子表示)。
③部分是NaAlO2,部分是Al(OH)3,a的取值范围是 。反应所生成的Al(OH)3的物质的量为
mol,反应所生成的各物质的总物质的量(包括水)为 mol(用含b的式子表示)。
 ④在上述条件下,若要生成7.8g沉淀,则a的值等于 或
。
④在上述条件下,若要生成7.8g沉淀,则a的值等于 或
。
21.(14分)某芳香族化合物A的结构简式是 (其中R为饱和烃基),A在一定条件下有如下图所示的转化关系。已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2。

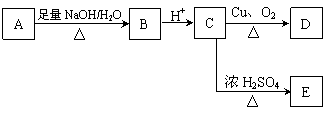

 (1)E的分子式是
。
(1)E的分子式是
。
 (2)关于上述各步转化中,下列说法正确的是
。
(2)关于上述各步转化中,下列说法正确的是
。
 a.
以上各步没有涉及加成反应 b. E比C的相对分子质量小18
a.
以上各步没有涉及加成反应 b. E比C的相对分子质量小18
 c. A、B、C、D中都含有-COOH d . A与C发生酯化反应后得到的有机物分子式可能是C18H18O4Cl
c. A、B、C、D中都含有-COOH d . A与C发生酯化反应后得到的有机物分子式可能是C18H18O4Cl
 (3)写出所有符合下列要求的E的同分异构体的结构简式: 、 (①分子中苯环上有三个取代基,且苯环上的一氯代物有两种 ②1 mol该有机物与足量银氨溶液反应能产生4 mol Ag)。
(3)写出所有符合下列要求的E的同分异构体的结构简式: 、 (①分子中苯环上有三个取代基,且苯环上的一氯代物有两种 ②1 mol该有机物与足量银氨溶液反应能产生4 mol Ag)。
 (4)针对以下不同情况分别回答:
(4)针对以下不同情况分别回答:
 ①若E能使溴的四氯化碳溶液褪色,还能与NaHCO3溶液反应生成F;D能发生银镜反应。
①若E能使溴的四氯化碳溶液褪色,还能与NaHCO3溶液反应生成F;D能发生银镜反应。
 则D的结构简式是 。欲由A通过一步反应得到F,该反应的化学方程式是 。
则D的结构简式是 。欲由A通过一步反应得到F,该反应的化学方程式是 。
 ②若E中除苯环外,还含有一个六元环,则C→E的化学方程式是 。
②若E中除苯环外,还含有一个六元环,则C→E的化学方程式是 。
20.(10分)X、Y、Z为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应: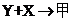 (g),
(g),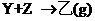 。甲、乙可化合生成离子化合物,甲的相对分子质量小于乙。
。甲、乙可化合生成离子化合物,甲的相对分子质量小于乙。
 (1)X的结构式是 。
(1)X的结构式是 。
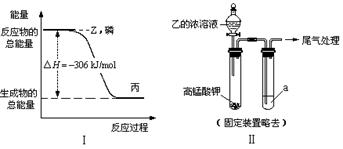
 (2)磷在Z气体中燃烧可生成液态丙分子,也可生成固态丁分子。已知丙分子中各原子最外层均是8电子结构,丙的电子式是 。磷单质和Z单质反应生成1 mol丙时,反应过程与能量变化如图Ⅰ所示,该反应的热化学方程式是 。
(2)磷在Z气体中燃烧可生成液态丙分子,也可生成固态丁分子。已知丙分子中各原子最外层均是8电子结构,丙的电子式是 。磷单质和Z单质反应生成1 mol丙时,反应过程与能量变化如图Ⅰ所示,该反应的热化学方程式是 。
 (3)某同学拟用图Ⅱ所示装置证明氧化性Z>I2,已知高锰酸钾与乙的浓溶液反应生成Z,则a是
的水溶液。若仅将a换为甲的浓溶液,实验时会产生大量白烟并有气体单质生成,该反应的化学方程式是 。
(3)某同学拟用图Ⅱ所示装置证明氧化性Z>I2,已知高锰酸钾与乙的浓溶液反应生成Z,则a是
的水溶液。若仅将a换为甲的浓溶液,实验时会产生大量白烟并有气体单质生成,该反应的化学方程式是 。

 (4)向一定浓度的BaCl2溶液中通入SO2气体,未见沉淀生成,若在通入SO2气体的同时加入由甲和乙中的一种或几种元素组成的某纯净物,即可生成白色沉淀,
(4)向一定浓度的BaCl2溶液中通入SO2气体,未见沉淀生成,若在通入SO2气体的同时加入由甲和乙中的一种或几种元素组成的某纯净物,即可生成白色沉淀, 该纯净物可能是________、________。
该纯净物可能是________、________。
19.(8分)废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
(1)下列处理印刷电路板的回收利用可实现资源再生,并减污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末是 。
A.热裂解形成燃油 B.露天焚烧 C.作为有机复合建筑材料的原料 D.直接填埋
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(S)+2H+(aq)=== Cu2+(aq)+H2(g) ΔH=64.39kJ·mol-1
2H2O2(I)===2H2O(I)+O2(g) ΔH=-196.46kJ·mol-1
H2(g)+
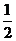 O2(g)===H2O(I) ΔH=-285.84kJ·mol-1
O2(g)===H2O(I) ΔH=-285.84kJ·mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 。
(3)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0 mol·L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
|
温度(℃) |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
铜平均溶解速率 (×10-3mol·L-1·min-1) |
7.34 |
8.01 |
9.25 |
7.98 |
7.24 |
6.73 |
5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 。
(4)在提纯后CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀。制备CuCl的离子方程式是 。
18.(8分)以氯化钾和钛白厂的副产品硫酸业铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:
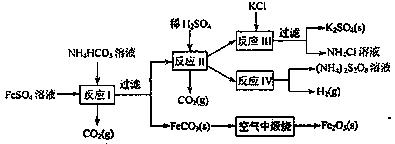
(1) 反应I前需在FeSO4溶液中加入__________(填字母),以除去溶液中的Fe3+。
A.锌粉 B.铁屑 C.KI溶液 D.H2
(2)反应Ⅰ需控制反应温度低于35℃,其目的是 。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是 。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com