
5.(09上海卷4)用浓氯化铵溶液处理过的舞台幕布不易着火。其原因是
①幕布的着火点升高 ②幕布的质量增加
③氯化铵分解吸收热量,降低了温度 ④氯化铵分解产生的气体隔绝了空气
A.①② B.③④ C.③④ D.②④
答案:B
4.(09广东化学 15)取五等份NO2 ,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:
15)取五等份NO2 ,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:
 2NO2(g)
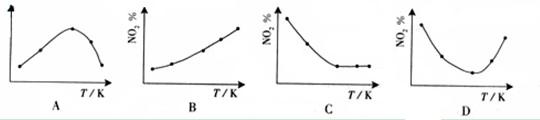
2NO2(g) N2O4(g),ΔH<0 反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是
N2O4(g),ΔH<0 反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是

 答案:BD
答案:BD
 解析:
解析:
在恒容状态下,在五个相同的容器中同时通入等量的NO2,反应相同时间。那么则有两种可能,一是已达到平衡状态,二是还没有达到平衡状态,仍然在向正反应移动。若5个容器在反应相同时间下,均已达到平衡,因为该反应是放热反应,温度越高,平衡向逆反应方向移动,NO2的百分含量随温度升高而升高,所以B正确。若5个容器中有未达到平衡状态的,那么温度越高,反应速率越大,会出现温度高的NO2转化得快,导致NO2的百分含量少的情况,在D图中转折点为平衡状态,转折点左则为未平衡状态,右则为平衡状态,D正确。
3.(09广东理科基础 29)已知汽车尾气无害化处理反应为
29)已知汽车尾气无害化处理反应为

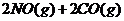
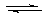
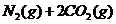
 。
。
 下列说法不正确的是
下列说法不正确的是
 A.升高温度可使该反应的逆反应速率降低
A.升高温度可使该反应的逆反应速率降低
 B.使用高效催化剂可有效提高正反应速率
B.使用高效催化剂可有效提高正反应速率
 C.反应达到平衡后,N0的反应速率保持恒定
C.反应达到平衡后,N0的反应速率保持恒定
 D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
 答案:A
答案:A
 解析:
解析:
升温,无论是正反应,还是逆反应,速率均加快,A项错;
催化剂可以加快化学反应速率,B项正确;
达平衡后,各组分的速率保持不变,C项正确;
由于CO和CO2的计量系数相等,故当两者同时消耗的量相等时,反应即达平衡,D项正确。
1.
 (09全国卷Ⅱ6) 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
(09全国卷Ⅱ6) 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是

 A. 1:4 B.1:5 C. 2:3 D.2:5
A. 1:4 B.1:5 C. 2:3 D.2:5

 答案:A
答案:A
 解析:
解析:
设2molZn参与反应,因Zn无剩余,则最终生成了2molZn(NO3)2,显然含有4molNO3- ,这部分是没有参与氧化还原反应的HNO3,根据得失电子守恒有:2×n(Zn)=n(HNO3)×4,则n(HNO3)=1mol,即有1molHNO3被还原。
2.(09江苏卷
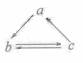 3)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
3)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
|
a |
b |
c |
|
A |
Al |
AlCl3 |
Al(OH)3 |
|
B |
HNO3 |
NO |
NO2 |
|
C |
Si |
SiO2 |
H2SiO3 |
|
D |
CH2=CH2 |
CH3CH2OH |
CH3CHO |
答案:B
 解析:
解析:
A项: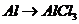 (
(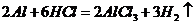
或者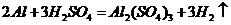 ,
,
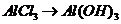 (
(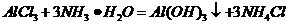 ),
), (
(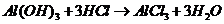 ),
),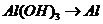 的转化必须经过
的转化必须经过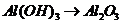 (反应方程式为:
(反应方程式为: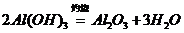 )和
)和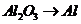 (
(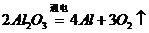 )这两步,所以A项不选;
)这两步,所以A项不选;
 B项:
B项: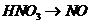 (
(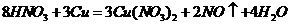 ),
),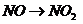 (
(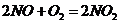 ),
),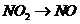 (
(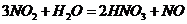 ),
),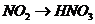 (
(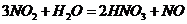 ),所以B项正确;
),所以B项正确;
 C项:
C项: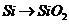 (
(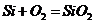 ),
),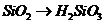 必须经过两步
必须经过两步
( 、
、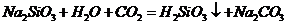 ),
),
 D项:
D项: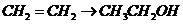 (
(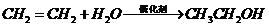 ),
),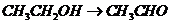 (
(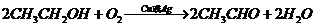 ),
),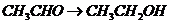 (
( ),
),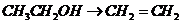 就必须经过两步(
就必须经过两步( 和
和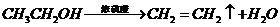 )
)
13.(09海南卷 20)(20分)
20)(20分)

 20-1.下列有关肥皂的叙述中错误的是:
20-1.下列有关肥皂的叙述中错误的是:
 A.肥皂与纯碱的去污原理相同
A.肥皂与纯碱的去污原理相同
 B.肥皂可以加速油污在水中的分散
B.肥皂可以加速油污在水中的分散
 C.肥皂是油脂在碱性条件下水解生成的
C.肥皂是油脂在碱性条件下水解生成的
 D.肥皂主要成分的分子中含有亲油基团和亲水基团
D.肥皂主要成分的分子中含有亲油基团和亲水基团
20-1答案:A
解析:纯碱的去污原理是利用水解呈碱性,使油脂水解,而肥皂则是利用含有的亲油基团和亲水基团.
 20-2.下列使用化肥、农药的描述中正确的是:
20-2.下列使用化肥、农药的描述中正确的是:
 A.高温多雨时比较适合施用钾肥
A.高温多雨时比较适合施用钾肥
 B.长期施用硫铵会造成土壤板结
B.长期施用硫铵会造成土壤板结
 C.石硫合剂必须与硫酸混合后才能施用
C.石硫合剂必须与硫酸混合后才能施用
 D.过磷酸钙必须经硫酸处理后才能施用
D.过磷酸钙必须经硫酸处理后才能施用
20-2答案:B
解析:A容易在成钾流失,C石硫合剂呈碱性,D过磷酸钙可直接使用,不需加入硫酸.
 20-3.下列有关硬水及其软化的说法中错误的是:
20-3.下列有关硬水及其软化的说法中错误的是:
 A.离子交换法可以软化硬水
A.离子交换法可以软化硬水
 B.硬水中含有较多Ca2+、Mg2+
B.硬水中含有较多Ca2+、Mg2+
 C.生产、生活使用的天然水必须经软化
C.生产、生活使用的天然水必须经软化
 D.加热可使暂时硬水中的Ca2+生成CaCO3沉淀
D.加热可使暂时硬水中的Ca2+生成CaCO3沉淀
20-3答案:C
解析:本题可采用排除法,ABD肯定正确,C中是用天然水视具体情况不一定都要软化.
 20-4(11分)
20-4(11分)
 工业上常用氨氧化法生产硝酸,其过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题:
工业上常用氨氧化法生产硝酸,其过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题:
 (1)氨催化氧化的化学方程式为
:
(1)氨催化氧化的化学方程式为
:
 (2)原料气中空气必须过量,其主要原因是
;
(2)原料气中空气必须过量,其主要原因是
;
 (3)将铂铑合金做成薄丝网的主要原因是
;
(3)将铂铑合金做成薄丝网的主要原因是
;
 (4)水吸收二氧化氮生成硝酸为放热反应,其化学方程式为
,为了提高水对二氧化氮的吸收率,可采取的措施为
(答2项)
(4)水吸收二氧化氮生成硝酸为放热反应,其化学方程式为
,为了提高水对二氧化氮的吸收率,可采取的措施为
(答2项)
 答案:
答案: 20-4(11 分)
20-4(11 分)

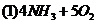
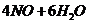 (3分)
(3分) (2)提高氨的转化率和一氧化氮的转化率(2分)
(2)提高氨的转化率和一氧化氮的转化率(2分) (3)增大单位质量的催化剂与反应物的接触面积(2分)
(3)增大单位质量的催化剂与反应物的接触面积(2分)
 (4)
(4)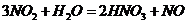 加压 降温
加压 降温
解析:本题较为基础,主要考查硝酸的工业制法。
12.(09上海卷 31)烟气中
31)烟气中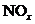 是NO和
是NO和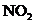 的混合物(不含
的混合物(不含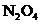 )。
)。
 (1)根据废气排放标准,
(1)根据废气排放标准,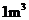 烟气最高允许含400mg
烟气最高允许含400mg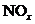 。若
。若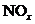 中NO质量分数为0.85,则
中NO质量分数为0.85,则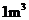 烟气中最高允许含NO__________L(标准状况,保留2位小数)。
烟气中最高允许含NO__________L(标准状况,保留2位小数)。
 (2)工业上通常用溶质质量分数为0.150的
(2)工业上通常用溶质质量分数为0.150的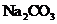 水溶液(密度1.16g/mL)作为
水溶液(密度1.16g/mL)作为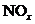 吸收剂,该碳酸钠溶液物质的量浓度为____________mol/L(保留2位小数)。
吸收剂,该碳酸钠溶液物质的量浓度为____________mol/L(保留2位小数)。
 (3)已知:
(3)已知: 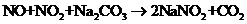 ①
①

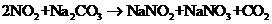 ②
②

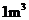 含2000mg
含2000mg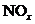 的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,
的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,
吸收后的烟气__
_____排放标准(填“符合”或“不符合”),理由:____________________。
 (4)加入硝酸可改变烟气中NO和NO2的比,反应为:
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:
 NO+2HNO3→3NO2+H2O
NO+2HNO3→3NO2+H2O
 当烟气中
当烟气中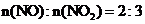 时,吸收率最高。
时,吸收率最高。

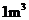 烟气含2000mg
烟气含2000mg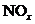 ,其中
,其中 。
。
 计算:(i)为了达到最高吸收率,
计算:(i)为了达到最高吸收率,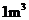 烟气需用硝酸的物质的量(保留3位小数)。
烟气需用硝酸的物质的量(保留3位小数)。
 (ii)
(ii)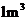 烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)。
烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)。
答案: (1)0.25
(1)0.25 (2)1.64
(2)1.64 (3)不符合 因吸收后烟气总体积减小,
(3)不符合 因吸收后烟气总体积减小,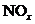 含量仍超过
含量仍超过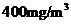
 (4)(i)
(4)(i)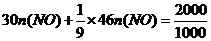
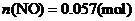

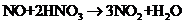

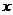
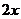


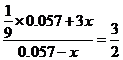
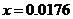
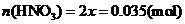
 (ii)
(ii)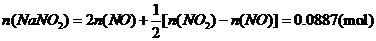

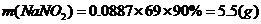
解析:(1)1L烟气中最高允许含NO质量为400×10-3g×0.85=0.34g
其体积为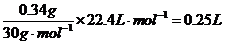
(2)此题考查物质的量浓度与质量分数的换算,可直接利用公式求解。
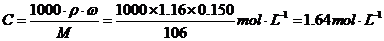
(3)若烟气中的其他成分不被吸收,刚好达到排放标准,但烟气中的CO2等酸性气体也能被吸收,所以吸收后烟气中NOx的含量仍超标。
11.(09四川卷27)(15分)已知A-O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。
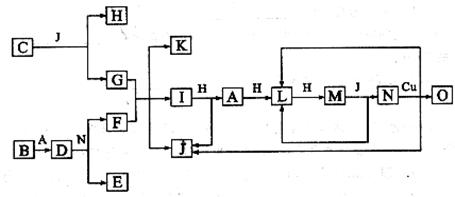
请回答下列问题:
(1)组成B单质的元素位于周期表第______________周期,第_______________族。化合物C的电子式为_________________________。
(2)J的沸点比硒化氢(H2Se)的沸点高,其原因是_________________。
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:________________。
(4)写出D与足量的N反应生成E和F的化学方程式:_____________________。
(5)上图中,在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有_______个。
答案:(1)三(1分)II A (1分) (2分)
(2分)
(2)水分子之间存在氢键且比硒化氢的分子间作用力强(2分)
(3)4NH3+3O2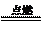 2N2+6H2O(3分)
2N2+6H2O(3分)
(4)Mg3N2+8HNO3=Mg(NO3)2+2NH4NO3(3分)
(5)2(3分)
 [解析]框图推断题抓住题眼如根据B是由短周期元素组成的单质,B与冷水缓慢反应,与沸水迅速反应,放出氢气,可判断B为金属镁。D是一种离子化合物,其阴阳离子的个数比为2:3,就可以判断D为氮化镁,所以A为氮气。 C为淡黄色固体化合物, 判断为过氧化钠。O能与G的水溶液反应生成蓝色沉淀,说明有氢氧化铜生成。通过分析可得:A:氮气B:镁C:过氧化钠D:二氮化三镁E:硝酸镁F:硝酸铵G:氢氧化钠H:氧气I:氨气J:水K:硝酸钠L:一氧化氮M:二氧化氮N:硝酸O:硝酸铜
[解析]框图推断题抓住题眼如根据B是由短周期元素组成的单质,B与冷水缓慢反应,与沸水迅速反应,放出氢气,可判断B为金属镁。D是一种离子化合物,其阴阳离子的个数比为2:3,就可以判断D为氮化镁,所以A为氮气。 C为淡黄色固体化合物, 判断为过氧化钠。O能与G的水溶液反应生成蓝色沉淀,说明有氢氧化铜生成。通过分析可得:A:氮气B:镁C:过氧化钠D:二氮化三镁E:硝酸镁F:硝酸铵G:氢氧化钠H:氧气I:氨气J:水K:硝酸钠L:一氧化氮M:二氧化氮N:硝酸O:硝酸铜
 [点评]
[点评] 本题是典型的无机框图题,主要考查元素及其化合物的性质、化学方程式书写、氧化还原反应。
本题是典型的无机框图题,主要考查元素及其化合物的性质、化学方程式书写、氧化还原反应。
10.(09北京卷27)(14分)某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将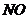 氧化成
氧化成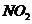 ,而稀硝酸不能氧化
,而稀硝酸不能氧化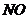 。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
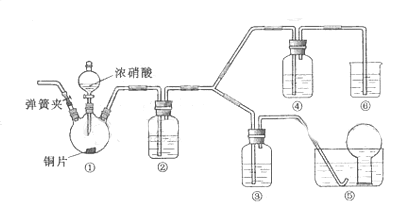
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与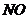 反应,能与
反应,能与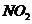 反应
反应
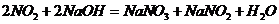
(1) 实验应避免有害气体排放到空气中,装置③、④、⑥中乘放的药品依次是
(2) 滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
(3) 装置①中发生反应的化学方程式是
(4) 装置②的作用是 ,发生反应的化学方程式是
(5) 该小组得出的结论依据的试验现象是
(6) 试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别涉及了一下4个试验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)
a. 加热该绿色溶液,观察颜色变化
b. 加水稀释绿色溶液,观察颜色变化
c. 向该绿色溶液中通入氮气,观察颜色变化
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体,观察颜色变化
答案: (1)3mol/L稀硝酸、浓硝酸、氢氧化钠溶液
(1)3mol/L稀硝酸、浓硝酸、氢氧化钠溶液
 (2)通入CO2一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内
(2)通入CO2一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内
 (3)Cu + 4HNO3(浓)= Cu(NO3)2 + 2NO2↑ + 2H2O
(3)Cu + 4HNO3(浓)= Cu(NO3)2 + 2NO2↑ + 2H2O
 (4)将NO2转化为NO 3NO2 +
H2O =2HNO3 + NO
(4)将NO2转化为NO 3NO2 +
H2O =2HNO3 + NO
 (5)装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
(5)装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
 (6)a c d
(6)a c d
 [解析]本题主要考查HNO3的性质、化学基本实验设计和评价能力。(1)根据装置特点和实验目的,装置⑤是收集NO,装置⑥中盛放NaOH溶液吸收NO2,因为要验证稀HNO3不能氧化NO,所以装置③中应该盛放稀硝酸。
[解析]本题主要考查HNO3的性质、化学基本实验设计和评价能力。(1)根据装置特点和实验目的,装置⑤是收集NO,装置⑥中盛放NaOH溶液吸收NO2,因为要验证稀HNO3不能氧化NO,所以装置③中应该盛放稀硝酸。
 (2)由于装置中残存的空气能氧化NO而对实验产生干扰,所以滴加浓HNO3之前需要通入一段时间CO2赶走装置中的空气,同时也需将装置⑤中导管末端伸入倒置的烧瓶内防止反应产生的NO气体逸出。
(2)由于装置中残存的空气能氧化NO而对实验产生干扰,所以滴加浓HNO3之前需要通入一段时间CO2赶走装置中的空气,同时也需将装置⑤中导管末端伸入倒置的烧瓶内防止反应产生的NO气体逸出。
 (3)Cu与浓HNO3反应生成Cu(NO3)2、NO2、H2O:Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑ +2 H2O。
(3)Cu与浓HNO3反应生成Cu(NO3)2、NO2、H2O:Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑ +2 H2O。
 (4)装置②中盛放H2O,使NO2与H2O反应生成NO:3NO2 + H2O=2HNO3 + NO。
(4)装置②中盛放H2O,使NO2与H2O反应生成NO:3NO2 + H2O=2HNO3 + NO。
 (5)NO通过稀HNO3溶液后,若无红棕色NO2产生,说明稀HNO3不能氧化NO,所以盛放稀HNO3装置的液面上方没有颜色变化即可说明之。装置④中盛放的是浓HNO3,若浓HNO3能氧化NO则装置④液面的上方会产生红棕色气体。
(5)NO通过稀HNO3溶液后,若无红棕色NO2产生,说明稀HNO3不能氧化NO,所以盛放稀HNO3装置的液面上方没有颜色变化即可说明之。装置④中盛放的是浓HNO3,若浓HNO3能氧化NO则装置④液面的上方会产生红棕色气体。
 (6)要证明是Cu(NO3)2浓度过低或是溶解了NO2导致装置①中溶液呈绿色,一是可设计将溶解的NO2赶走(a、c方案)再观察颜色变化。二是增加溶液中Cu(NO3)2溶液的浓度(d方案)观察反应后的颜色变化。
(6)要证明是Cu(NO3)2浓度过低或是溶解了NO2导致装置①中溶液呈绿色,一是可设计将溶解的NO2赶走(a、c方案)再观察颜色变化。二是增加溶液中Cu(NO3)2溶液的浓度(d方案)观察反应后的颜色变化。
9. (09全国卷Ⅰ29)(15分)已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。回答下列问题:
(1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是 ;
(2)Q的具有相同化合价且可以相互转变的氧化物是 ;
(3)R和Y形成的二元化合物中,R呈现最高化合价的化合物的化学式是 ;
(4)这5个元素的氢化物分子中,①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式) ,其原因是
;
②电子总数相同的氢化物的化学式和立体结构分别是
;
(5)W和Q所形成的结构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCL气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是
。
答案: (1)原子晶体。(2)NO2和N2O4(3)As2S5。(4)①NH3> AsH3 > PH3,因为前者中含有氢键,后两者构型相同,分子间作用力不同;②电子数相同的有SiH4、PH3和H2S结构分别为正四面体,三角锥和V形。(5)SiCl4 + 4NH3 = Si(NH2)4
+ 4HCl,3Si(NH2)4 =
8NH3 + Si3N4
(1)原子晶体。(2)NO2和N2O4(3)As2S5。(4)①NH3> AsH3 > PH3,因为前者中含有氢键,后两者构型相同,分子间作用力不同;②电子数相同的有SiH4、PH3和H2S结构分别为正四面体,三角锥和V形。(5)SiCl4 + 4NH3 = Si(NH2)4
+ 4HCl,3Si(NH2)4 =
8NH3 + Si3N4
 解析:本题可结合问题作答。W的氯化物为正四体型,则应为SiCl4或CCl4,又W与Q形成高温陶瓷,故可推断W为Si。(1)SiO2为原子晶体。(2)高温陶瓷可联想到Si3N4,Q为N,则有NO2与N2O4之间的相互转化关系。(3)Y的最高价氧化的的水化物为强酸,且与Si、N等相邻,则只能是S。R为As,所以R的最高价化合物应为As2S5。(4)显然x为P元素。①氢化物沸点顺序为NH3> AsH3
> PH3,因为前者中含有氢键后两者构型相同,分子间作用力不同。②SiH4、PH3和H2S的电子数均为18。,结构分别为正四面体,三角锥和V形。(5)由题中所给出的含字母的化学式可以写出具体的物质,然后配平即可。
解析:本题可结合问题作答。W的氯化物为正四体型,则应为SiCl4或CCl4,又W与Q形成高温陶瓷,故可推断W为Si。(1)SiO2为原子晶体。(2)高温陶瓷可联想到Si3N4,Q为N,则有NO2与N2O4之间的相互转化关系。(3)Y的最高价氧化的的水化物为强酸,且与Si、N等相邻,则只能是S。R为As,所以R的最高价化合物应为As2S5。(4)显然x为P元素。①氢化物沸点顺序为NH3> AsH3
> PH3,因为前者中含有氢键后两者构型相同,分子间作用力不同。②SiH4、PH3和H2S的电子数均为18。,结构分别为正四面体,三角锥和V形。(5)由题中所给出的含字母的化学式可以写出具体的物质,然后配平即可。
8.(09宁夏卷7) 将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为
A.NO2 B.N2O2 C.N2O D.N2O4
答案:A 解析:根据2NxOy+2yCu=2yCuO+xN2,以及题中数据反应后气体体积为反应前气体体积的一半,可以得到x=1,因此只有A选项符合题意。
解析:根据2NxOy+2yCu=2yCuO+xN2,以及题中数据反应后气体体积为反应前气体体积的一半,可以得到x=1,因此只有A选项符合题意。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com