
9.下列离子方程式正确的是( )
A.向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
C.向FeCl3溶液中加入铜片:Fe3++Cu=Fe2++Cu2+
D.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-==CO2↑+H2O
8.下列各组离子在给定条件下可能大量共存的是( )
A.在酸性溶液中:NH4+、K+、S2O32-、Cl-
B.有SO42-存在的溶液中:H+、Mg2+、Ba2+、I--
C.在碱性溶液中:K+、SO32-、Br-、S2-
D.下列无色溶液中:Na+、S2-、AlO2-、CrO42-
7.关于反应:①2C2H2(g)
+ 5O2(g) = 4CO2 (g) + 2H2O(l) ΔH= -2600kJ/mol ; ②2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol ;
②2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol ; ③CH4(g)+H2O(g)
=CO(g)+3H2(g) ΔH=+216 kJ/mol下列叙述正确的是( )
③CH4(g)+H2O(g)
=CO(g)+3H2(g) ΔH=+216 kJ/mol下列叙述正确的是( )
A.CO的燃烧热为-283 kJ/mol 
B.在③反应时,若加入催化剂,可以使ΔH减小
C.若有3.2g CH4与足量水蒸汽按③反应,则放出热量是43.2 kJ
D.若生成相同质量的CO2,则放出的热量C2H2大于CO
6.向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.24mol B.0.21mol C.0.16mol D.0.14mol
5.我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl NaHCO3↓+NH4Cl的反应原理制备纯碱。下面是在实验室进行模拟实验的生产流程示意图:
NaHCO3↓+NH4Cl的反应原理制备纯碱。下面是在实验室进行模拟实验的生产流程示意图:
 则下列叙述错误的是( )
则下列叙述错误的是( )
A.A气体是NH3,B气体是CO2
B.把纯碱及第Ⅲ步得到的晶体与某些固体酸性物质(如酒石酸)混合可制得发酵粉
C.纯碱可广泛地用于玻璃、制皂、造纸、纺织等工业中
D.第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶
4.下列实验操作中错误的是( )
A.蒸发操作时,当有大量晶体析出时,才能停止加热
B.蒸馏操作时,应使温度计水银球浸在液面之下
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应使溶质在萃取剂中的溶解度远大于在水中的溶解度
3.下列叙述正确的是( )
A.金属与盐溶液的反应都是置换反应
B.阴离子都只有还原性
C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物
D. 国庆60周年放的烟花是某些金属元素焰色反应所呈现出来的色彩
A.食盐水
B.清洁剂 C.次氯酸钠
D.70%酒精
2.下列说法中正确的是( )
A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
C.电离出的阳离子都是H+的化合物一定是酸
D.沼气、天然气和水煤气分别属于化石能源、可再生能源和二次能源
22.某一温度下将1 mol N2和4mol H2导入一体积为2L的密闭容器中,测得容器内压强为40Mpa,当20 min后,反应达到平衡,测得NH3在混合气体里占25%(体积含量)。求:(1)N2的平衡转化率; (2)H2的平均反应速率; (3)平衡时容器内的压强。
重庆市第二外国语学校
2009--2010学年上学期期中考试
21、同温同压下,在甲、乙两个等体积的
干燥圆底烧瓶中分别充满 、
、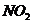
进行喷泉实验。如图:
(1)实验室制备 的化学方程式为:
的化学方程式为:
____________________________________
(2)形成喷泉后,甲烧瓶内液体呈______色,原因是_______________________(用化学方程式说明);乙烧瓶内液体呈______色,原因是________________________(用化学方程式说明)
(3)喷泉停止后,甲烧瓶中溶质的物质的量浓度_____(填“大于”“小于”或“等于”)乙烧瓶中溶质的物质的量浓度。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com