
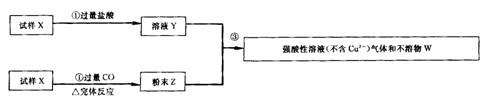
17.试样X由氧化亚铁和氧化铜组成.取质量相等的两份试样按图3-3所示进行实验:
(1)请写出步骤③中所发生的全部反应的离子方程式.
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶液物W的质量是M,则
每份试样X中氧化铜的质量为 (用m表示)
D.奥赛一瞥
16.①向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式
.
②在以中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式
.
15.向50毫升,18摩/升H2SO4溶液中加入足量铜片并加热.充分反应后,被还原的H2SO4
的物质的量( )
A.小于0.45摩 B.等于0.45摩
C.在0.45摩和0.90摩之间 D.大于0.90摩
C.能力训练
14.使用浓H2SO4时,若不慎沾在皮肤上,正确的清洗方法是( )
A.用饱和的NaOH溶液中和
B. 用大量水冲洗,然后用3%-5%碳酸氢钠溶液清洗,并涂上碳酸氢钠溶液
C. 用干布擦,然后用水冲洗
D.用稀氨水冲洗
13.等物质的量的氯气和二氧化硫气体通入滴有紫色石蕊试液的氯化钡溶液中,以下叙述正确的是( )
A.无沉淀产生,溶液变成无色 B.产生BaSO3沉淀,溶液变成红色
C.产生BaSO4白色沉淀,溶液变色成红色 D.产生BaSO3白色沉淀,溶液变成无色
12.下列说法正确的是( )
A.能使石灰水变浑浊的气体一定是CO2
B. 能使品红溶液褪色,将其煮沸又变红的无色气体一定为SO2
C. 用NaHSO3,Na2SO3与浓H2SO4反应都可产生SO2
D.某酸性溶液经分析含大量S2-,SO42-,MnO4-
11.将2.5毫升0.1摩/升的Na2S溶液,1毫升0.1摩/升的Na2SO3溶液,7毫升0.1摩/升盐酸相混和于一密封容器内,体系内硫元素以各形式存在的相对含量是( )
A.H2S>HS->S2->S B.H2S> S2->S>HS-
C.S>H2S>HS->S2- D. S> S2-> H2S>HS-
10.赤热的炭与浓硫酸共热产生气体能使下列物质的水溶液变浑浊的为( )
A.H2S溶液 B.CaCl2溶液 C.溴单质的水溶液 D.Ca(OH)2溶液
B.提高训练
9.下列离子方程式不正确的是( )
① 碳酸氢钙溶液遇盐酸:Ca(HCO3)2+2H+ Ca2++2H2O+2CO2↑
碳酸氢钙溶液遇盐酸:Ca(HCO3)2+2H+ Ca2++2H2O+2CO2↑
 ②H2S通入大量NaOH溶液中:OH-+H2S HS-+H2O
②H2S通入大量NaOH溶液中:OH-+H2S HS-+H2O
 ③Ba(OH)2溶液中通入足量的SO2气体:Ba2++SO2+H2O BaSO3↓+H2O
③Ba(OH)2溶液中通入足量的SO2气体:Ba2++SO2+H2O BaSO3↓+H2O
 ④实验室制硫化氢:S2-+2H+ H2S↑
④实验室制硫化氢:S2-+2H+ H2S↑
A.①②③④ B.②④ C.②③④ D.①③
8.把浓硫酸滴入浓盐酸中,会有氯化氢气体逸出,对此现象的合理解释是( )
A.氯化氢难溶于水
B. 浓硫酸有脱水性
C. 浓硫酸是一种高沸点的酸
D.浓硫酸溶于水放出大量的热,降低了氯化氢的溶解度
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com