

1、 下列反应的离子方程式书写正确的是( )
A、 铁和稀硫酸反应:2Fe+6H+ = 2Fe3++3H2↑
B、氯化亚铁溶中通入氯气:Fe2++Cl2=Fe3++Cl-
C、往水中投入一小块金属钠:Na+2H2O=Na++2OH-+H2个
D、铝粉溶于NaOH溶液中:2Al +2OH-+2H2O=2AlO2-+3H2↑
18、若以ω1和ω2分别表示浓度为a mol·L-1和b mol·L-1氨水的质量分数,且知b=2a,则
下列推断正确的是( )
A.ω2 =2ω1 B.ω1=2ω2 C.ω2>2ω1 D.ω1<ω2<2ω1
17.某结晶水合物化学式X·nH2O,其相对分子质量为M,在25℃时,Ag该结晶水合物溶于Bg水中即可达到饱和,形成密度为D g/cm3的饱和饱和溶液VmL,下列表达式中不正确的是( )
A.该饱和溶液的质量分数为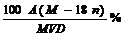
B.X在25℃时的溶解度为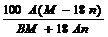
C.该饱和溶液的物质的量浓度为
D.该饱和溶液的物质的量浓度为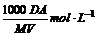
16.已知一种盐酸的物质的量浓度为M1,密度为d1g/cm3,体积为V1L,另一种盐酸的物质的量浓度为M2,密度为d2g/cm3,体积为V2L,两者混合后,溶液的密度为d3g/cm3,用数学式表示混合溶液的物质的量浓度是( )
A.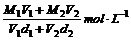 B.
B.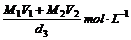
C.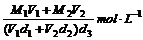 D.
D.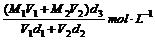
15.将标准状况下,将VL HX气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶液的物质的量浓度(mol/L)为( )
A.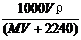 B.
B.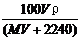 C.
C.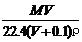 D.100VρM(MV+2240)
D.100VρM(MV+2240)
14.200mL 硫酸铁溶液中含有Fe3+为28g,取20mL溶液加水稀释到400 mL,则稀释后溶液中SO42-的物质的量浓度是( )
A.1/16mol/L B.3/16mol/L C.1/64mol/L D.0.2mol/L
13.某实验室用下列溶质配制一种混合溶液,已知溶液中:
(K+)=(Cl-)=1/2(Na+)=(SO42-),则其溶质可能是( )
A.CuCl2、Na2SO4 B.KCl、Na2SO4、NaCl
C.NaCl、Na2SO4、K2SO4 D.KCl、K2SO4、Na2SO4
12.分别用0.05mol/L的AgNO3溶液20mL与相同体积的下列溶液恰好完全反应。则物
质的量浓度最大的是( )
A.NaCl B.MgCl2 C.BaCl2 D.AlCl3
11.将0.1mol/L的K2SO4溶液、0.2mol/L的Al2(SO4)2溶液和纯水混合,要使混合液中的K+、Al3+、SO42-的浓度分别为0.1mol/L、0.1mol/L、0.2mol/L,则所取的K2SO4溶液、Al2(SO4)3溶液、水三者体积比约为( )
A.1:1:1 B.1:2:3 C.2:1:1 D.4:1:2
10.已知某饱和溶液的:①溶液的质量;②溶液的体积;③溶剂的质量;④溶质的摩尔质量;⑤溶液的密度;⑥溶质的溶解度。从以上条件的组合中不能用来计算该饱和溶液的物质的量浓度的是 ( )
A.①②④ B.①②③④ C.①②④⑥ D.④⑤⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com