
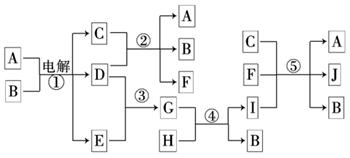
23.(8分)如下图所示物质间的相互转变关系,反应①在工业上可用来生产化合物C,反应⑤在工业上可生产化合物J(Na2FeO4),反应①、②、④和⑤均是在水溶液中进行的反应.常温下D、E、G均是气体,B是无色液体;F的水溶液可作为杀菌消毒剂;H是一种铁矿石的主要成分,它由两种元素组成,且其中铁元素的质量分数为70%.
请回答下列问题:
(1)写出F的化学式:________________.
(2)人们将反应①涉及的化学工业称为 ________________.
(3) 写出B与D反应的离子方程式________________________________________.
(4) 写出反应④的离子方程式______________________________________________.
(5)写出反应⑤的离子方程式______________________________________________.
(6)高铁酸钠(Na2FeO4)被人们认为是一种“绿色环保高效”的净水剂,其原因为:
①Na2FeO4具有强氧化性可杀菌消毒;
②___________________________________________________________________
22. (9分)A、B、C、D均为中学化学中常见的物质,它们之间的转化关系如下图(部分产物已略去):
(9分)A、B、C、D均为中学化学中常见的物质,它们之间的转化关系如下图(部分产物已略去):
试回答:
(1)若D是具有氧化性的单质,A元素属于主族金属元素,则A为________(填元素名称).
(2)若D是金属,C溶液在储存时应加入少量D,其理由是(用必要的文字和离子方程式表示)____________________________________________________;D在潮湿的空气中易发生吸氧腐蚀,写出腐蚀时原电池正极的电极反应式:____________________________.
(3)若A、B、C为含同一种金属元素的无机化合物,在溶液中A和C反应生成 B.
请写出B转化为C的所有可能的离子方程式:________________________________、___________________________________.
21.(8分)某溶液仅含下表离子中的5种(不考虑水的电离及离子的水解)且各种离子物质的量均为1mol。
|
阳离子 |
Na+
Mg2+ Fe3+ Al3+ Fe2+ |
|
阴离子 |
OH- CO32- Cl- NO3- SO42- |
①若向溶液中加入KSCN溶液无明显变化;
②若向原溶液中加入稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,且溶液中阴离子种类不变;
请推断:
(1)原溶液中含有阳离子: ;含有阴离子: ;
(2)向原溶液中加入足量稀盐酸发生反应的离子方程式: ;
(3)若向原溶液中加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为 g。
20.将a g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得参加反应的HCl为0.08 mol,放出标准状况下气体0.224 L.则下列判断中正确的是( )
A.无法计算原混合物的质量a
B.原混合物中n(Fe)∶n(Fe2O3)=2∶1
C.向溶液中滴入KSCN溶液,显红色
D.此时溶液中Fe2+和Fe3+的物质的量之比为3∶1
19.常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1 mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是 ( )

A.原合金质量为0.92 g B.产生氢气0.04mol
C.图中m值为1.56 g D.图中V2为60 mL
18.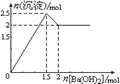 右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是 ( )
右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是 ( )
A.MgSO4
B.Al2(SO4)3
C.KAl(SO4)2
D.NaAlO2
17.在标准状况下,将V L A气体(摩尔质量是M g/mol)溶于0.1 L水中,所得溶液的密度为d g/cm3,则此溶液的物质的量浓度为 ( )
A. B. C. D.
16.下列叙述正确的是
A.与V L CO具有相同分子数的CO2的体积一定是V L
B.所含原子数相等的CO与CO2的密度之比为21∶22
C.所含原子数相等的CO与CO2的密度之比为7∶11
D.与28 g CO具有相同分子数的CO2的质量一定是44 g
15.CsICl2是一种碱金属的多卤化物,这类物质在化学反应中既可表现氧化性又可表现还原性,有关该物质的说法正确的是 ( )
A.Cs显+3价,I 、Cl 均显-1
B.Cs显 +1价,Cl显+1价,I显-1价、
C.在CsICl2溶液中通入Cl2 ,有单质碘生成
D.在CsICl2溶液中通入SO2气体,有硫酸生成
14.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+===2As+3SnCl+6M,关于该反应的说法中正确的组合是 ( )
①氧化剂是H3AsO3 ②还原性:Cl->As ③每生成7.5 g As,还原剂失去的电子为0.3 mol ④M为OH- ⑤SnCl是氧化产物
A.①③⑤ B.①②④⑤ C.①②③④ D.①③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com