
15ЃЎ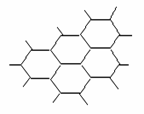 (1)ЖўбѕЛЏЙшОЇЬхжаЃЌУПИіЙшдзгжмЮЇга________ИібѕдзгЃЌУПИібѕдзгжмЮЇга________ИіЙшдзгЃЌЙшбѕдзгИіЪ§БШЮЊ________ЁЃ
(1)ЖўбѕЛЏЙшОЇЬхжаЃЌУПИіЙшдзгжмЮЇга________ИібѕдзгЃЌУПИібѕдзгжмЮЇга________ИіЙшдзгЃЌЙшбѕдзгИіЪ§БШЮЊ________ЁЃ
(2)ЪЏФЋОЇЬхНсЙЙШчЭМЫљЪОЃЌУПвЛВугЩЮоЪ§Иіе§СљБпаЮЙЙГЩЁЃ
ЦНОљУПИіе§СљБпаЮЫљеМгаЕФЬМдзгЪ§ФПЮЊ________ЁЂ
ЦНОљУПИіе§СљБпаЮЫљеМгаЕФЙВМлМќЪ§ФПЮЊ________ЁЃ
[ЬНЫїЬсИп]
14ЃЎдкН№ИеЪЏЕФЭјзДНсЙЙжа,КЌгагЩЙВМлМќаЮГЩЕФЬМдзгЛЗ,ЦфжазюаЁЕФЛЗЩЯгаЁЁЁЁ (ЬюЪ§зж)ИіЬМдзг,УПИіЬМдзгЩЯЕФШЮвтСНИіC-CМќЕФМаНЧЖМЪЧЁЁЁЁ (ЬюНЧЖШ).
13ЃЎТШЛЏФЦЪєгкЁЁЁЁ ОЇЬхЃЌЖўбѕЛЏЙшЪєгк ЁЁ ЁЁОЇЬхЃЌNaClКЭSiO2ВЂВЛДњБэЫќУЧЕФ ЁЁЁЁ ЪНЃЌжЛФмБэЪОзщГЩОЇЬхЕФИїжжЮЂСЃЕФЁЁЁЁЁЁ ЁЃ
12ЃЎЯТСаЮяжЪЕФШлЕуОљАДгЩИпЕНЕЭЕФХХСаЃЌЦфдвђЪЧгЩгкМќФмгЩДѓЕНаЁХХСаЕФЪЧ (ЁЁЁЁ )
AЃЎТСЁЂФЦЁЂИЩБљЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎН№ИеЪЏЁЂЬМЛЏЙшЁЂОЇЬхЙш
CЃЎЕтЛЏЧтЁЂфхЛЏЧтЁЂТШЛЏЧтЁЁЁЁЁЁ DЃЎЖўбѕЛЏЙшЁЂЖўбѕЛЏЬМЁЂвЛбѕЛЏЬМ
11ЃЎЙЬЬхШлЛЏЪББиаыЦЦЛЕЗЧМЋадЙВМлМќЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎБљЁЁЁЁЁЁЁЁ BЃЎОЇЬхЙшЁЁЁЁЁЁ CЃЎфхЕЅжЪЁЁЁЁ DЃЎЖўбѕЛЏЙш
10ЃЎЯТСаа№Ъіжае§ШЗЕФЪЧЃК (ЁЁЁЁ )
AЃЎдзгОЇЬхжаЃЌЙВМлМќЕФМќФмдНДѓЃЌШлЗаЕудНИп
BЃЎЗжзгОЇЬхжаЃЌЗжзгМфЕФзїгУСІдНДѓЃЌИУЗжзгдНЮШЖЈ
CЃЎЗжзгОЇЬхжаЃЌЙВМлМќЕФМќФмдНДѓЃЌШлЗаЕудНИп
DЃЎФГОЇЬхШмгкЫЎКѓЃЌПЩЕчРыГіздгЩвЦЖЏЕФРызгЃЌИУОЇЬхвЛЖЈЪЧРызгОЇЬх
9ЃЎЗжЮіЯТСаИїЮяжЪЕФЮяРэаджЪЃЌХаЖЯЦфЙЬЬЌВЛЪєгкЗжзгОЇЬхЕФЪЧЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎЬМЛЏТСЃЌЛЦЩЋОЇЬхЃЌШлЕу2200ЁцЃЌШлШкЬЌВЛЕМЕч
BЃЎфхЛЏТСЃЌЮоЩЋОЇЬхЃЌШлЕу98ЁцЃЌШлШкЬЌВЛЕМЕч
CЃЎЮхбѕЛЏЗАЃЌЮоЩЋОЇЬхЃЌШлЕу19.5ЁцЃЌвзШмгкввДМЁЂТШЗТЁЂБћЭЊжа
DЃЎфхЛЏМиЃЌЮоЩЋОЇЬхЃЌШлШкЪБЛђШмгкЫЎжаЖМФмЕМЕч
8ЃЎЫЎЕФЗаЕуЪЧ100ЁцЃЌСђЛЏЧтЕФЗжзгНсЙЙИњЫЎЯрЫЦЃЌЕЋЫќЕФЗаЕуШДКмЕЭЃЌЪЧ -60.7ЁуCЃЌв§Ц№етжжВювьЕФжївЊдвђЪЧЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎЗЖЕТЛЊСІЁЁЁЁ ЁЁЁЁBЃЎЙВМлМќЁЁЁЁЁЁ ЁЁЁЁCЃЎЧтМќЁЁЁЁЁЁЁЁЁЁ DЃЎЯрЖдЗжзгжЪСП
7ЃЎSiCl4ЕФЗжзгНсЙЙгыCCl4РрЫЦЃЌЖдЦфзіГіШчЯТЭЦЖЯЃКЂйSiCl4ОЇЬхЪЧЗжзгОЇЬхЃЛЂкГЃЮТГЃбЙSiCl4ВЛЪЧЦјЬхЃЛЂлSiCl4ЗжзгЪЧгЩМЋадМќЙЙГЩЕФЗЧМЋадЗжзгЃЛЂмSiCl4ШлЕуИпгкCCl4ЁЃЦфжае§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎжЛгаЂйЁЁЁЁЁЁЁЁ BЃЎжЛгаЂйЂкЁЁЁЁЁЁЁЁ CЃЎжЛгаЂкЂлЁЁЁЁЁЁ DЃЎЂйЂкЂлЂм
6ЃЎЯТСаЫЕЗЈжаЃЌе§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎБљШмЛЏЪБЃЌЗжзгжаH-OМќЗЂЩњЖЯСб
BЃЎдзгОЇЬхжаЃЌЙВМлМќЕФМќГЄдНЖЬЃЌЭЈГЃШлЕуОЭдНИп
CЃЎЗжзгОЇЬхжаЃЌЙВМлМќМќФмдНДѓЃЌИУЗжзгЕФШлЗаЕуОЭдНИп
DЃЎЗжзгОЇЬхжаЃЌЗжзгМфзїгУСІдНДѓЃЌдђЗжзгдНЮШЖЈ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com