

25.在25℃、101KPa时,____________________________时所放出的热量,叫做该反应的燃烧热。在25℃、101KPa时,1g乙醇完全燃烧生成CO2和液态水时放热29.713kJ,则能表示乙醇燃烧热的热化学方程式为_________________________________________________。
24.在一定温度下容积固定的密闭容器中,进行反应H2(g)+Br2(g)
 2HBr(g)。已知加入1 mol H2和2 mol Br2时,达到平衡后生成a mol HBr。在相同条件下,起始时加入H2、Br2、HBr的物质的量分别为x、y、z(均不为0),如果仍保持平衡时各组分的质量分数不变,以下判断正确的是
2HBr(g)。已知加入1 mol H2和2 mol Br2时,达到平衡后生成a mol HBr。在相同条件下,起始时加入H2、Br2、HBr的物质的量分别为x、y、z(均不为0),如果仍保持平衡时各组分的质量分数不变,以下判断正确的是

A.x、y应满足的关系是y = 2x

B.x、y、z应满足的关系是4x + z =
2y
C.达到平衡时HBr物质的量为(2y – x)a mol 
D.达到平衡时HBr物质的量一定为a mol
23.将1mol SO2和1mol O2通入恒容密闭容器中,在一定条件下反应达到平衡时,SO3为0.3 mol。此时若移走0.5 mol O2和0.5 mol SO2,则反应达到新的平衡时,SO3的物质的量是

A. 0.3 mol
B.0.15 mol C.小于0.15 mol D.大于0.15 mol小于0.3 mol
22.下列各组离子在指定的环境中能大量存在的是
A.pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl-
B.能使石蕊试纸变蓝色的溶液中:Na+、K+、S2-、CO32-
C.加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3-
D.水电离出的c(H+)=1×10-12mol/L的溶液中:K+、Na+、Cl-、HCO3-
21.体积固定的密闭容器内进行可逆反应:N2O4(g)  2NO2
(g)。下列不能说明该反应已经达到反应限度的是:①N2O4
2NO2
(g)。下列不能说明该反应已经达到反应限度的是:①N2O4 的消耗速率与NO2的生成速率之比为1:2
②NO2的生成速率与NO2消耗速率相等
③气体的压强不再变化 ④气体的质量不再变化 ⑤NO2的物质的量浓度不再改变
⑥气体的颜色不再加深 ⑦气体的平均相对分子质量不再变化 ⑧气体的密度不再变化
的消耗速率与NO2的生成速率之比为1:2
②NO2的生成速率与NO2消耗速率相等
③气体的压强不再变化 ④气体的质量不再变化 ⑤NO2的物质的量浓度不再改变
⑥气体的颜色不再加深 ⑦气体的平均相对分子质量不再变化 ⑧气体的密度不再变化
A.②③⑥⑦
 B.①④⑧
C.只有①④
D.只有⑦⑧
B.①④⑧
C.只有①④
D.只有⑦⑧
20. 在一固定容积的密闭容器中充入2 mol A和2 mol B,发生反应 2
A(g ) + B(g)  x C(g ),达平衡后,C的体积分数为w,若维持容器体积和温度不变,按0.6 mol A、 1.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w,则x 值为
x C(g ),达平衡后,C的体积分数为w,若维持容器体积和温度不变,按0.6 mol A、 1.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w,则x 值为
A.1 B.2
C.2或3 D.4
19.一氧化氮和一氧化碳都是汽车尾气里的有害物质,它们能缓慢地发生如下反应:2NO(g)+2CO(g)  N2(g)+2CO2(g)(正反应为放热反应)。现利用此反应,拟设计一种环保装置以减轻汽车尾气对大气的污染。下列设计方案可以提高尾气处理效果的是
N2(g)+2CO2(g)(正反应为放热反应)。现利用此反应,拟设计一种环保装置以减轻汽车尾气对大气的污染。下列设计方案可以提高尾气处理效果的是
A.不断向装置中鼓入空气
B.提高反应装置的温度
C.降低反应装置的压强
D.在反应装置中装入碱石灰
18.某温度下,C(s)和H2O(g)在密闭容器中发生下列反应:
C(s)+ H2O(g )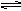 CO(g) +
H2(g);CO(g) + H2O(g)
CO(g) +
H2(g);CO(g) + H2O(g)
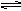 CO2(g) + H2(g)
CO2(g) + H2(g)
当反应达到平衡时,测得c(H2)=
1.9 mol/L , c(CO)= 0.1 mol/L ,则CO2 的浓度为
A.0.1 mol/L B.0.9 mol/L C.1.9 mol/L D.1.8 mol/L
17.下列叙述正确的是
A.95℃纯水的pH<7,说明加热后可导致水呈酸性
B.pH=3的醋酸溶液稀释至10倍后pH=4
C.0.2mol/L的盐酸与等体积水混合后pH=1 
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
16.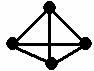 最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知断裂1molN-N吸收167kJ热量,生成1mol
N≡N放出942kJ热量。根据以上信息和数据,则由N2气体生成1mol气态N4的△H为
最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知断裂1molN-N吸收167kJ热量,生成1mol
N≡N放出942kJ热量。根据以上信息和数据,则由N2气体生成1mol气态N4的△H为
A.+882kJ·mol-1 B.+441kJ·mol-1 
C.-882kJ·mol-1 D.-441kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com